Brain: 阿尔茨海默病血液检测大PK——Lumipulse与ALZpath SIMOA,谁更胜一筹?
2025-04-07 MedSci原创 MedSci原创
这项研究为AD的早期诊断带来了新的希望。
阿尔茨海默病(AD)是一种起病隐匿的神经退行性疾病,随着全球人口老龄化加剧,它已成为威胁老年人健康的"沉默杀手"。据统计,目前全球约有5000万AD患者,预计到2050年这一数字将增长至1.52亿。然而,这种疾病的早期诊断一直面临巨大挑战——传统的诊断方法要么需要昂贵的PET扫描,要么要通过痛苦的腰椎穿刺获取脑脊液,不仅费用高昂,还让很多患者望而却步。
近年来,医学界在血液生物标志物研究方面取得重大进展。其中,血液中的磷酸化tau蛋白(p-tau217)因其与AD病理的高度相关性,被视为最具潜力的诊断标志物。研究表明,p-tau217不仅能准确区分AD与其他类型的痴呆,甚至可以在临床症状出现前15-20年就检测到异常变化。这一发现让科学家们兴奋不已,因为这意味着未来可能通过简单的抽血就能实现AD的早期筛查。

然而,在实际临床应用前,一个重要问题亟待解决:目前市场上不同的检测技术,究竟哪一种更可靠?最近发表在权威期刊上的一项研究给出了答案。这项研究由国际知名科研团队开展,共纳入392名参与者,其中包括162名经临床确诊的AD患者、70名其他神经退行性疾病患者(通过脑脊液生物标志物确认)和160名健康对照者。研究人员采用目前最先进的两种检测技术——全自动化的Lumipulse系统和半自动化的ALZpath SIMOA系统,对所有受试者的血浆p-tau217水平进行了检测和对比。
研究结果令人振奋。数据显示,两种技术测得的p-tau217水平具有高度一致性,相关系数达到0.9以上。在诊断效能方面,两者表现同样出色:在区分AD患者与其他神经退行性疾病患者时,Lumipulse系统的准确率(AUC)为0.952,SIMOA系统为0.955;在区分AD患者与健康人群时,两者的准确率都在0.937左右。这些数据表明,无论采用哪种检测技术,p-tau217都能以超过90%的准确率识别AD患者。
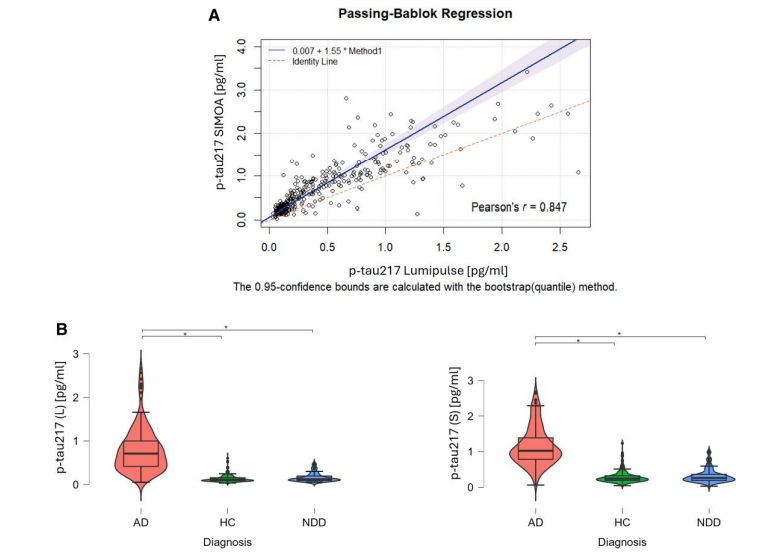
值得注意的是,这两种技术各有优势。全自动化的Lumipulse系统操作简便,适合在医院检验科开展大规模检测,2小时内就能完成近百份样本的分析;而SIMOA系统则凭借其"单分子阵列"技术,具有更高的灵敏度,更适合科研场景下的微量样本检测。研究人员还发现,两种技术测得的结果都与脑脊液中p-tau181的水平高度相关,这进一步验证了血液检测的可靠性。
这项研究为AD的早期诊断带来了新的希望。随着今年7月美国FDA批准首款基于p-tau217的AD血液检测试剂盒,这种无创、便捷的检测方法距离临床应用又近了一步。
原始出处:
Andrea Pilotto, et al, Plasma p-tau217 in Alzheimer’s disease: Lumipulse and ALZpath SIMOA head-to-head comparison, Brain, Volume 148, Issue 2, February 2025, Pages 408–415, https://doi.org/10.1093/brain/awae368

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





















#阿尔茨海默病# #血液标志物#
14