【衡道丨文献】他山之石:首款Claudin18.2靶向药物获批,胃癌治疗新靶点的免疫组化检测该如何进行?
9小时前 衡道病理 衡道病理 发表于陕西省
我国首个 Claudin18.2 靶向药获批,目前正编相关共识文件。介绍胃及胃食管交界处腺癌 Claudin18.2 免疫组化检测各方面要求,附图例赏析,提供对应参考文献。
近日,注射用佐妥昔单抗联合方案顺利通过了中国国家药品监督管理局(NMPA)的审批,成为中国首个获批的Claudin18.2靶向治疗药物,为我国胃癌患者提供了一种更加精准靶向的治疗选择。在胃及胃食管交界处腺癌的靶向治疗中,Claudin18.2免疫组化检测已成为进展期/转移性病例相应单克隆抗体治疗的重要一环。然而,当前却并没有关于这一指标检测的相应指南。据悉,目前国内相关学术团队正积极编纂关于Claudin18.2在晚期胃癌检测中的相关共识性文件。
2023年5月至7月,一个来自世界各地的国际性病理医师专家组对51例相应病例HE切片及Claudin18.2免疫组化切片进行了评阅和讨论,最后形成了胃及胃食管交界处腺癌Claudin18.2免疫组化检测的相关共识性意见。目前,相关文献已发表于《Mod Pathol》杂志。

为帮助大家更好的了解相关信息,武汉市黄陂区中医医院病理科王强医师将该文要点编译介绍如下。
胃及胃食管交界处腺癌免疫组化Claudin18.2评估注意事项
标本要求
1. 对于原发肿瘤的活检标本来说,至少应评估6个组织片;如果组织较少,应对所有取得的肿瘤组织标本都进行检测;
2. 只有浸润性腺癌成分才考虑进行评分;要避开仅有异型增生/非浸润性病变的标本;
3. 至少应评估50个恶性细胞;但积液细胞学标本中建议至少应评估100个恶性细胞;
4. 配对的原发及转移性病变中,Claudin18.2的表达高度一致;选择最适用的标本即可;
5. 混合型腺癌中,选择包括不同表型的有代表性的标本进行检测;
6. 拟做电镜、或未固定的标本,不能做Claudin18.2免疫组化检测。
检测方案要求
1. 免疫组化Claudin18.2的检测应在常规处理的、福尔马林固定、石蜡包埋组织中进行;
2. 未染色的切片(白片)中,抗原稳定性可以至少维持45天;根据每一个实验室的具体验证研究,可以适当延长;
3. 亚基特异性抗体或针对Claudin18全长的抗体都可以得出差不多的结果,因为Claudin18.1亚基在胃组织中的表达可以忽略。
染色结果评估
1. Claudin18.2明确的细胞膜着色(环周、基底侧、或侧方),即可判定相应细胞为阳性;
2. 胞质颗粒状着色判为阴性;
3. 着色强度记为0-3+,无着色为0,弱阳性为1+,中等程度阳性为2+,强阳性为3+;
4. 3+的着色强度,是指(DAB做显色剂的情况下)强棕色着色、低倍镜(5倍物镜)下呈显著鸡笼状分布;
5. Claudin18.2的免疫组化着色在肿瘤内具有高度异质性;
6. 应在低倍镜下全面评估、确定总体的表达情况和表达的异质性;
7. 正常的胃部腺体为Claudin18.2阳性,对于具体标本来说,着色强度呈混合型表现;
8. 如果标本中无任何着色、且无着色的腺癌中内对照的非肿瘤组织无阳性着色,应考虑假阴性;建议重复检测、或(如果可能的话)另选组织块进行检测;
9. 前驱病变(肠化生、异型增生)也可表达Claudin18.2,但不要纳入结果评分;
10. 肿瘤细胞≥75%的呈中至强(2+或3+)阳性细胞膜着色,是临床可以应用相应单克隆抗体佐妥昔单抗(zolbetuximab)治疗的阈值;
11. 对于低黏附性癌来说,免疫组化Claudin18.2评估时强烈建议要结合相应的HE染色切片;
12. 一位病理医师首次评估结果为60-80%的癌细胞为2+或3+时,应由第二位病理医师复阅;
13. 结果不明确的情况下,应解读为不足以得出Claudin18.2免疫组化评分结果,应另选标本再次检测及评分。
结果的报告
1. 用于检测的标本类型(活检标本、还是手术标本),标本的部位(原发灶,还是转移灶;如果是转移灶,需注明部位);
2. 标本是否充分;如果不充分,注明原因;
3. 检测所用的抗体克隆号以及免疫组化染色方案;
4. 是实验室自建检测项目(Laboratory Developed Test,LDT)、还是伴随诊断(Companion Diagnostic,CDx);
5. 结果应报告中至强阳性(2+或3+)细胞膜着色的肿瘤细胞所占比例,并备注阳性阈值是这类细胞占比≥75%。
图例赏析
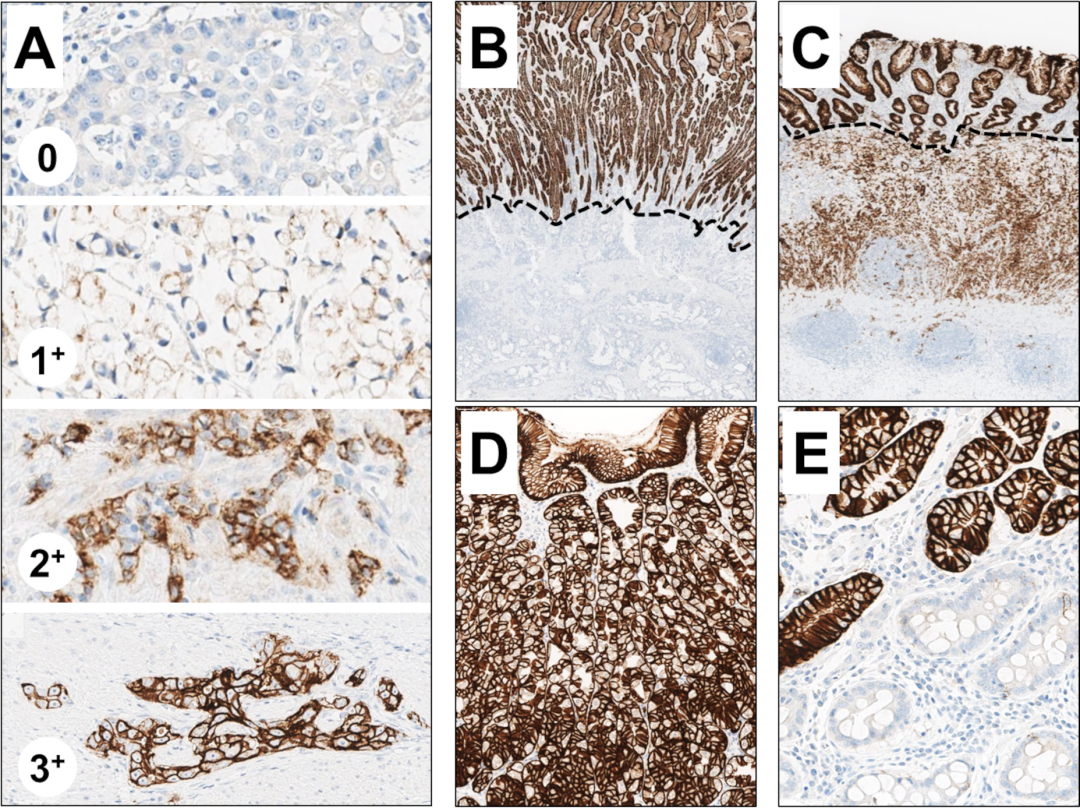
图1. 免疫组化Claudin18.2着色强度示例。(A)胃癌细胞中,0-3+的示例;(B)非肿瘤的胃部腺体(虚线上部分)为细胞膜强阳性着色,和肿瘤(虚线下部分)中的阴性着色形成对比;(C)非肿瘤的胃部腺体(虚线上部分)为细胞膜强阳性着色,本例肿瘤(虚线下部分)也是阳性着色;(D)正常胃部腺体着色高倍观,细胞膜强阳性,呈鸡笼状分布;(E)萎缩性胃炎标本中,局灶肠上皮化生区域免疫组化Claudin18.2阴性,非肠化腺体为阳性着色。
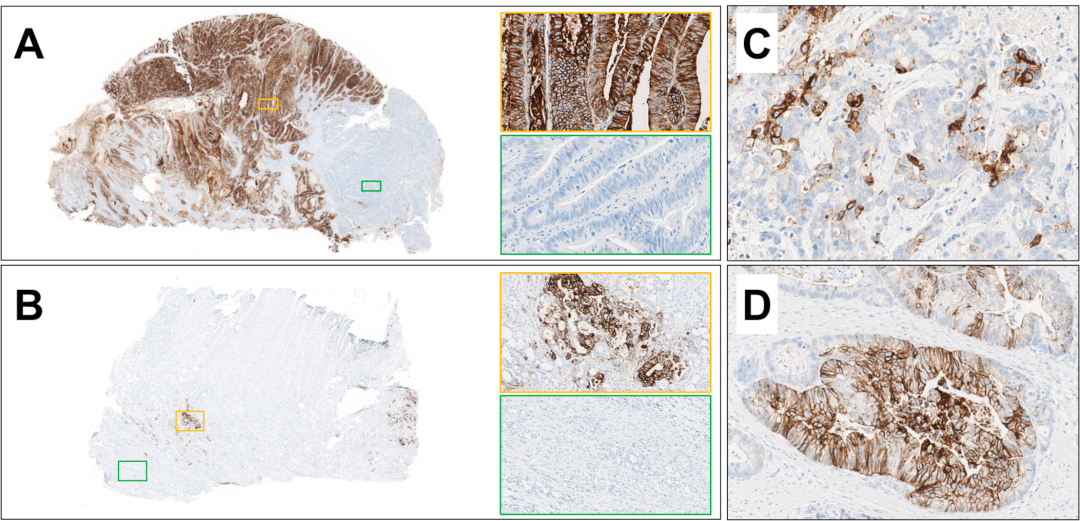
图2. 胃癌中免疫组化Claudin18.2着色的异质性。(A、B)两例具有显著肿瘤异质性的胃腺癌,部分区域为强阳性着色,而同时有部分区域为完全不着色;(C、D)腺体内免疫组化Claudin18.2着色异质性。
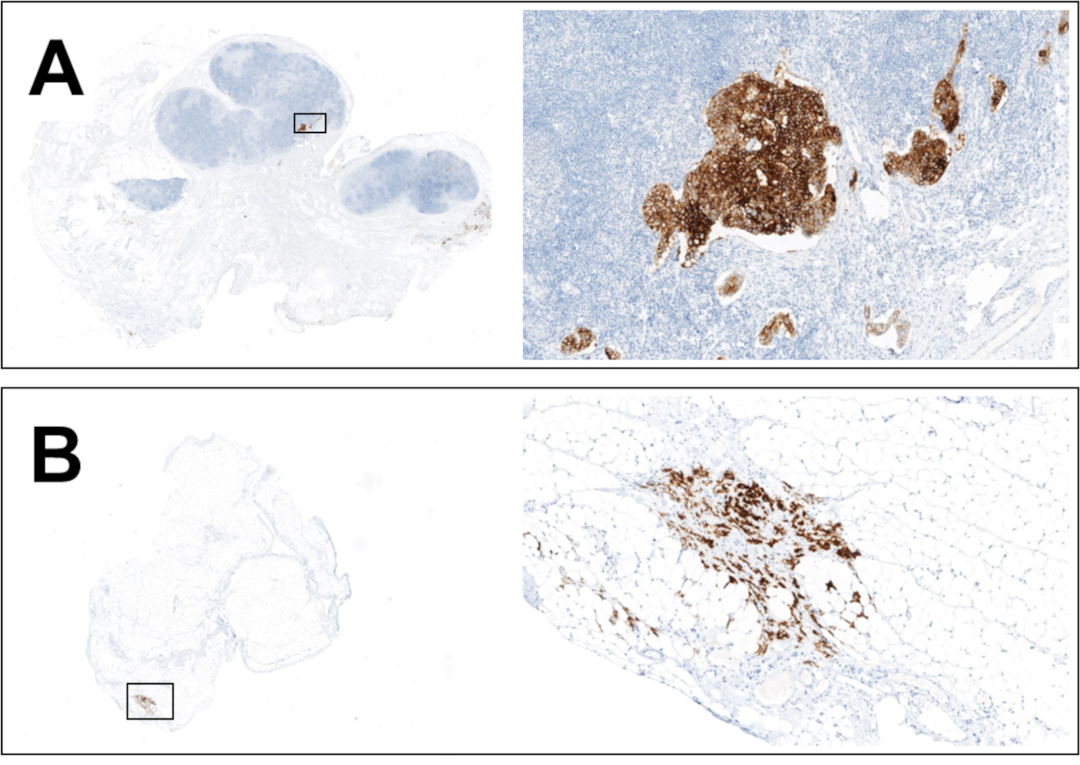
图3. Claudin18.2阳性的转移性腺癌。(A)淋巴结微转移;本例需结合相应的HE染色切片才能准确评估肿瘤范围;转移灶极少,但Claudin18.2却为明确的3+;(B)腹膜转移,转移灶极小;做Claudin18.2评分的话,建议至少应有50个肿瘤细胞供评估(最好100个细胞)。
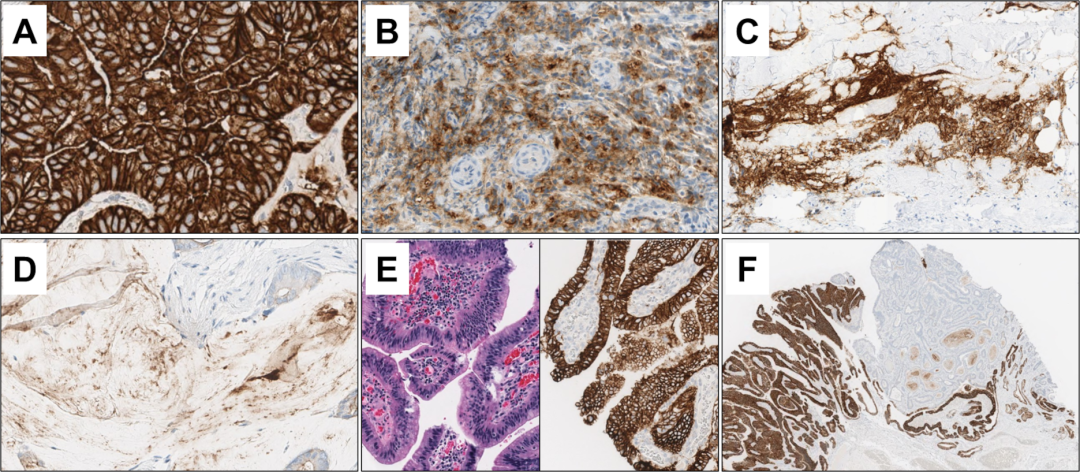
图4. 免疫组化Claudin18.2评估中可能存在的陷阱。(A)Claudin18.2强阳性的腺癌中,胞质广泛着色,会导致细胞膜着色评估困难;(B)呈胞质颗粒状着色的胃癌;(C)Claudin18.2阳性腺癌中的烧灼假象;(D)无细胞黏液中呈微弱至中等的表达;(E)低级别异型增生,呈弥漫、强阳性着色;(F)低级别和高级别异型增生,着色模式不一致;图中所有上皮成分都有异型增生。
参考文献及书籍:
Fassan M, Kuwata T, Matkowskyj KA, Röcken C, Rüschoff J. Claudin-18.2 Immunohistochemical Evaluation in Gastric and Gastroesophageal Junction Adenocarcinomas to Direct Targeted Therapy: A Practical Approach. Mod Pathol. Published online August 2, 2024.
doi:10.1016/j.modpat.2024.100589
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#胃癌# #Claudin18.2 #
4