Circ Res 香港中文大学生物医学学院田小雨教授团队揭示PPARδ调控急性肺损伤中血管内皮通透性的新机制
2025-02-28 论道心血管 论道心血管 发表于陕西省
该研究阐明了PPARδ在血管内皮屏障功能中的调控作用,并探讨其在ALI中的潜在保护机制。
脓毒症是一种危及生命的综合征,由感染引发的炎症反应失控导致多器官功能障碍。脓毒症中的急性肺损伤(ALI)以破坏肺泡-毛细血管屏障为特征,导致白细胞渗出、水肿形成和缺氧,最终可能发展为严重的急性呼吸窘迫综合征(ARDS)。目前尚无针对脓毒症相关ALI的有效治疗方法,研究维持血管屏障完整性的分子机制,将有助于开发新的治疗策略。
2025年2月25日,香港中文大学生物医学院田小雨教授团队在Circulation Research杂志在线发表题为“Endothelial PPARδ Ablation Exacerbates Vascular Hyperpermeability via STAT1/CXCL10 Signaling in Acute Lung Injury”的研究论文。该研究阐明了PPARδ在血管内皮屏障功能中的调控作用,并探讨其在ALI中的潜在保护机制。

首先,研究人员采用内皮细胞特异性PPARδ敲除小鼠和对照小鼠,并通过脂多糖(LPS)诱导ALI。结果显示,内皮细胞PPARδ敲除小鼠的肺部炎症明显加重,表现为白细胞浸润增多、促炎细胞因子(TNFα、IL-6、IL-12)水平升高,以及更高的死亡率。此外,PPARδ缺失导致血管内皮通透性增加,肺组织蛋白渗漏加剧,间质水肿,并伴随内皮细胞间紧密连接蛋白下调,表明PPARδ在维持内皮屏障功能中的关键作用。
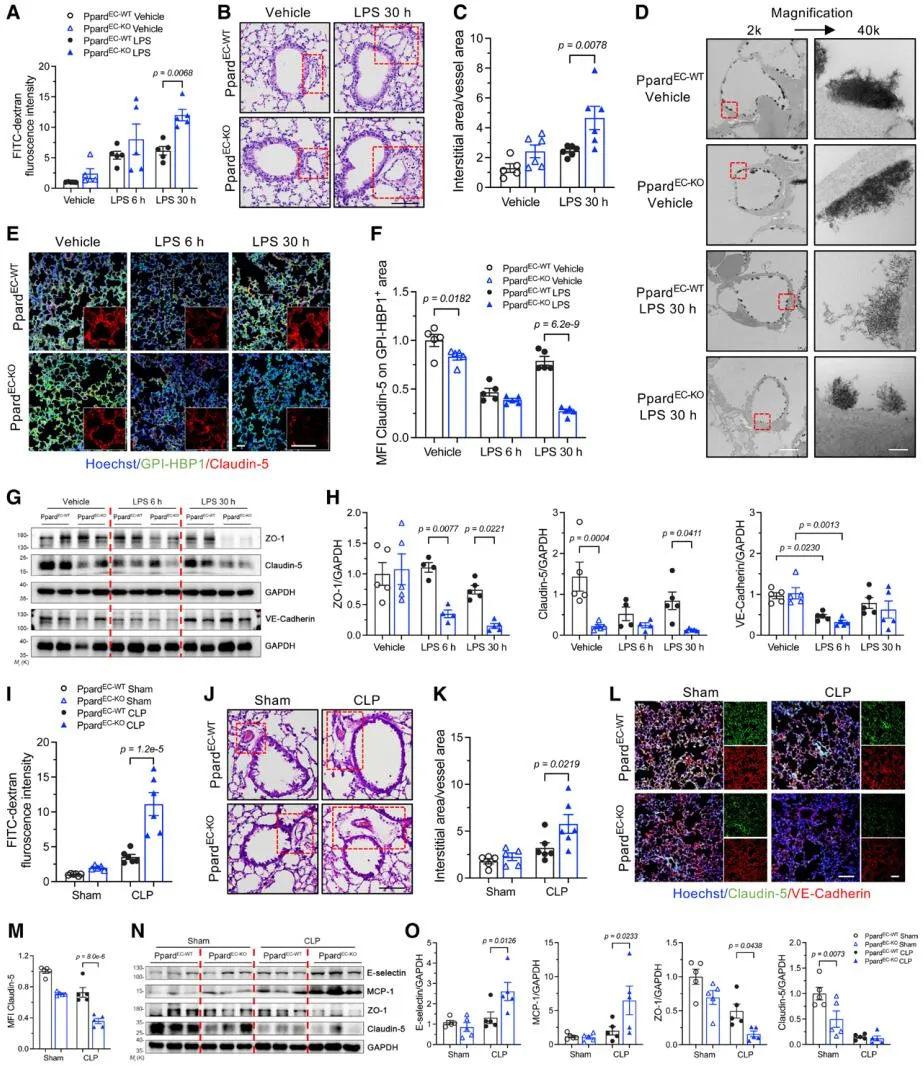
PPARδ缺失加剧LPS引起的肺部血管内皮通透性
对肺血管内皮细胞进行单细胞RNA测序分析发现,在内皮细胞PPARδ敲除小鼠中,LPS诱导了一种干扰素活化的毛细血管内皮细胞亚群,该亚群特征性地表达高水平的CXCL10。进一步研究表明,沉默PPARδ通过激活STAT1信号通路显著增加CXCL10的表达,CXCL10则通过泛素-蛋白酶体系统降解紧密连接蛋白ZO-1和Claudin-5,从而破坏细胞间连接,导致血管通透性增加。

scRNA-seq揭示CXCL10介导的内皮细胞屏障损伤
研究人员进一步评估阻断CXCL10/CXCR3信号传导能否保护血管内皮屏障功能并减轻LPS 介导的肺损伤。实验结果表明,应用抗CXCL10中和抗体或CXCR3拮抗剂AMG487,可有效减少PPARδ敲除小鼠中的T细胞浸润,降低炎症水平,并显著改善肺部血管屏障功能。此外,微型CT扫描显示,CXCL10中和抗体可减少LPS诱导的肺部水肿,并恢复紧密连接蛋白的表达。这些结果表明,CXCL10/CXCR3信号通路可能是治疗ALI的潜在靶点。

阻断CXCL10/CXCR3可改善肺部炎症反应及血管屏障功能
综上,该研究揭示了PPARδ在内皮细胞中通过抑制STAT1/CXCL10信号通路的激活发挥了对血管屏障功能的保护作用。CXCL10通过介导紧密连接蛋白的降解破坏细胞间连接完整性。使用抗CXCL10中和抗体或CXCR3拮抗剂AMG487阻断CXCL10/CXCR3信号通路,可抑制肺血管屏障功能紊乱和内皮炎症。该研究阐明了PPARδ调控ALI中肺血管通透性增加的分子机制,揭示阻断CXCL10信号可能是治疗脓毒症介导的急性肺损伤的潜在治疗策略。

香港中文大学生物医学学院田小雨教授为该论文通讯作者,洪慧玲博士和伍亚蓝博士为该论文共同第一作者。该工作得到了香港研究资助局研究基金、香港中文大学研究系列基金、香港中文大学罗桂祥生物医学研究基金(初创)、国家自然科学基金、中国广东省科技计划等项目的资助。
原文链接:
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.124.325855

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#急性肺损伤# #PPARδ#
8