Neurocritical Care:我国学者揭示基于年龄分层分析微循环功能障碍对动脉瘤性蛛网膜下腔出血后持续性脑水肿的影响
2025-03-25 Selene MedSci原创 发表于陕西省
微循环功能障碍与 aSAH 后持续性 GCE 风险增加之间存在年龄依赖性关联,这为未来研究研究不同年龄的定制治疗提供了有希望的见解。
动脉瘤性蛛网膜下腔出血 (Aneurysmal subarachnoid hemorrhage,aSAH) 是一种严重的卒中亚型,对幸存者的功能独立性和生活质量有长期影响。近年来,越来越多的证据表明,早期脑损伤 (early brain injury ,EBI) 是动脉瘤破裂诱导的病理过程的结果,是 aSAH 后不良预后的关键因素。尽管评估 EBI 的谱系存在挑战,但脑水肿 (global cerebral edema,GCE) 已得到广泛认可,并且是 EBI 的重要可识别影像学标志物。先前的研究表明,aSAH 后入院 GCE 的发生率约为 6-57% ,约 12% 的患者在平均 6 天内出现迟发性脑水肿。重度 GCE 患者入院时 GCE 消退的中位时间为 8 日。因此,入院时和 1 周左右都存在 GCE 可能在某种程度上表明 aSAH 后脑损伤的持续过程。
此外,GCE 的机制复杂且未得到充分探索。微循环功能障碍是 GCE 的机制之一 。既往研究表明,大脑前动脉 A2 段或大脑中动脉 M2 段与矢状窦上段达到峰值的时间差可以在一定程度上作为评估微循环损伤的指示性指标。计算机断层扫描灌注(Computed tomographic perfusion,CTP) 可实现时间分辨的血管成像数据,从三相最大强度投影重建得出的时间密度曲线描述了动脉流入、动静脉传输过程和静脉流出的综合概况。因此,CTP 被认为是评估动静脉峰值时间(peak time,DV) 差异值的可靠方法,DV 定义为大脑前动脉 A2 段峰值对比与矢状窦上段之间的时间间隔。然而,迄今为止还没有研究调查微循环损伤对持续性 GCE 的影响。此外,年龄是 GCE 测量的一个关键混杂参数,与年轻患者相比,由于年龄相关性动脉粥样硬化,老年患者的大脑自动调节能力较差,血管顺应性受损,使他们更容易出现严重和持久的微循环功能障碍和随后的组织缺氧,最终导致持续的GCE。
1月7日,首都医科大学赵性泉教授团队xing在Neurocritical Care(if=3.1)在线发表了题为“Impact of Microcirculatory Dysfunction on Persistent Global Cerebral Edema After Aneurysmal Subarachnoid Hemorrhage: An Age-Stratified Analysis”的研究,目的是调查从 CTP 获得的 DV 是否与不同年龄组 aSAH 患者的持续性 GCE (即较低的 SSV) 相关。结果发现微循环功能障碍与 aSAH 后持续性 GCE 风险增加之间存在年龄依赖性关联,这为未来研究研究不同年龄的定制治疗提供了有希望的见解。

该研究于 2020 年 10 月至 2023 年 7 月在北京天坛医院进行。前瞻性纳入发作后 24 小时内接受计算机断层扫描灌注的 aSAH 患者。作为微循环障碍指标的动静脉峰值时间 的差异值来自 CTP 的时间密度曲线。持续性 GCE 定义为入院时和发作后 7 ± 1 天的选择性脑沟体积≤ 11.3 mL。应用年龄分层多变量分析来确定微循环功能障碍与持续性 GCE 之间的关联。
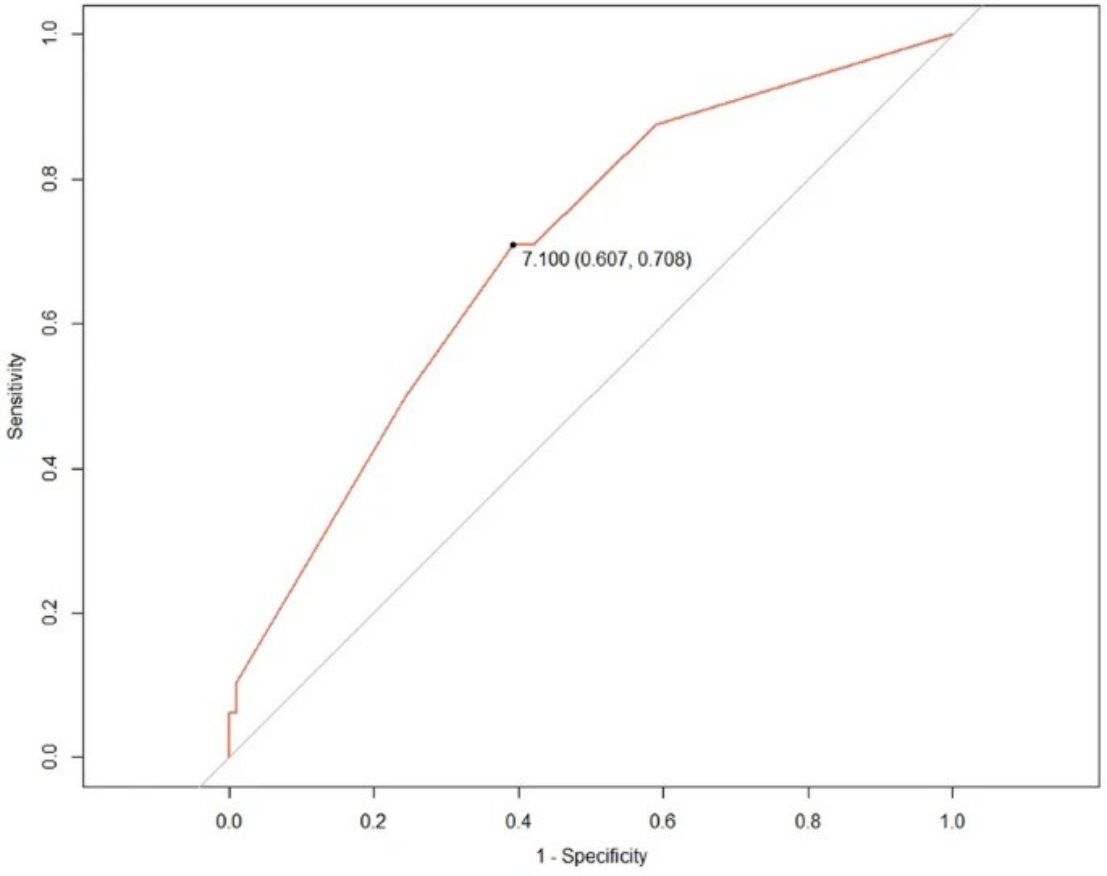
DV 的受试者工作特征曲线预测动脉瘤性蛛网膜下腔出血后持续性整体脑水肿
本研究的主要发现是,在 60 岁以上的患者中,CTP 时间强度曲线上的延长 DV 与 aSAH 后持续性 GCE 的风险增加显著相关。最重要的是,我们发现这种关联是年龄依赖性的,揭示了微循环功能障碍对 aSAH 后持续性 GCE 的影响对于年轻和老年患者来说并不相同。
微循环功能障碍是 aSAH 后 GCE 的潜在病理生理机制之一 本研究扩展了先前研究的结果,并首次发现 CTP 在 24 小时内检测到的 DV 也可以预测 60 岁以上患者 aSAH 后的持续性 GCE。
微循环变化(检测为 DV 延长)与持续性 GCE 相关的潜在解释可能如下。首先,DV 延长可能表明更严重的微循环损伤和更低的局部血流量。其次,aSAH 后蛛网膜下腔血液积聚导致 ICP 快速升高,可能导致自我调节受损和脑灌注压降低。第三,细胞毒性和血管源性脑水肿也可反过来引起微血管的机械压迫,从而加剧缺血性脑损伤和 GCE 的恶性循环。然而,在本研究中,延长的 DV 并不是所有纳入患者中持续性 GCE 的独立预测因子。当将研究人群限制在入院时的 GCE 个体进行进一步的敏感分析时,DV 和其他脑血流动力学指标仍然不是持续性 GCE 的预测因素。因此,这种现象表明 DV 或其他 CTP 成像标志物可能不是由脑水肿、ICP 升高或其他严重情况驱动的。在未来的研究中,应进一步研究微血管系统的潜在病理生理变化或导致脑血流动力学过程紊乱和持续性 GCE 后续发展的其他潜在因素。
在本研究中,观察到微循环损伤与持续性 GCE 之间的年龄依赖性关联。DV 对不同年龄组持续性 GCE 的预测价值可以阐明如下:一方面,老年 aSAH 患者的大脑自动调节能力较差。老年 aSAH 患者可能表现出对缺血性损伤和更严重的微循环功能障碍的更大易感性,从而由于组织氧的更明显减少,使他们易患随后的细胞毒性和血管源性脑水肿。相反,年轻患者表现出更强的适应性和更健康的脑血管,可以有效地调节脑血流以响应代谢需求,从而减少 aSAH 后的缺血性脑损伤。此外,衰老与脑血流量下降有关。因此,与老年患者相比,年轻患者的脑血流储备更充足。考虑到更好的大脑自动调节和更充足的脑血流储备,可以推测 aSAH 后年轻患者的微循环损伤和随后的组织缺氧可能是短暂的和可逆的,使他们不易发生持续性 GCE。
总之,检测为 DV 延长的微循环功能障碍与 60 岁以上患者 aSAH 后持续性 GCE 的风险增加显著相关。在 60 岁以下的患者中未观察到这种关联。本研究阐明了微循环功能障碍对持续性 GCE 的年龄特异性影响,这为未来的研究提供了有希望的见解,以调查不同年龄组的定制治疗。
原始出处:
Impact of Microcirculatory Dysfunction on Persistent Global Cerebral Edema After Aneurysmal Subarachnoid Hemorrhage: An Age-Stratified Analysis. Neurocrit Care. 2025 Jan 7. doi: 10.1007/s12028-024-02188-8. Epub ahead of print. PMID: 39776342.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#年龄# #动脉瘤性蛛网膜下腔出血# #脑水肿# #微循环功能障碍#
7