卵巢癌中HRR相关基因胚系变异的发生率为12.8%,浆液性癌和III/IV期患者中更为常见
2025-04-06 苏州绘真医学 苏州绘真医学
本研究旨在确定EOC患者中与癌症易感性相关基因的变异频率,确定与这些基因PVs相关的临床特征,并根据HRR状态评估它们对预后的影响。
胚系致病性变异(PVs)在妇科肿瘤学中至关重要。本研究关注上皮性卵巢癌(EOC)患者中同源重组修复(HRR)PVs的发生率、临床病理特征以及对生存的影响。这是一项多中心回顾性队列研究,共登记了1248例EOC患者。符合条件的患者(n = 1112)进行了胚系DNA分析,以检测26种癌症易感基因,其中包括9种HRR相关基因,如BRCA1/2、BRIP1、PALB2、RAD51C/D和ATM。本研究分析了临床病理因素与HRR相关致病性变异之间的关联,并进行了 Kaplan-Meier 分析和 Cox 回归分析。在1091例接受分析的患者中,153例(14.0%)携带致病性变异,其中140例(12.8%)与HRR相关。HRR PV阳性状态与浆液性癌显著相关(22.9% vs. 4.8%,P < 0.0001),也与疾病晚期显著相关(18.5% vs. 5.9%,P < 0.0001)。HRR PV阳性组的个人乳腺癌病史(12.9%)和家族性乳腺癌/卵巢癌病史(29.2%)的发生率更高。在III/IV期疾病中,HRR状态独立地改善了总生存期(OS,P = 0.04),但对无进展生存期(PFS)没有影响。HRR相关胚系PVs表现出独特的临床病理特征,并对生存有影响。这些变异与浆液性癌和晚期疾病显著相关,强调了基因检测对于制定个性化EOC治疗策略的重要性。考虑到本研究的时间范围(2000年-2019年),应该认识到贝伐珠单抗和PARP抑制剂作为维持治疗的使用有限。
研究背景
EOC在2022年约有324398例新发病例,全球每年有206839人死于该病。EOC是全球女性中与癌症相关的死亡率第八高的病因。据报道,所有EOC病例中约10%-15%源于胚系BRCA PVs,而在高级别浆液性亚型中,约20%-25%的病例存在胚系BRCA PVs。
下一代测序技术的进步已确定了11个与遗传性卵巢癌相关的基因。美国临床肿瘤学会指南建议评估至少六个HRR相关基因,包括BRCA1、BRCA2、RAD51C、RAD51D、BRIP1和PALB2,以及四个错配修复(MMR)缺陷相关基因,即MLH1、MSH2、MSH6和PMS2。在这些基因中,BRCA1、BRCA2、RAD51C、RAD51D和BRIP1与DNA HRR通路相关。HRR通路缺陷(同源重组缺陷)是由它们的功能缺失引起的。携带胚系BRCA1/BRCA2 PVs的患者预后更好,因为他们对化疗的反应更好。Bolton等人报告称,携带BRCA1或BRCA2胚系PVs的患者5年总生存率有所提高(非携带者为36%,BRCA1携带者为44%,BRCA2携带者为52%)。SOLO-2研究是一项双盲、随机、安慰剂对照的3期试验,该研究证实,对于携带BRCA1/2 PV的铂敏感复发性卵巢癌患者,奥拉帕利与安慰剂相比可带来约12.9个月的生存获益。其他临床试验表明,使用PARP抑制剂(PARPi)治疗可带来显著的生存获益,尤其是在携带BRCA1/2 PVs和/或存在同源重组缺陷的患者中。然而,关于这些非BRCA HRR相关PVs与临床特征之间关系的信息有限。此外,关于非HRR相关基因变异的数据也有限。
下一代DNA测序技术能够在短时间内同时分析多个基因。研究已确定RAD51D、PTEN、TP53、BRIP1、RAD51C、MSH6和MSH2 PVs是卵巢癌和乳腺癌的高危因素。此外,已对12个乳腺癌和/或卵巢癌易感基因的胚系PVs进行了研究;对于BRCA1/2以外的基因,突变频率≤1.0%,只有PALB2与患病风险有显著关联(OR为5.79,95%CI为1.09-30.83)。对于卵巢癌特异性死亡,BRCA1对应的HR为0.61(95%CI为0.34-1.11),BRCA2对应的HR为0.82(95%CI为0.51-1.29)。
对卵巢癌患者胚系变异的分析显示,携带胚系突变的患者,尤其是携带BRCA1/2 PVs的患者,OS明显更长。此外,还对BRCA1/2以外基因的PVs进行了研究,包括非同源重组修复相关基因,如MSH6、BRIP1、PMS2、TP53和MLH1。除BRCA1/2外,卵巢癌易感基因中遗传性PVs的临床特征尚不完全清楚。
本研究旨在确定EOC患者中与癌症易感性相关基因的变异频率,确定与这些基因PVs相关的临床特征,并根据HRR状态评估它们对预后的影响。
研究结果
患者特征:
日本四个医疗中心共有1248名被诊断为EOC的患者被纳入了这个队列。如图1所示,排除了136名患者,随后对1112名患者的胚系DNA进行了26种癌症易感基因的多基因panel检测,并确定了PVs。其中,有21名患者因测序失败而被排除。最终,1091名患者被纳入了该研究。
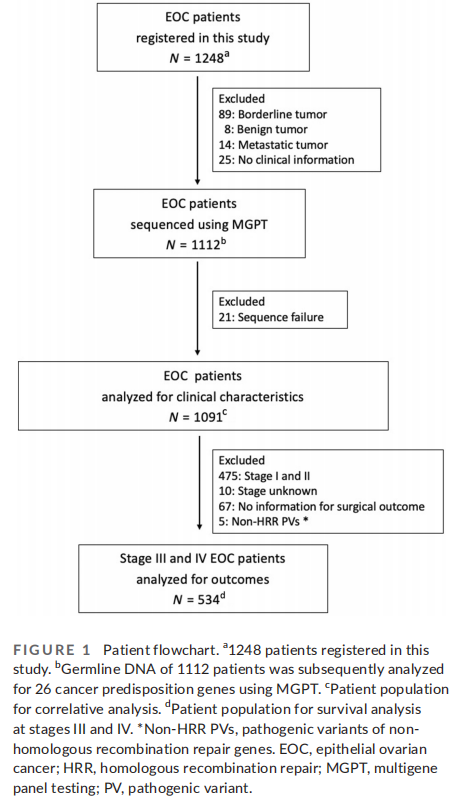
图1
患者特征见表1。诊断时的中位年龄为58岁(范围19-89岁)。浆液性癌是最常见的组织学类型(n = 484,占44.3%),其次是透明细胞癌(n = 244,占22.3%)。在数据库中,无法区分浆液性癌的分级。在总体人群中,55.5%的患者被诊断为III/IV期疾病。分别有50名(4.5%)和27名(2.4%)患者先前有乳腺癌和子宫内膜癌的病史。分别有95名(8.7%)和43名(3.9%)患者的一级或二级亲属患有乳腺癌或卵巢癌,16名(1.4%)患者既有乳腺癌病史又有卵巢癌病史。在一线化疗中,933名(85.5%)患者接受了铂类化疗。其中,分别有24名和1名患者使用了贝伐珠单抗和PARPi。
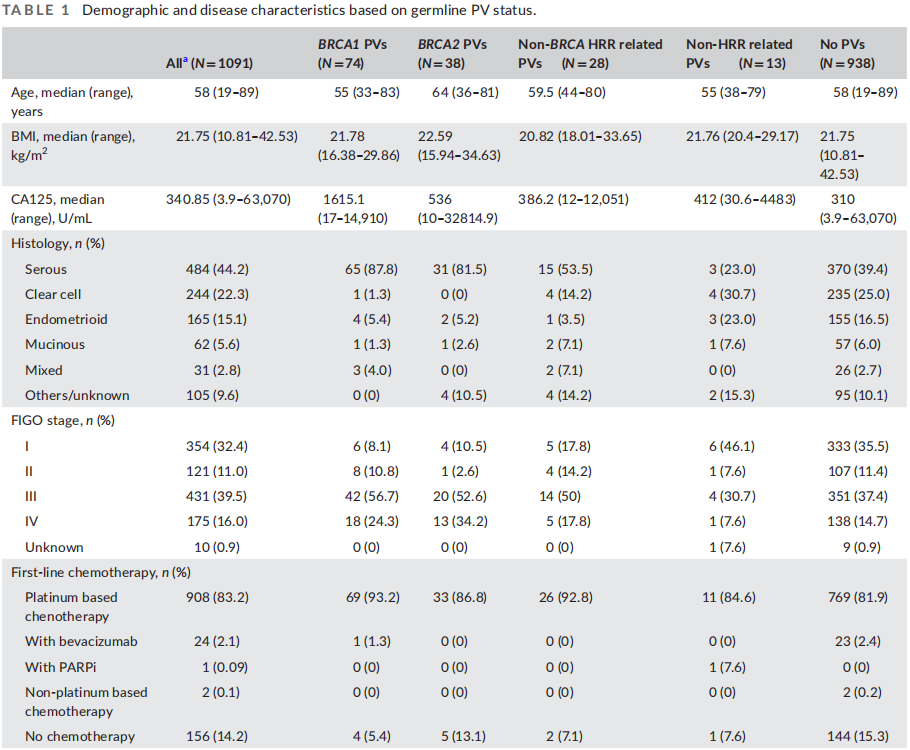
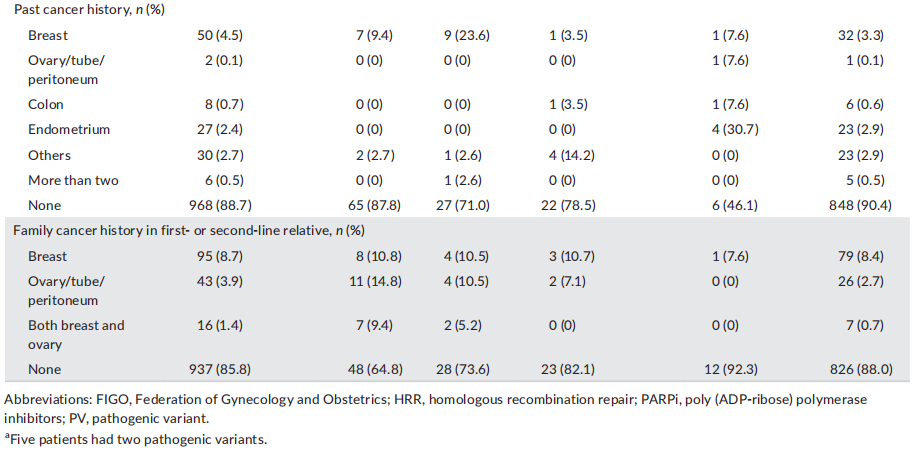
表1
胚系致病性变异的频率:
在接受检测的1091名EOC患者中,有153名患者在分析的26个基因中的任何一个基因中发现了PVs。5名患者有两种PVs,在这个队列中共鉴定出了158种PVs。检测panel中26个基因的PVs被分为HRR PVs组(BRCA1、BRCA2、BRIP1、PALB2、RAD51D、RAD51C、BARD1、ATM、CHEK2)和non-HRR PVs组(TP53、MLH1、MSH2、MSH6、PMS2、EPCAM、MUTYH、NF1、APC、PTEN、BMPR1A、CDH1、CDH4、CDKN2A、NBN、SMAD4、STK11)。在这个队列中,未在CHEK2、BMPR1A、CDH1、CDH4、CDKN2A、NBN、SMAD4和STK11中检测到PVs。5名有两种PVs的患者的详细情况如下:BRCA1和BRCA2、BRCA1和RAD51、BRCA1和MUTYH、RAD51C和NF1、BARD1和TP53。
如表1、图2A所示,在140名(12.8%)患者中观察到了HRR PVs。BRCA1(n = 74,占6.8%)是最常观察到的PVs,其次是BRCA2(n = 38,占3.5%)。在28名患者(2.6%)中观察到了Non-BRCA HRR PVs。在Non-BRCA HRR PVs组中,最常观察到的基因是RAD51D(10名患者),其次是ATM(7名患者)。至于non-HRR PVs变异,在6名患者(0.5%)中检测到了包括EPCAM PVs在内的MMR基因。
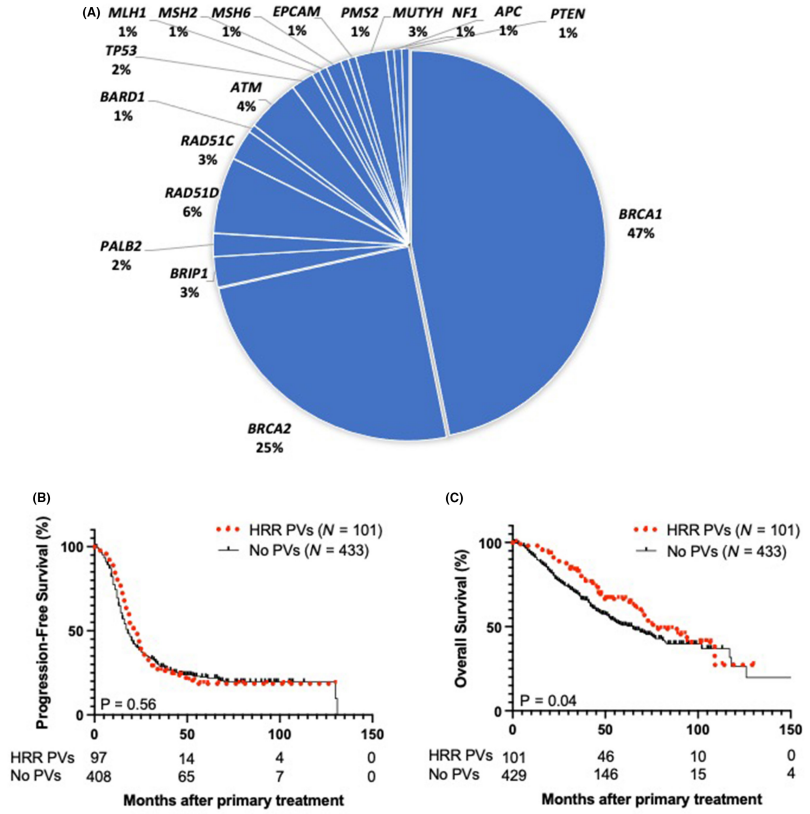

图2
HRR相关PVs与临床病理因素之间的关联:
表1和表2总结了基于临床和病理因素的PVs频率。对每个因素的HRR PVs状态进行了研究。未发现HRR PVs阳性与年龄或体重指数之间存在关联。HRR阳性组的血清CA125水平也高于HRR阴性组(883 U/mL vs.311 U/mL,P = 0.0076)。与其他组织学类型相比,HRR PVs大多在浆液性癌中观察到(22.9% vs. 4.8%,P < 0.0001)。在484名浆液性癌患者中,分别有65名(13.4%)和31名(6.4%)患者有BRCA1和BRCA2 PVs。在浆液性癌患者中也观察到了15名(3.0%)非BRCA HRR PVs患者。在III/IV期疾病患者中也观察到了更高频率的HRR PVs(18.5% vs. 5.9%,P < 0.0001)。
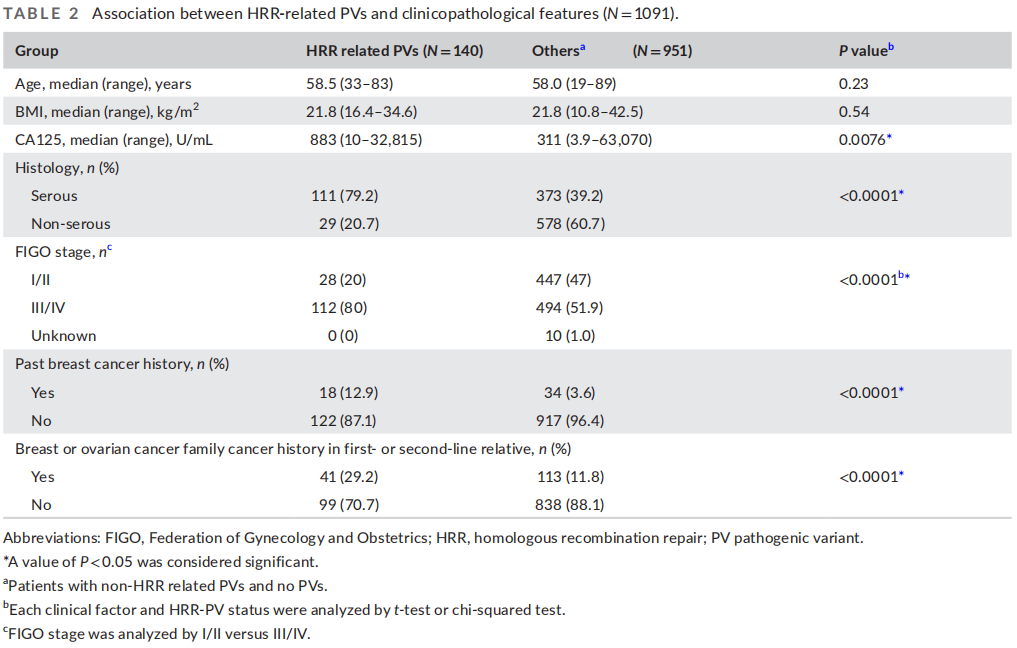
表2
HRR阳性组中个人乳腺癌病史的比例高于HRR阴性组(12.9% vs. 3.6%,P < 0.0001)。此外,分别有20.2%、15.7%和10.7%的BRCA1、BRCA2和非BRCA HRR PVs患者的一级或二级亲属有乳腺癌病史。关于乳腺癌/卵巢癌家族史,29.3%的HRR阳性组患者有一级或二级亲属的乳腺癌/卵巢癌家族史,而HRR阴性组为11.9%(P < 0.0001)。在非HRR组中,仅在APC或MUTYH患者中观察到了癌症家族史。
生存分析:
HRR PVs可能对EOC患者的生存产生积极影响。研究者使用对数秩检验和Kaplan-Meier生存曲线比较了两组患者的生存率。
研究者比较了有HRR相关PVs(HRR阳性组)的患者和没有HRR相关PVs的患者。由于HRR PVs主要在III/IV期疾病患者中观察到,研究者对III/IV期卵巢癌患者进行了生存分析。分析中排除了患有林奇综合征和非HRR相关PVs的患者,因为他们的癌症生物学特性与没有PVs的患者不同。总共分析了534名III/IV期疾病患者。中位随访时间为49个月。研究者确定了101名(18.7%)有HRR PVs的患者。如图2B所示,HRR阳性组和无PVs组之间未观察到PFS差异(P = 0.56)。HRR阳性组和无PVs组的中位PFS分别为22个月和18个月。相比之下,HRR阳性组的中位OS明显长于无PVs组(78个月vs. 65个月,95%CI 1.034-1.913,P = 0.04)(图2C)。
随后,研究者将人群分为三组,(A)BRCA1/2 PVs患者,(B)BRCA1/2以外的HRR相关PVs患者,以及(C)无PVs患者,并进行了生存分析。如图3A、B所示,BRCA1/2 PVs组和无PVs组之间未观察到PFS和OS差异,但BRCA1/2 PVs组的OS可能更长(78个月vs. 65个月,P = 0.05)。
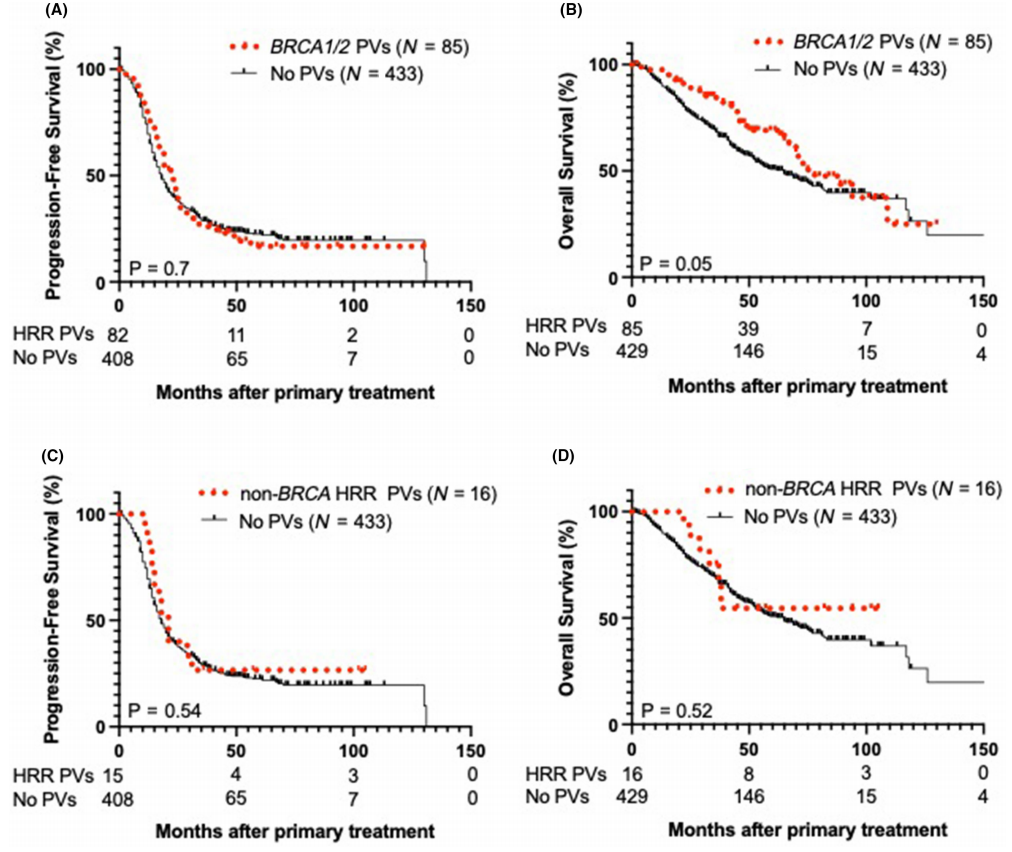

图3
非BRCA HRR PVs组和无PVs组之间未观察到PFS差异(21个月vs. 18个月,P = 0.54)。在这项分析中,非BRCA HRR PVs的患者数量有限,难以进行比较(图3C、D)。
表3显示了单因素和多因素Cox回归模型的结果。分析中纳入了年龄、HRR状态、FIGO分期、初始治疗类型和残留肿瘤状态。单因素分析显示,FIGO分期、初始治疗类型和残留肿瘤状态是PFS的重要指标。HRR状态、FIGO分期和残留肿瘤状态是OS的重要指标。在多因素分析中,初始治疗类型和残留肿瘤状态是PFS的独立预后因素,而HRR状态、FIGO分期和残留肿瘤状态是OS的独立预后因素。HRR状态是OS的独立因素,但不是PFS的独立因素。
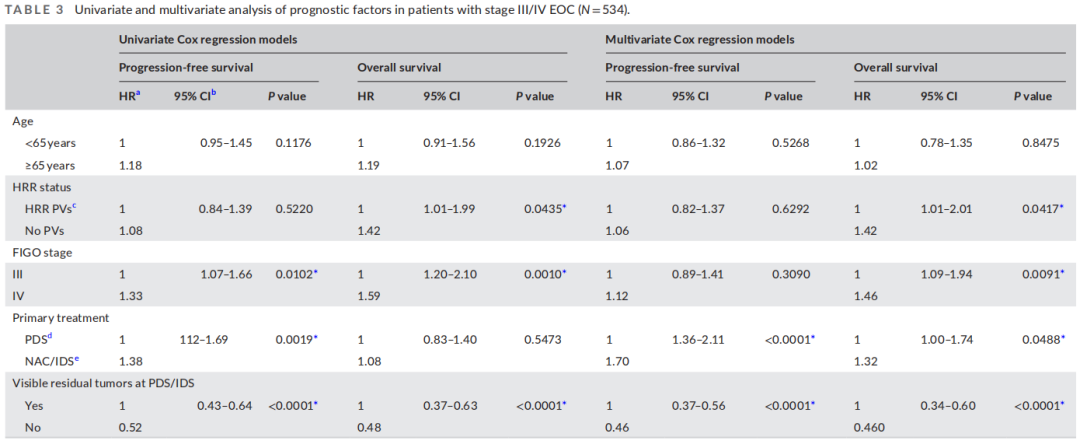
表3
此外,研究者通过将BRCA1、BRCA2、非BRCA HRR和非HRR PVs的每组患者与无致病性变异的患者进行比较,研究了它们对生存的潜在影响。与无PVs组相比,任何PVs组在PFS和OS方面均未显示出统计学上的显著影响。然而,BRCA1和BRCA2 PVs组的OS可能更长(BRCA1 vs. 无PVs,89个月vs. 65个月,P = 0.077;BRCA2 vs. 无PVs,78个月vs. 65个月,P = 0.36)。在这项分析中,非BRCA HRR和非HRR PVs的患者数量有限,难以进行比较。
讨 论
在本研究分析的1091名上皮性卵巢癌患者中,140名(12.8%)患者被检测出HRR相关基因的PVs,112名(10.3%)患者存在BRCA1/2PVs。在III/IV期疾病患者中,携带HRR相关PVs和BRCA1/2 PVs的患者分别占18.4%和15.3%。在存在PVs的患者中,74.5%(114/153)为浆液性癌患者。在浆液性癌患者中,HRR相关PVs和BRCA1/2 PVs的发生率分别为22.9%(111/484)和19.8%(96/484)。
与无PVs的患者相比,携带HRR相关PVs的患者OS有所改善,多因素分析表明,对于III/IV期疾病患者,HRR相关PVs是OS的独立预后因素。关于胚系BRCA1/2和/或HRR相关PVs的发生率,Norquist等人利用GOG218和262试验的数据,报告了卵巢癌患者中胚系BRCA及其他易感基因PVs的发生率。在这些试验中,95.5%的患者为III/IV期,在1915名患者中,14.6%存在BRCA1/2 PVs。他们还报告称,胚系非BRCA HRR相关基因和DNA错配修复基因的发生率分别为3.3%和0.4% 。本研究中BRCA1/2和非BRCA HRR PVs的发生率与先前报道的相似。胚系PVs的发生率在不同种族和/或地区之间可能存在差异。
目前尚无关于日本人群中胚系HRR相关PVs状态的报道。CHARLOTTE研究是一项日本多中心研究,该研究调查了上皮性卵巢癌患者中胚系BRCA1/2 PVs的发生率,结果显示,与全球人群相比,BRCA1/2 PVs的发生率相对较高。该研究发现,上皮性卵巢癌患者中14.7%(93/634)存在胚系BRCA1/2 PVs,III/IV期患者中24.1%(78/324)存在胚系BRCA1/2 PVs。与该研究相比,本研究中BRCA1/2 PVs的发生率相对较低。这可能是由于每项研究纳入的患者背景不同。在CHARLOTTE研究中,有乳腺癌和卵巢癌家族史(一级或二级)的患者比例分别为18.6%和5.7%,而在本研究中,这一比例分别为10.2%和5.4%。CHARLOTTE研究和本研究中患者的背景可能存在差异。CHARLOTTE研究可能纳入了更多有乳腺癌/卵巢癌家族史的患者,因为该研究是日本首次对上皮性卵巢癌患者的胚系BRCA1/2 PVs进行评估的研究。
已有多项研究报告了卵巢癌患者中胚系BRCA1/2 PVs的发生率及其家族史情况。Alsop等人报告称,在141名携带胚系BRCA1/2 PVs的患者中,75名(53.2%)有乳腺癌/卵巢癌家族史 。如前所述,在CHARLOTTE研究中,有乳腺癌和卵巢癌家族史(一级或二级)的患者比例分别为18.6%和5.7%。在携带BRCA1或BRCA2 PVs的患者中,64.5%有乳腺癌/卵巢癌家族史。在本研究中,32.1%的携带BRCA1/2 PVs的患者有一级或二级亲属的乳腺癌/卵巢癌家族史(P < 0.0001)。在HRR PVs阳性组中,癌症家族史的发生率为29.3%。尽管本研究是回顾性的,但在BRCA1/2 PVs阳性的患者中观察到了较高的癌症家族史发生率。仔细检查乳腺癌/卵巢癌家族史可能会增加胚系检测的数量,并发现更多HRR PVs阳性的患者。
HRR相关PVs在浆液性癌患者或III/IV期疾病患者中更为常见,因此研究者仅对III/IV期疾病患者进行了生存分析。如图2B、C所示,携带HRR相关PVs的患者的OS比未携带的患者更长(P = 0.04)。Pennington等人报告称,在367名患者中,与无HRR PVs的患者相比,携带胚系BRCA1/2和HRR PVs的患者OS更好(中位生存期分别为70个月vs. 41个月,P = 0.001,HR为0.5,95%CI为0.4-0.8;以及59个月vs. .41个月,P = 0.05,HR为0.7,95%CI为0.5-1.0)。本研究的数据与上述研究结果一致。在各项研究中,携带HRR相关PVs的患者和未携带患者的PFS相似。这可能表明,携带HRR相关PVs的患者在首次疾病进展后的预后更好。这些患者可能对多种化疗方案反应良好。在本研究中,研究者比较了BRCA1、BRCA2、非BRCA HRR相关和非HRR相关PVs患者与无PVs患者的OS和PFS。所有组别的OS均呈现出更好的趋势,但在统计学上无显著差异。由于每组患者数量较少,这些研究结果尚无定论,因此,分析更大队列的数据以制定针对这些患者群体的治疗策略非常重要。
本研究存在以下局限性。首先,在本研究队列中,无法区分浆液性癌的分级(高级别或低级别)。由于低级别浆液性癌曾被诊断为浆液性交界性肿瘤的一部分,研究者认为本队列中的大多数浆液性癌为高级别。然而,本研究中的浆液性癌可能包含一些低级别浆液性癌。Allison等人报告了晚期浆液性癌的预后情况,其中低级别浆液性癌的发生率为4.3% 。因此,低级别浆液性癌对预后的潜在影响可能较小。其次,贝伐珠单抗和奥拉帕利分别于2013年和2019年在日本被批准用于一线治疗。本研究中的患者几乎没有人将PARPi或贝伐珠单抗作为一线治疗药物,因此本研究的PFS数据可能无法反映当前的临床实践情况。最后,由于本研究的范围限制,研究者没有排除HRR相关基因存在体细胞致病性变异的患者,因为纳入这些患者可能会对分析结果产生潜在的干扰。
12.8%的上皮性卵巢癌患者和18.5%的III/IV期上皮性卵巢癌患者被检测出HRR相关PVs。胚系HRR PVs状态会影响上皮性卵巢癌的预后,被认为是选择治疗方案的重要指标。
参考文献:
Miwa M, Kitagawa M, Asami Y, et al. Prevalence and outcomes of germline pathogenic variants of homologous recombination repair genes in ovarian cancer. Cancer Sci. 2024;115(12):3952-3962. doi:10.1111/cas.16367

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















感谢您的分享
2
EOC是全球女性中与癌症相关的死亡率第八高的病因
3
卵巢癌治疗
4
#卵巢癌# #HRR#
10