Eur J Pharm Sci:小儿急性淋巴细胞白血病维持期地塞米松治疗的优化——地塞米松和代谢物的群体药代动力学和药效学研究
2024-11-26 将军的九分裤 MedSci原创 发表于上海
这些结果支持对地塞米松如何个体化给药进行更多的研究并调整剂量以限制副作用

急性淋巴细胞白血病(ALL)是最常见的儿童恶性肿瘤,地塞米松在小儿急性淋巴细胞白血病(ALL)的治疗中起着至关重要的作用,但地塞米松及其代谢物的药代动力学研究较少。这项研究进行了全面的地塞米松和代谢物的药代动力学-药效学分析,探讨其相关性地塞米松致毒性,对推进个体化精确给药具有重要意义。
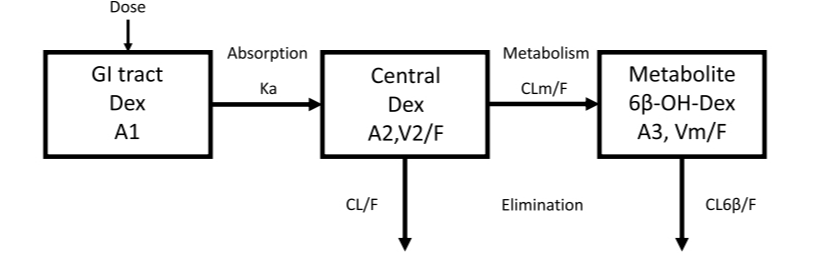
图1:地塞米松代谢物模型的示意图
研究人员在维持阶段采集峰谷浓度来自接受口服地塞米松(6mg/m2/天)的ALL患儿。采用NONMEM方法研究人群药代动力学包括协变量。药代动力学(PK)和药效学(PD)的相关性药物及其活性代谢物暴露和不良反应之间的关系被检查。382个样品(dexa-美松:n=191;6β-羟地塞米松:191例)来自104名儿童(年龄3.0-18.8岁)收集的单室模型最好地描述了数据。

图2:基础模型和最终模型的PK参数

图3:地塞米松的视觉预测检查(VPC)结果。
估计的地塞米松表观总量清除率为26L/h/70kg,个体间变异率为18%,表观分布体积为123L/70kg,产生的半衰期为3.3h给药后,地塞米松的清除率和程度都降低了50%地塞米松代谢为6β-羟地塞米松。统计上显著但微弱的阳性观察地塞米松药物暴露与空腹饥饿评分之间的相关性。地塞米松通过抑制CYP3A4通路,天冬酰胺酶共给药显著增加暴露。

图4:两种标准儿科ALL患者在第5天至第7天,不同协变量组合对地塞米松 (a,b) 及其活性代谢物6β-羟基地塞米松 (c,d) 浓度的模拟结果。
总的来说,研究证实了地塞米松及其代谢产物6β-羟基地塞米松的药代动力学。联合用药,特别是与门冬酰胺酶联合用药,可通过抑制CYP3A通路对地塞米松的清除产生显着影响。此外,地塞米松曲线下面积(AUC)和空腹饥饿得分之间存在微弱但具有统计学意义的正相关性,这对未来在更大患者群体和丰富样本的研究更好地理解地塞米松的药代动力学药效学(PK-PD)作用并确定其最佳浓度目标至关重要。
原始出处:
Li L, van Hulst AM, Verwaaijen EJ, et al. Towards optimization of dexamethasone therapy in the maintenance phase of pediatric acute lymphoblastic leukemia: A population pharmacokinetic and pharmacodynamic study of dexamethasone and metabolite. Eur J Pharm Sci. Published online November 17, 2024. doi:10.1016/j.ejps.2024.106964
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#地塞米松# #药代动力学# #小儿急性淋巴细胞白血病(ALL)#
38