她曾被判无期,如今重获新生:多学科团队如何逆转命运?
2025-03-18 肿瘤医学论坛 肿瘤医学论坛 发表于陕西省
本文介绍了一名 54 岁乙状结肠腺癌肝转移女性患者的治疗过程。患者初诊后经转化治疗、手术及多种化疗和靶向治疗,期间病情有反复,基因检测结果也发生变化。
一、病例介绍
患者基本情况
患者: 王某,女,54岁,160cm,59kg, BMI 23.0, ECOG 0分, NRS2002: 0分
主诉:大便带血2周
既往史:2018年6月行胃镜下息肉切除术
家族史,个人史:无特殊
治疗经过
初步检查
2019年10月15开始无明显诱因出现间断大便带鲜血,每日大便3-4次, 稍感腹痛,无腹胀,便后缓解,无恶心呕吐,无发热,无胸闷心慌等不适。
2019-10-30武汉大学中南医院门诊肠镜:乙状结肠距肛门17-20cm可见一菜花状新生物,质硬脆,中央溃烂。其余部分未见明显异常
肠镜活检病理报告:(乙状结肠)腺癌。
2019-11-5就诊于武汉大学中南医院, CEA:14.7ng/mL↑。
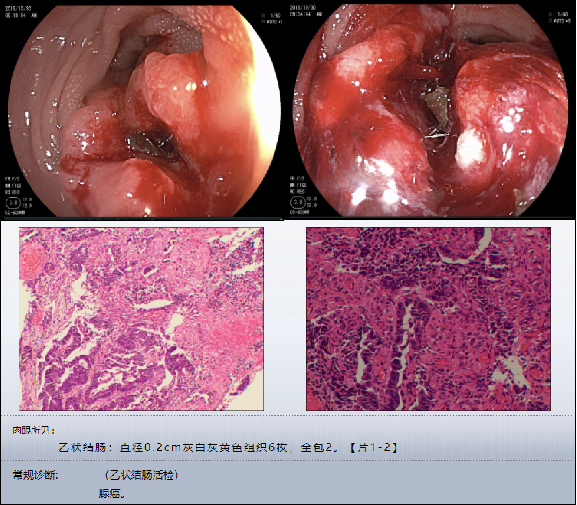
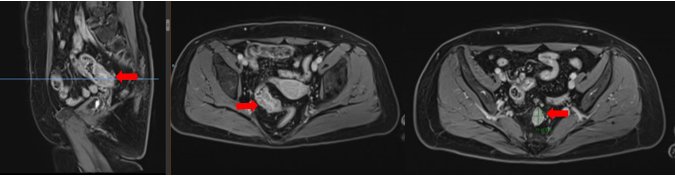
进一步完善影像检测可见:乙状结肠-直肠交界处管壁不均匀增厚伴周围淋巴结肿大。
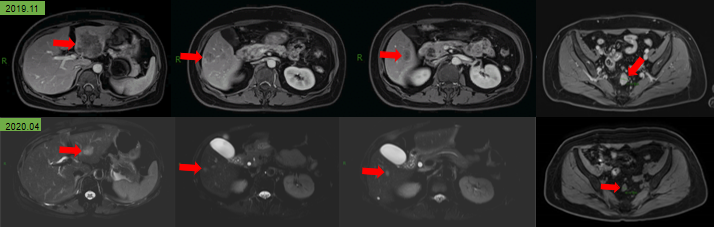
增强CT检查发现:肝脏多发转移瘤,进一步行肝脏MRI检查确认。
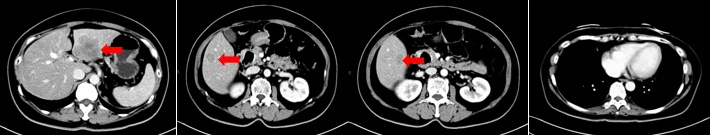
MRI报告:肝脏多发转移瘤,最大转移瘤直径超过5cm。
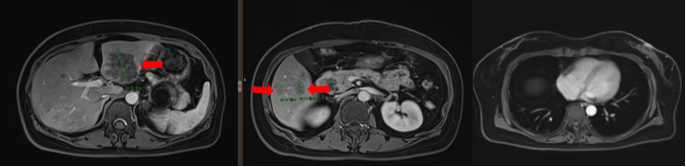
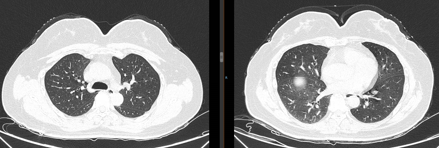
肺部CT未见转移。
基因检测结果:未检测到KRAS、NRAS、BRAF、PIK3CA突变,PD-L1阳性,MSS。
第一次MDT讨论
患者的诊断,分期:乙状结肠腺癌肝转移 cT3N1M1a,CRS评分:4分,KRAS、NRAS、BRAF、PIK3CA基因均为野生型,MSS。
治疗目的:NED
治疗策略及方案:转化治疗后行手术切除。
一线治疗
2019.11.11至2020.1.20行6个周期mFOLFOX6联合西妥昔单抗治疗,因新冠肺炎疫情中断近3月。
6个周期治疗后,疗效PR,CEA:14.7ng/mL→3.3ng/mL。
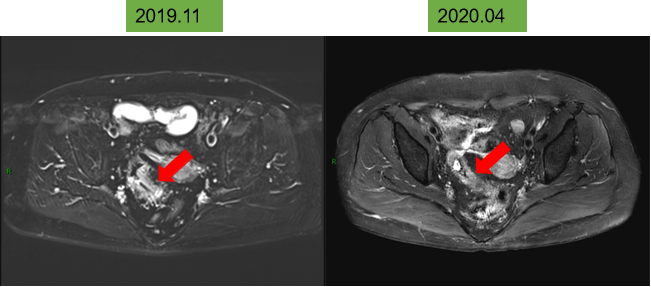
进一步完善肠镜复查可见:治疗后距离肛门17cm可见深基溃疡,占据肠管2/5,质脆,接触出血,周边粘膜肿胀,内镜通过顺畅。

第二次MDT讨论
经MDT讨论后,于2020-4-14 腹腔镜乙状结肠切除术+根治性淋巴结清扫术+肝左外叶切除术+肝右叶肿瘤射频消融术,病理提示:中分化腺癌,ypT3N2M1,TRG2,脉管浸润。
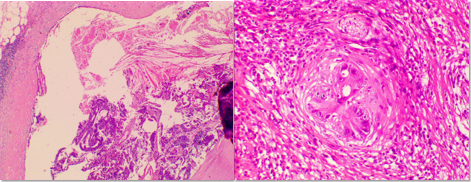
乙状结肠癌肝转移转化治疗后术后(ypT3N2M1a)。
预后不良因素:初始CRS评分4分,术后TRG2,神经侵犯,Ki67:60%。
2020-5-14术后一个月复查未见肿瘤复发转移,CEA:3.33ng/mL。
2020-5-21至2020-6-19行第7-9周期mFOLFOX6方案化疗联合西妥昔单抗靶向治疗。
2020-07-08至2021-6-16行西妥昔单抗(500mg/m2 ,每两周)靶向治疗+口服卡培他滨化疗。
2021-6-29常规复查发现:右侧腹壁瘢痕处见直径6mm的增强结节。
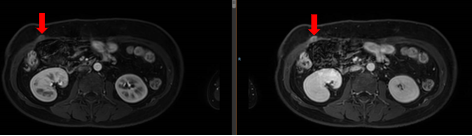
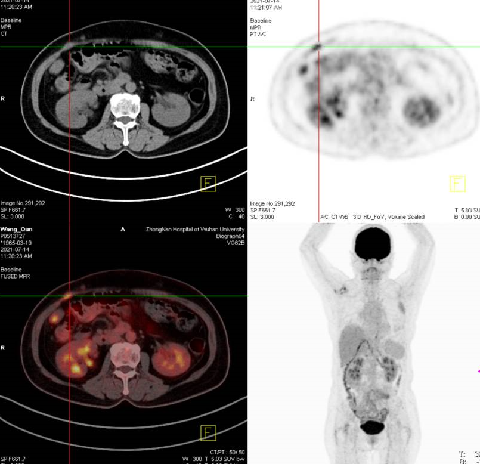
为明确结节性质,于2021-7-14做了PET-CT检查。诊断意见为:乙状结肠腺Ca肝转移综合治疗后:1.右上腹壁术区周圈皮下软组织结节,代谢异常增高,考虑多为转移性病变。2.乙状结肠、腹壁、肝脏及胆囊术后改变。3.余探测部位未见明显恶性肿瘤病变及转移征象。
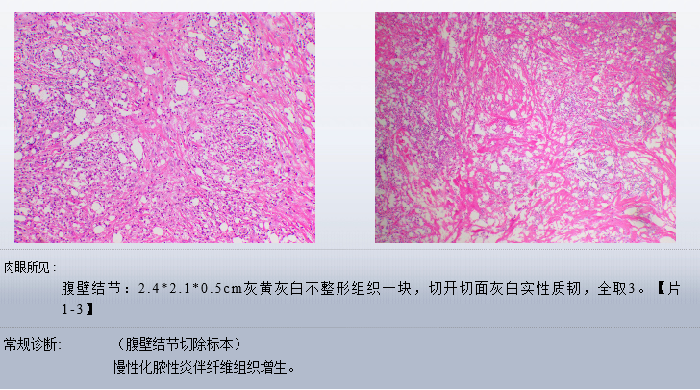
2021-7-21经皮腹腔肿物活组织检查+腹壁切开术+腹腔探查术。手术记录:根据CT引导及触诊腹壁肿物位置,取原肋缘下切口约8cm进腹,仔细分离粘连后探查腹腔,未见未触及明显结节,未见肿瘤复发迹象,遂将腹壁肿物及周围包裹组织切除,后逐层关腹。
2021-8-20至2021-11-10行西妥昔单抗(800mg)靶向治疗+卡培他滨维持化疗后自行停药,共维持治疗16m。
2022-4-13常规复查发现:肝右叶下段新发结节,其余脏器组织未见转移。肝右下叶前段可见小结节样稍长T2信号灶(增强可见环形强化),CEA:2.88ng/mL。
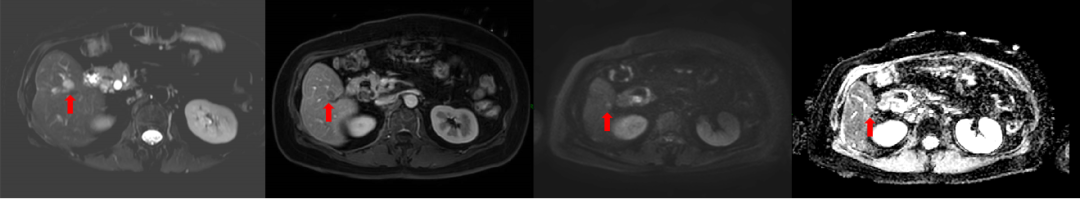
2022-6-1行肝右叶结节穿刺活检术,病理提示为:符合转移性结肠腺癌。
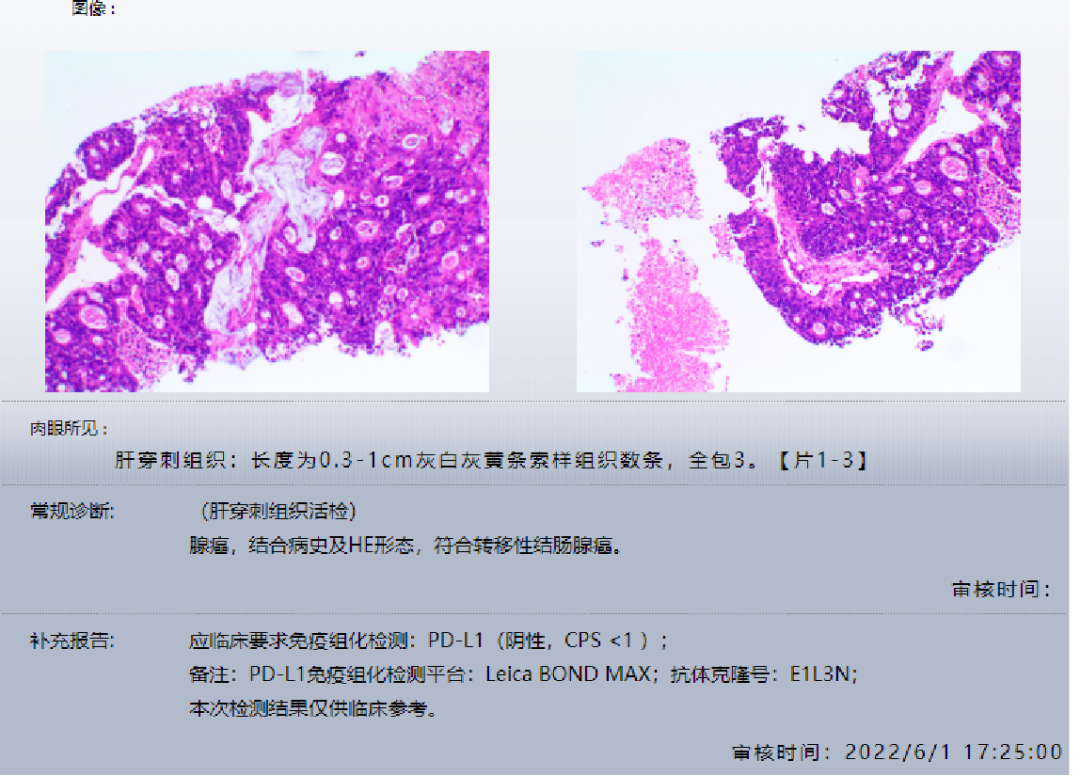
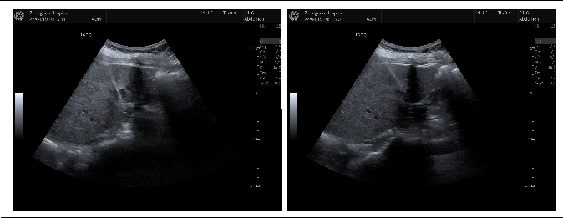
随后进行了肝右叶转移灶射频消融术:术中超声检查:右肝内可见一个大小为1.3x1.1cm的低回声光团,周边轮欠清晰,内部回声不均,CDFI;上述低回声光团内未见明显彩色血流信号显示。
术中超声引导下肝w射频治疗:患者半左侧卧位,全麻后常规消毒铺巾,在超声引导下进单极射频针入上述低回声光团射频治疗,治疗时间共的为12分钟;上述低回声光团回声增强。惠者生命体征平稳。
2022-4-13 肝右叶新发转移灶基因检测:KRAS Q61H突变。
二线治疗
于2022-5-31至2022-9-31行6个周期XELOX化疗,口服卡培他滨至2023-5。
2023-6-6常规复查发现:肝脏病灶灭活,余未见复发转移灶。
诊断意见:乙状结肠恶性肿瘤及肝继发肿瘤治疗后;肝左叶切除术后;肝右前叶下段转移射频治疗后,未见明显强化及弥散受限;肝切缘异常灌注并囊性灶,右叶肝内胆管稍扩张,较前变化不大;十二指肠降部憩室;双肾多发囊肿;宫颈小囊肿。右肺下叶磨玻璃小结节,建议年度复查;右肺少许纤维灶。
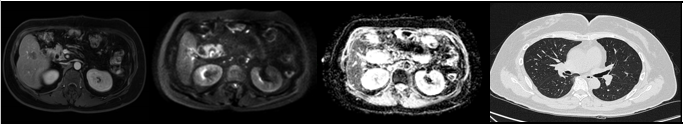
2023-10-16 复查:CA199为523 U/mL↑,肺新发转移,余未见异常。
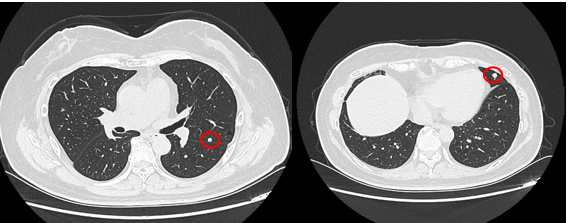
2023-10-18行肺转移灶放疗,PTV-GTV=65Gy/50Gy/10F。
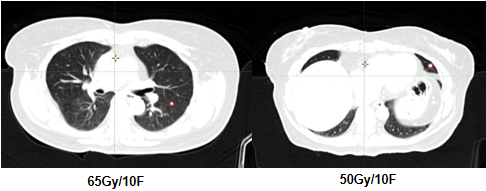
三线治疗
放疗结束后,于2023-11-1开始行TAS-102治疗1年,目前状态:NED。
治疗小结
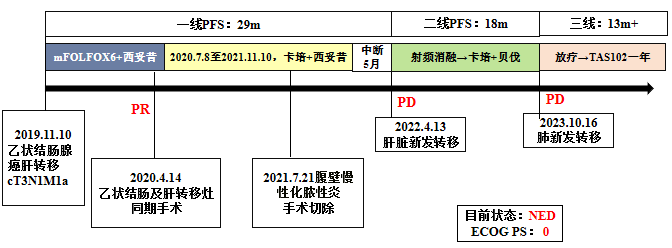
二、病例讨论
问题 1:请谈谈对这个患者治疗过程的体会及后续治疗的建议。
华中科技大学同济医学院附属协和医院-肿瘤科-李品东:
徐教授团队带来了一个非常精彩且成功的病例。徐会教授的团队为这位患者制定了有效的治疗方案,患者的毒副反应轻微,结合其具体病情,在结肠癌肝转移后已经生存超过50个月,并且仍在继续生存,这无疑是一个非常成功的病例。
患者在初诊时即存在肝转移,是一个非常经典的病例,54岁,KRAS、NRAS、BRAF野生型。在治疗过程中,该患者接受了成功的同期切除手术加上术后治疗,总体治疗效果显著,无进展生存期(PFS)达到29个月。在后续的复发过程中,患者再次出现转移,团队在这种情况下选择了合适的药物治疗,包括贝伐珠单抗联合卡培他滨的维持治疗。这种治疗策略与2024年的新进展非常契合,将局部治疗与药物治疗有机结合,使患者接近五年的生存期。
患者初始治疗到3个月后进展时,使用了TAS-102方案,效果显著,没有过度使用药物。TAS-102维持了一年的时间,较平均6.8个月的PFS表现更佳。这与徐会教授团队在肺转移时给予肺部病灶高剂量立体定向放疗或消融治疗息息相关。在积极的局部治疗基础上,采用适当的药物治疗,使全身影响较小,复发性较轻。
我个人非常认可这种方法,因为我们需要充分结合不同治疗手段的长处和优点,避免过多使用药物联合治疗,可能会增加患者的肝肾负担,影响患者耐受性。通过局部治疗和放疗的结合,可以避免强烈的后线药物治疗,因为在后续的治疗中,可能会面临药物可用但身体无法耐受的情况。
结合最新的进展,TAS-102方案的应用,无论是联合贝伐珠单抗还是单独使用,都能更好地适应不同的临床场景。如果患者再次出现蛋白尿或肝功能损害,未来还有更多的选择可以使用。这种治疗策略不仅提高了患者的生存期,也为临床实践提供了有益的经验。
华中科技大学同济医学院附属协和医院-肿瘤中心腹部肿瘤科-于丹丹:
徐教授介绍的这个肠癌病例的情况其实在我们的日常工作中是经常会遇到的。她在初诊时被确诊为乙状结肠癌并伴有肝转移。幸运的是,患者是全野生型,这从她的病史中可以看出,符合全野生型癌症的特征。
首先,从整个病史来看,这个病例充分体现了多学科治疗的重要性。每当患者在治疗过程中遇到问题,我们都能及时进行处理,使患者能够达到NED或接近NED的状态。其次,这个病例还展示了肠癌晚期基因型可能发生变化的情况。在经过治疗后,患者的部分转移病灶出现了基因型的改变,我们根据这些变化,采用了不同的靶向联合治疗策略。
再者,患者每次病灶的发现都非常及时,这得益于患者与医生之间的充分配合和交流。每当出现苗头时,我们都能及时控制住病情,这也体现了在肿瘤负荷较小时,争取为患者达到NED状态的重要性。这样,患者的PFS和OS才能得到更长时间的延长。
最后一点是关于TAS-102的应用。TAS-102在该患者身上无疑是一个优势选择。临床研究显示,PFS一般为半年多,而这位患者接近一年的PFS,充分得益于以往接受的强有力的局部治疗。再次进展时,患者非常幸运地出现了肺部进展,这种情况相对缓慢,药物治疗也能更持久地控制病情。
从各个方面来看,这位患者的治疗非常成功。在临床应用中,我们并没有严格按照指南进行标准化治疗,而是根据患者的具体情况,避免使用高剂量或难以耐受的高强度化疗。目前,这位患者在TAS-102治疗过程中已经维持了很长时间的PFS,我相信他仍有很长的PFS。希望在今后的MDT分享过程中,徐教授能继续为我们分享这个患者的病例。
孝感市中心医院-肿瘤科-庞振国:
徐教授分享的这个病例是一个非常成功的案例,也是我们临床工作中常见的肠癌经典病例。目前,肠癌和其他肿瘤已经进入了慢病管理时代,患者的生存期明显延长,这就要求我们在治疗中需要全面统筹考虑。
在长期治疗过程中,首要考虑的是患者能够持续接受治疗,既要保证疗效,又要关注患者的身体耐受性。因为有些患者在后期虽然还有治疗方案可选,但由于前期治疗导致身体状况和耐受性下降,无法继续接受治疗,这会影响总生存期。因此,在选择治疗方案时需要考虑多个因素,既要关注疗效,也要权衡身体耐受性。
徐教授使用的方案很好地结合了局部治疗和全身治疗。因为这是一位Ⅳ期患者,同时存在局部和全身病灶,治疗中需要同时考虑这两个方面。通过合理的治疗排序,达到了较好的总体控制效果。
在维持治疗方面,需要考虑在适当时机调整方案,将治疗强度降到合适程度,在控制病情的同时确保患者在耐受性和不良反应方面能够继续维持治疗。这位患者从2020年至今已经存活近四年,虽然使用了一些治疗方案,但后期还有很多方案未使用。从整体来看,如果后续使用这些方案,预期效果应该还是比较理想的。
三、MDT小结
华中科技大学同济医学院附属协和医院-肿瘤中心-杨盛力:
徐会老师分享的这个病例确实非常精彩,尤其是患者的生存时间已经超过了五年,这在晚期肠癌病例中是一个非常令人鼓舞的结果。患者能够取得如此好的预后,主要得益于中南医院的多学科诊疗(MDT)团队的规范化管理和多次深入的讨论。每一次的MDT讨论都为患者制定了精准的治疗策略,而患者也严格遵循了这些专业意见,这无疑是成功的关键。
多学科诊疗模式在现代肿瘤治疗中扮演着至关重要的角色。通过MDT讨论,来自不同专业领域的专家能够集思广益,为患者制定出个性化的治疗方案。这种协作不仅提高了治疗的精准性,还能更好地管理患者的综合健康状况,减少并发症的发生。特别是在复杂的晚期肠癌治疗中,MDT的优势更加明显,它可以帮助医务人员在面对多种治疗选择时,做出最优决策。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#肝转移# #乙状结肠腺癌#
4