转移性结直肠癌肝切除前后血液检测7基因,仅术后ctDNA持续阳性与复发紧密相关
2025-03-22 苏州绘真医学 苏州绘真医学 发表于陕西省
研究探索 ctDNA 分子特征持续存在对 CRLM 肝切除术后复发的预后价值,发现 51 例患者中术后 ctDNA 分子特征持续存在与复发相关,可预测 DFS,或助选术后策略,样本量小存局限。
肝切除术是结直肠癌肝转移(CRLM)的主要治疗方法,但术后复发率仍然较高。确定有效且可重复的复发预测指标,对于疾病的正确及时管理至关重要。在这种情况下,液体活检可能是一种用于对CRC患者进行临床分层的辅助手段,它具有侵入性较小、易于操作的特点。本研究旨在探索循环肿瘤DNA(ctDNA)分子特征持续存在对CRLM肝切除术后复发的预后价值。2020年1月至2023年3月期间,前瞻性纳入连续51例因CRLM接受肝切除术的患者。对患者手术前后外周血样本进行液体活检。还评估了其他疾病复发风险因素。术前(T0)ctDNA分析显示,29例患者NGS检出一种临床相关分子改变。单因素分析显示,总肿瘤大小大于60mm(p=0.046,HR 2.486)和术后ctDNA分子特征持续存在(p=0.024,HR 2.831)与复发显著相关。多因素Cox回归分析表明,只有术后ctDNA分子特征持续存在与复发相关(p=0.027,HR 2.766)。类似地,液体活检显示分子特征持续存在的患者,1-3年无病生存率(DFS)显著更低(100-49.5% vs 57.1-21.4%,p=0.018)。本研究表明,术后ctDNA分子特征持续存在,可能是预测CRLM患者肝切除术后复发的有效指标。
研究背景
转移性结直肠癌(CRC)是全球癌症死亡的主要原因之一,每年导致近100万人死亡。肝切除术是治疗CRC肝转移(CRLM)的基石,带来良好的长期临床结局,致病率和死亡率较低。然而,复发仍然是一个主要问题,高达75%的患者在手术治疗后会出现复发。人们普遍认为,高复发率受到起源于原发性CRC病灶的隐匿性全身疾病的影响。确定一个有效且可重复的复发预测指标,对疾病的早期识别和及时管理起着关键作用。遗憾的是,目前仍未找到这种理想的标志物。癌胚抗原(CEA)在多种癌症患者中经常升高。CEA检测广泛应用于CRC患者的管理,尤其是作为原发性I-III期CRC肿瘤切除后的早期监测工具。此外,先前的研究表明,围手术期CEA是CRLM患者切缘阴性手术(R0)后复发的预测指标。然而,围手术期CEA在CRLM患者管理中的应用尚不明确,因为其在CRLM患者术后监测中的有效性尚未得到充分研究。
Fong及其同事开发的一种临床评分系统,被证明能够预测长期结局。具体而言,与满足3 - 5项标准的患者相比,符合至多两项标准的患者可能有更好的结局。然而,Fong评分的作用可能与近期的临床进展不一致,比如分子靶向治疗和生物治疗,因为它的概念和验证可追溯到15年前。
液体活检获得的循环肿瘤DNA(ctDNA)是循环游离DNA(cfDNA)的一小部分,已被证实是一种动态、非侵入性、癌症特异性的生物标志物,具有重要的诊断和预后意义,在预测化疗反应和监测治疗疗效方面也有潜在应用。有趣的是,血液ctDNA检测比影像学和临床指标更早发现肿瘤反应或复发。此前两项针对转移性CRC患者的研究表明,术后可ctDNA阳性与复发率相关。此外,ctDNA作为一种有前景的工具,可基于化疗诱导动态评估肿瘤基因组特征。实际上,在CRLM患者中,ctDNA分析已被用于多种目的,包括其水平与生存率的相关性、治疗反应的监测,以及在不同时间点检测RAS/BRAF/PIK3CA等具有临床意义的突变。液体活检能够克服组织样本在监测转移性肿瘤患者肿瘤复发方面的技术和生物学局限性(如空间异质性),有助于对肿瘤患者的分子图谱进行全面的动态分析。
本研究在前瞻性连续CRLM患者群体中,比较了ctDNA与常规标准化预后标志物的预后预测能力,探索了肝切除术后ctDNA分子特征持续存在对CRLM复发的预测作用。
研究方法
本研究的主要目的是评估CRLM肝切除术后血液ctDNA持续存在是否为肿瘤复发的预测指标。2020年1月至2023年3月期间前瞻性纳入因CRLM接受肝切除术的连续患者。对于51例CRLM患者,在不同时间点前瞻性收集纵向液体活检样本:术前24小时(T0)、术后48小时(T1)、术后30天(T2)。每个时间点采集10mL外周血。使用定制的NGS panel进行分子检测,该panel能够检测7个癌症相关基因(EGFR、BRAF、KRAS、NRAS、PI3KCA、c-KIT、PDGFRA)的568种可操作改变。还使用NGS对匹配的组织样本进行检测。“分子特征”的存在定义为在与CRC发生相关的关键基因中,存在至少一种上述热点突变。术后ctDNA分子特征持续存在定义为在T0分析中已显示分子特征的患者群体中,T1和T2分析均检测到分子特征。
研究结果
患者和肿瘤特征
研究期间共纳入51例患者。患者的平均年龄为62.4±11岁,60.8%为男性。所有纳入患者均接受了肝切除术,其中47.1%的患者接受了非解剖性肝切除术,29.4%的患者接受了肝段切除术,15.7%的患者接受了肝双段切除术,其余7.8%的患者接受了半肝切除术。
总体而言,在51例患者中,29例(56.8%)的T0液体活检样本存在某个与转移性CRC发生相关的关键基因改变。T0时分子特征阳性和阴性的患者组之间未发现差异。患者和肿瘤特征的所有数据见表1。同样,T0时分子特征阴性和阳性的患者在1 - 3年DFS(分别为43.6 - 19.4%和79.3 - 35.8%;p = 0.096)和1 - 3年OS(分别为72.7 - 54.5%和100 - 75.5%;p = 0.066,图1)方面没有差异。
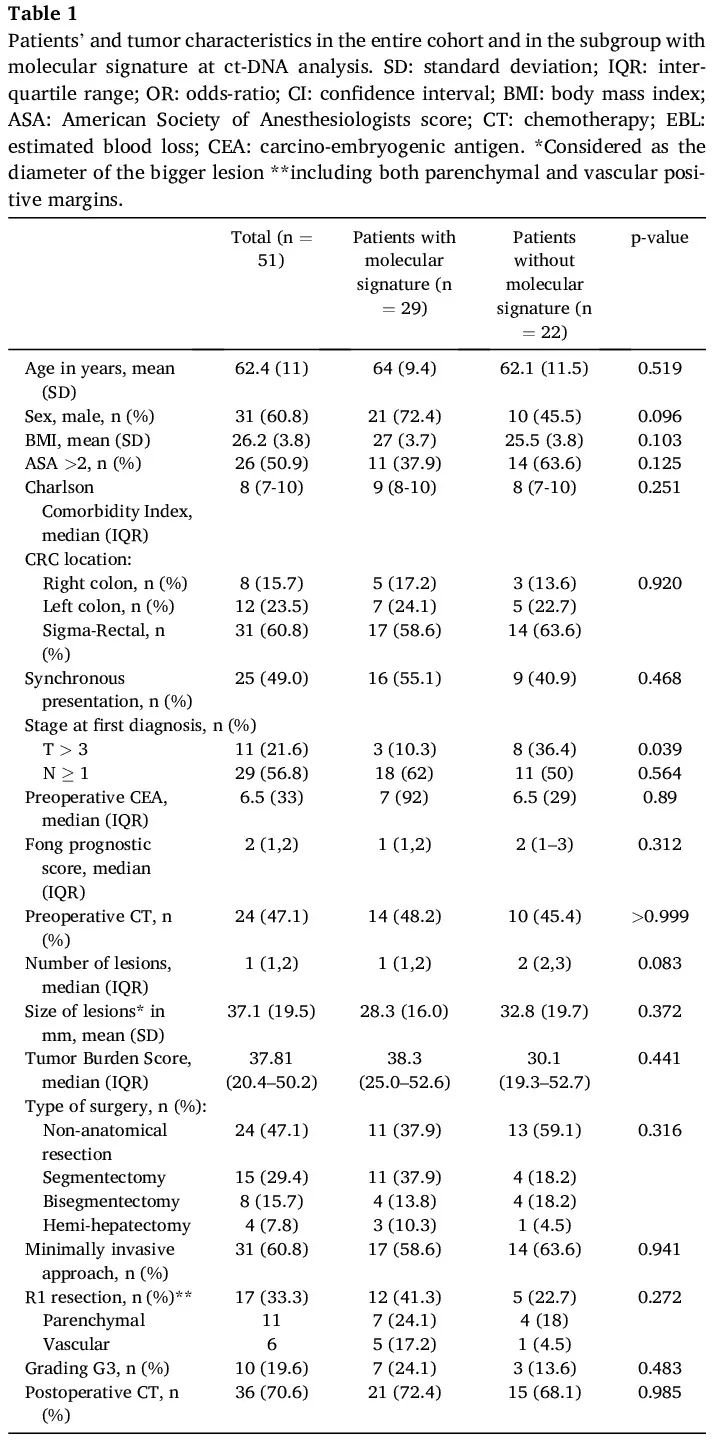
表1
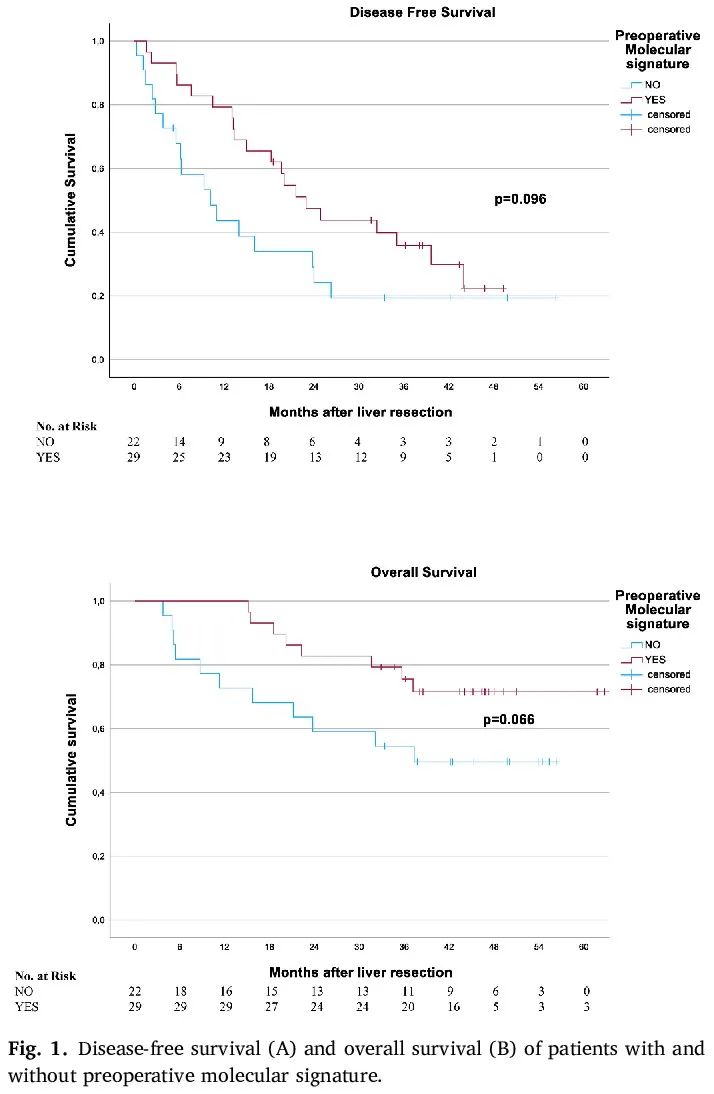
图1
基因突变和ctDNA分析
在29例具有术前ctDNA分子特征的患者中,最常见的点突变发生在KRAS基因的2 - 3 - 4外显子,共15例[15例CRC患者中,12例(80.0%)携带KRAS基因2号外显子点突变,3例(20.0%)携带3号外显子点突变]。4例患者检测到BRAF基因11 - 15外显子点突变[其中3例检测到BRAF基因15号外显子热点突变,1例检测到BRAF基因11号外显子单核苷酸改变]。在3例CRC患者中观察到NRAS基因3 - 4外显子热点改变[其中2例(66.7%)携带NRAS基因3号外显子改变,1例检测到NRAS基因4号外显子热点突变]。此外,9例CRC患者携带PIK3CA热点突变,分布在9号外显子(6例,66.6%)和20号外显子(3例,33.3%)。有趣的是,2例患者存在上述基因共突变(1例同时存在PIK3CA + KRAS临床相关突变,1例存在PIK3CA + BRAF分子改变)。术前和术后检测到的突变情况见图2。
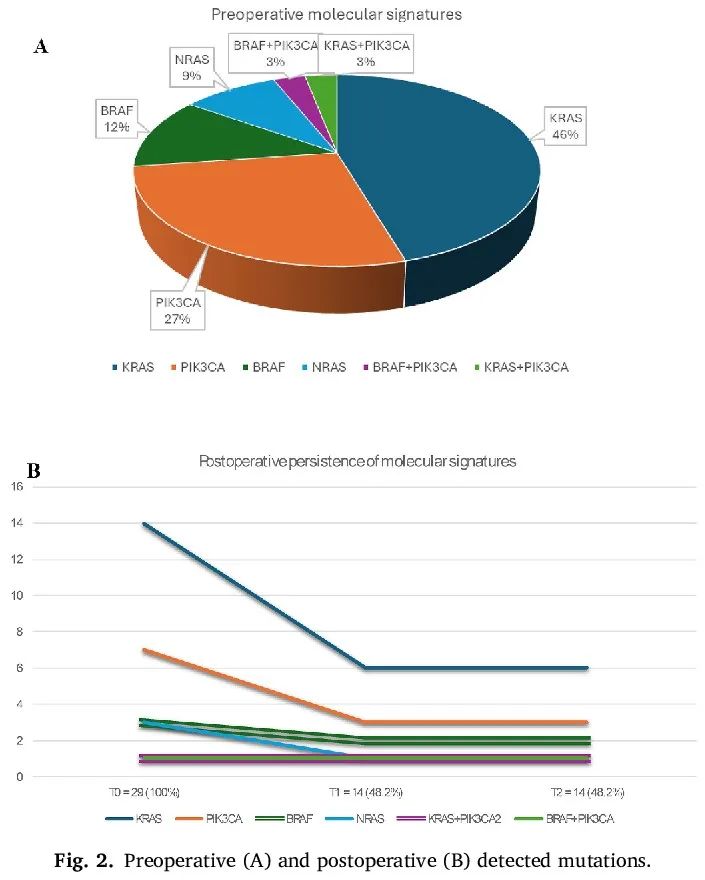
图2
在13例患者中检测到多态性变异[13例中有2例(15.4%)携带cKIT p.M541变异,8例(61.5%)携带PDGFRa p.V824V变异,3例(23.1%)同时携带这两种突变]。
在T0液体活检样本呈阳性的29例患者中,14例在术后(T1 - T2液体活检样本)检测到具有临床意义的KRAS、NRAS、BRAF、PIK3CA分子改变持续存在。此外,在术后T1液体活检样本中还发现了2种在T0液体活检样本中未观察到的分子改变[p.G13D KRAS(0.2%)和p.E545G PIK3CA(0.2%)热点突变]。
术前或术后ctDNA和匹配组织中的突变
在可及的组织样本(14/51,27.4%)中,分子分析显示,14例中有6例(42.8%)存在CRC临床相关分子改变,4例患者检测到多态性改变。在14例病例中,9例(64.3%)组织和T0液体活检的分子分析结果完全匹配,其中2例为突变型,7例为野生型。
复发预测因素分析
在具有术前ctDNA相关分子特征的患者中,单因素分析显示,病理标本中总肿瘤大小大于60mm(p = 0.046,HR 2.486 [95% CI 1.015 - 6.089])和术后ctDNA相关分子特征持续存在(p = 0.024,HR 2.831 [95% CI 1.148 - 6.980])与肿瘤复发相关(表2)。多因素分析表明,只有术后ctDNA分子特征持续存在与复发相关(p = 0.027,HR 2.766 [95% CI 1.119 - 6.832])。
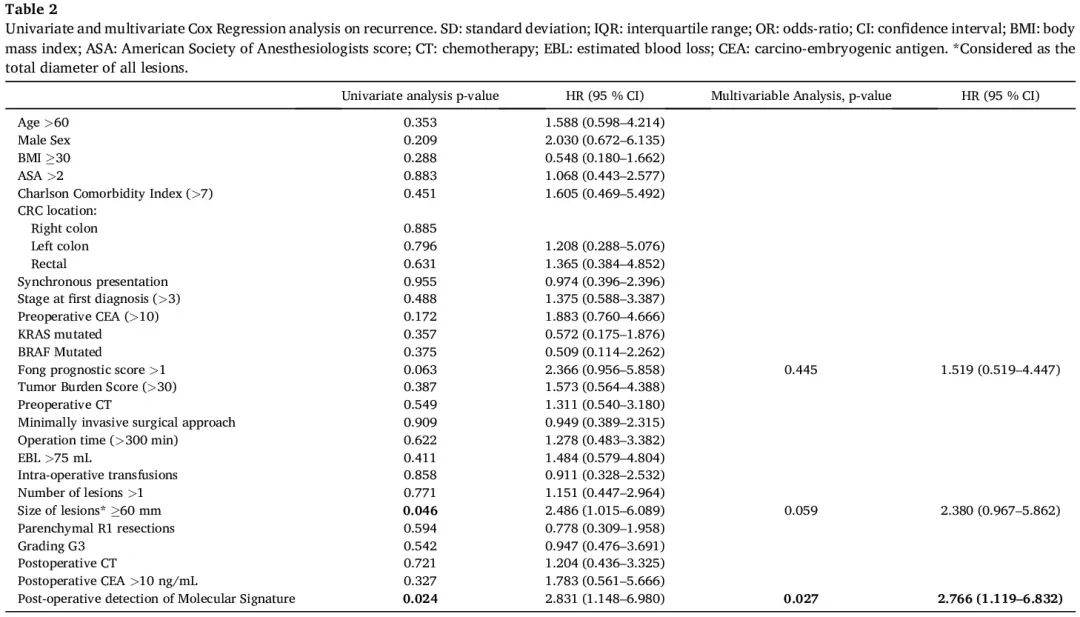
表2
生存结局
术后分子特征持续存在和不持续存在的患者的生存结局见图3。中位随访46.7个月后,术后液体活检显示分子特征持续存在的患者,1 - 3年DFS显著更低(100 - 49.5% vs 57.1 - 21.4%,p = 0.018)。
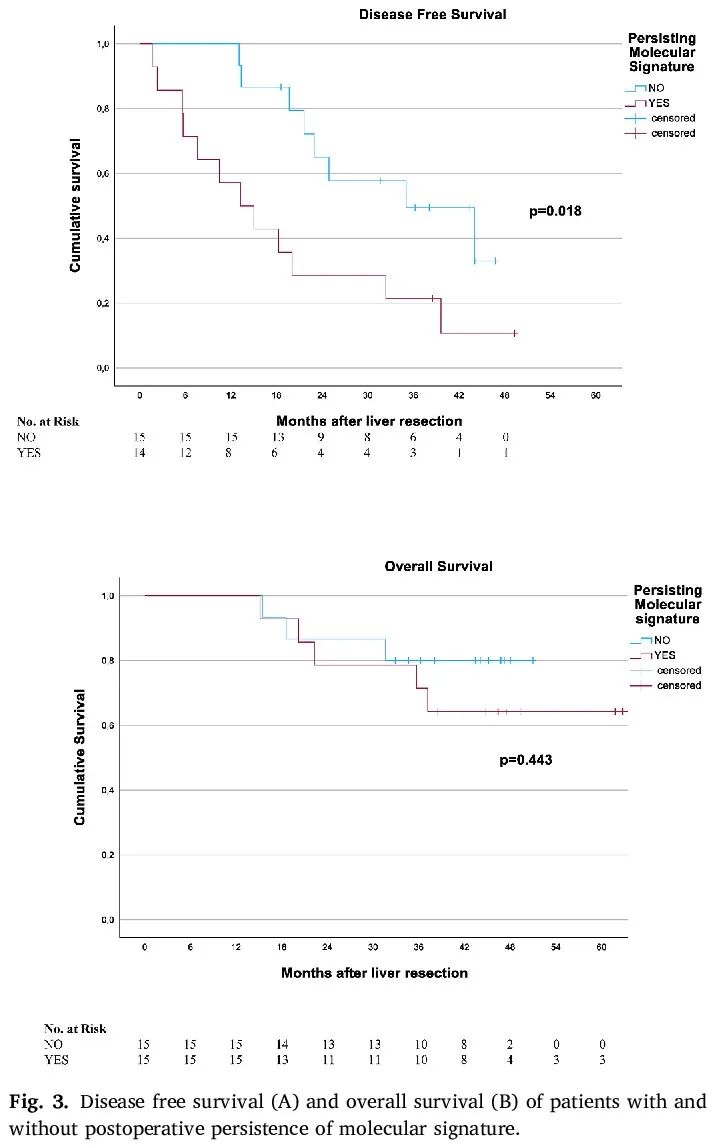
图3
相反,分子特征不持续存在和持续存在的患者之间,1 - 3年OS相似(100 - 80% vs 100 - 71.4%,p = 0.443)。
讨 论
这是首个专门探索在接受肝切除术的CRLM患者中,术后ctDNA分子特征持续存在的预后作用的研究。
近年来,ctDNA已显示出对包括CRLM患者在内的多种实体瘤临床管理的巨大潜在影响。事实上,生物体液是一种微创、动态且分子层面可靠的诊断工具,基于临床试验中快速涌现的诊断、预后和预测数据,它能够识别分子标志,对肿瘤进行分层。
在这项初步研究中,我们探究了选定接受手术的CRLM患者中ctDNA分子特征持续存在的情况。
接受手术的CRLM患者进行ctDNA液体活检的价值,通过ctDNA来源的分子改变与匹配组织样本的分子特征之间的相关性得到了证实。在9/14例(64.3%)病例中,术前液体活检样本证实了基于组织的分子评估结果,支持液体活检在纵向血浆样本中监测MAF变化的技术可行性。以组织作为金标准样本,在术前液体活检样本中未观察到假阳性结果,这与文献数据一致。考虑到这些信息,能够动态评估分子分析的技术方法在CRLM患者的临床管理中起着关键作用。
已有多项临床因素被报道与复发相关,如肿瘤大小、肿瘤数量、肿瘤分级、分期、Fong评分、术前和术后血清CEA水平、ctDNA分子特征以及肿瘤突变谱。单因素分析显示,复发与肿瘤大小和术后ctDNA分子特征持续存在显著相关。肿瘤大小是CRLM患者的已知预后因素。然而,在我们的研究中,多变量分析表明,与肿瘤复发相关的唯一因素是术后ctDNA相关分子特征持续存在。
针对CRLM患者,已经开发了多种预后系统,包括肝转移灶数量、原发性肿瘤分期、肿瘤大小、术前CEA水平、组织病理学特征和Fong预后评分。Fong预后评分涵盖了其中许多因素,被认为具有较高的预测价值。这些因素可用于CRLM患者的预后分析,但仍无法指导个体化患者管理。在常规患者的临床管理中,应确定一种能够准确评估CRLM患者复发风险的特异性预后生物标志物。特别是,一种可重复、准确且易于检测的预后生物标志物,可能会指导初始围手术期决策,例如术后化疗的选择或最佳监测策略。此外,我们的研究结果可能为新的场景开辟道路,术后ctDNA分子特征持续存在的患者可能会从新型全身治疗策略或更密集的监测中获益。这一假设应在未来的临床试验中进行探索。Tei等人报道了ctDNA动态变化与辅助治疗以及无病生存期和总生存期之间的相关性,表明治疗后ctDNA持续存在是不良预后因素,而ctDNA清除则是辅助治疗有效性的早期指标。我们的多变量分析表明,Fong临床评分和CEA均不能预测疾病复发。这在一定程度上与文献相符,文献并未明确血清CEA作为预测临床复发的可靠标志物的作用。类似地,Fong评分是仅在异时性转移情况下,为预测接受肝切除术的CLRM患者的长期生存和预后而开发和验证的。
值得注意的是,如图2所示,T1和T2时ctDNA分子特征的检出率相同。我们最初认为T1对于检测术后微小残留病可能更有意义。然而,这些患者在T2时仍检测到ctDNA分子特征,且这种ctDNA分子特征持续存在与复发风险密切相关。需要进一步开展大样本研究,聚焦于这些ctDNA检测时间点以证实我们的结果,有可能两次术后检测中的一次就足以预测复发。继续探讨未来的研究方向,ctDNA分子特征持续存在的潜在临床应用可能具有意义,例如根据术后ctDNA分子特征的持续存在情况调整患者管理方案(对于复发风险较高的患者,给予或不给予不同的化疗方案可能有用)。此外,研究基于治疗后ctDNA分子特征的变化对患者预后进行分层的可能性也很有意义:例如,是否像乳腺癌患者那样,新辅助化疗后ctDNA分子特征变为阴性的患者,具有更好的预后?或者,液体活检和组织样本之间的差异可能与新辅助治疗有关。应以这一目标设计进一步的研究,重点关注这一方面。
本研究存在一些局限性。首先,样本量较小,存在II型错误的风险。此外,小样本队列可能导致纳入病例的异质性,例如同时包括了同时性和异时性CRLM患者,尽管其预后相似,但肿瘤生物学特性不同。尽管如此,对比队列在研究变量之间未没有显著差异,纳入连续患者有助于研究真实的患者样本。其次,并非所有研究人群都有组织样本。最后,仅检测了5个与CRC相关的基因:对于定制NGS panel覆盖的预测生物标志物无分子改变的患者(野生型患者),将使用能够检测野生型患者分子特征的全面NGS panel进一步分析。同样,这些进一步的研究还将探究甲基化在CRLM患者中的作用。尽管存在上述局限性,本研究首次揭示了术后ctDNA分子特征持续存在的潜在作用,为进一步的验证研究奠定了基础,并且有可能启动一项随机对照研究,探索特定化疗方案的策略性干预作用。
ctDNA可能是可手术CRLM管理中一种有用且微创的动态肿瘤生物标志物。本研究表明,在接受肝切除术的CRLM患者中,液体活检显示术后ctDNA分子特征持续存在,可预测复发风险。未来,这可能有助于为患者选择术后策略。需要开展更大样本量的研究来证实这些结果。
参考文献:
Montalti R, Pepe F, Cassese G, Russo G, Malapelle U, Carlomagno C, Giglio MC, Falco G, Alagia M, De Simone G, Geboes K, Troncone G, Troisi RI, Rompianesi G. Prognostic role of postoperative persistence of ctDNA molecular signature after liver rep for colorectal liver metastases: Preliminary results from a prospective study. Eur J Surg Oncol. 2025 Feb 15;51(6):109706. doi: 10.1016/j.ejso.2025.109706. Epub ahead of print. PMID: 40009912.


本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#结直肠癌肝转移# #肝切除术#
4