Nature:肝星状细胞:肝脏健康的幕后守护者「eG学术观察」
23小时前 eGastroenterology eGastroenterology 发表于陕西省
多国研究团队发现肝星状细胞(HSCs)通过分泌 RSPO3 调控肝脏分区、再生和代谢。HSCs 从肝纤维化 “元凶” 转变为肝脏健康 “幕后英雄”,这为肝病治疗提供新方向,改写了对肝脏微环境的认知。
导读
肝脏是人体最大的代谢器官,承担着解毒、合成、储存等关键功能。然而,肝脏的健康不仅依赖于肝细胞,更离不开一群“幕后工作者”——肝星状细胞(Hepatic stellate cells,HSCs)。过去,HSCs因驱动肝纤维化而备受关注,然而,来自美国、德国、英国和西班牙等多国的研究团队最新发表于Nature的研究“Hepatic stellate cells control liver zonation, size and functions via R-spondin 3”揭示:HSCs是肝脏健康的“幕后英雄”,它们通过分泌R-spondin 3(RSPO3),像“精密工程师”一样调控肝脏分区、再生和代谢,甚至影响多种肝病的进展,为肝病治疗开辟了新方向。

一、HSCs的“双重身份”:从纤维化“元凶”到代谢“指挥官”
1. 传统认知:HSCs是肝纤维化的“推手”
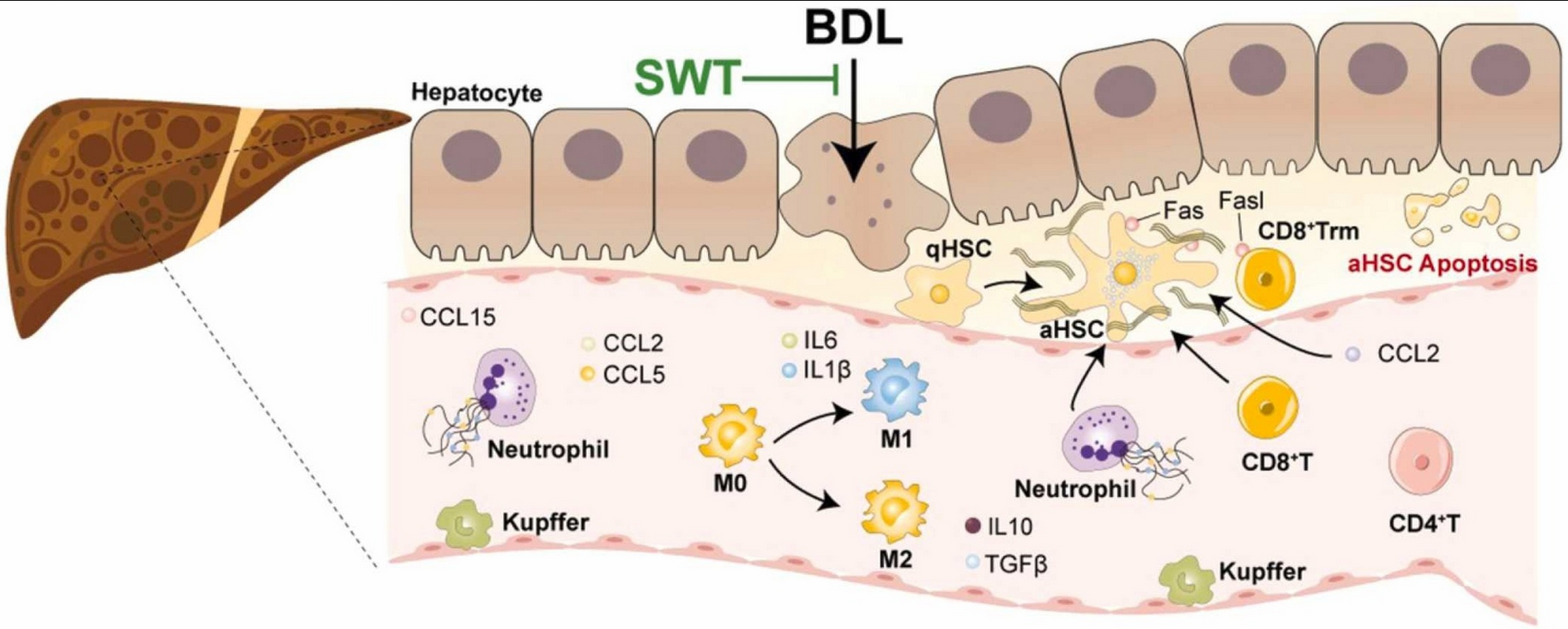
HSCs位于肝窦周围,长期被视为肝脏纤维化的核心驱动者。当肝脏受损时,HSCs被激活为肌成纤维细胞,分泌胶原蛋白,形成瘢痕组织。这一过程虽为修复而生,却可能导致肝硬化,甚至肝癌。
2. 新发现:HSCs的隐藏技能——调控肝脏代谢分区
最新研究通过基因敲除技术发现,HSCs的非纤维化功能才是维持肝脏稳态的关键。当特异性清除小鼠的HSCs后,肝脏出现显著异常:
-代谢分区紊乱:负责解毒的CYP450酶(如CYP2E1、CYP1A2)表达大幅下降,肝脏代谢毒素的能力减弱。
-再生能力受损:部分肝切除后,肝细胞增殖速度降低70%,修复效率骤降。
-损伤反应失衡:对乙酰氨基酚(APAP)等毒素的抵抗能力下降,但特定区域损伤反而加剧。
关键机制:HSCs通过分泌RSPO3激活肝细胞的WNT/β-catenin信号通路,这一通路是肝脏分区和功能的核心调控者。RSPO3的缺失直接导致肝细胞代谢“地图”混乱,再生与修复能力失调。
二、RSPO3:HSCs手中的“调控密钥”
1. RSPO3如何塑造肝脏的“功能地图”?
肝脏代谢具有严格的分区特性:
-门静脉区(Zone 1):参与糖原储存和胆汁酸代谢。
-中间区(Zone 2):兼具再生潜能。
-中央静脉区(Zone 3):高表达CYP450酶,负责解毒。
小百科:何为肝脏分区(liver zonation)
根据与门管区和中央静脉的相对位置,肝细胞被划分为三个功能迥异的区域:
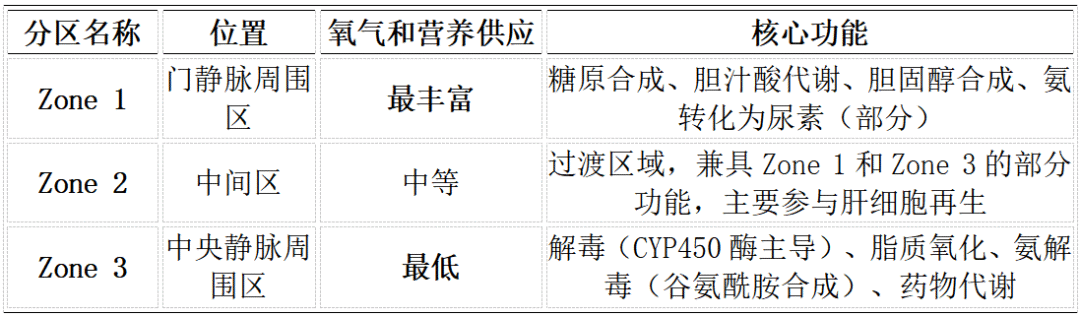
当肝脏分区被破坏时,功能失衡可导致多种疾病:
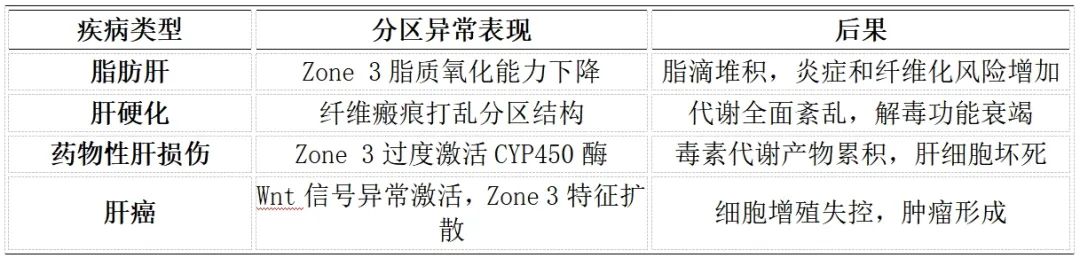
研究发现,HSCs分泌的RSPO3形成从中央到门静脉的浓度梯度,通过激活LGR4/5受体,维持各分区标志物的精准表达。当HSCs特异性敲除RSPO3时,Zone 3区域缩小,Zone 1异常扩张,肝脏代谢功能全面紊乱(见图1)。
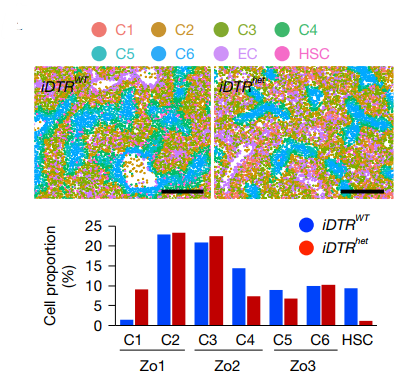
图1:上图表明定向清除HSCs后(iDTRhet)zone 1(Zo1,红色)明显扩大,而zone 3(Zo3,红色)则明显缩小
来源:原文图2f
2. RSPO3缺失:再生与损伤的“双刃剑”
-再生受阻:在70%肝切除模型中,RSPO3敲除小鼠的肝细胞增殖速度降低,修复延迟。
-损伤矛盾:
-
-中央区毒素(如CCl₄):损伤减轻(因代谢酶减少,毒素活化减弱)。
-
-门静脉区毒素(如烯丙醇):损伤加剧(因Zone 1扩张,敏感区域扩大)。
这一发现解释了为何HSCs在不同肝病模型中表现迥异。

图2:上图表明用iDTR定向清除HSCs后(iDTRhet),在APAP模型中,坏死区域变小,而在Allyl酒精模型中,坏死区域变大
来源:原文图1 d、f
3. 临床关联:RSPO3水平预测肝病进展
研究团队分析了酒精性肝病(Alcoholic liver disease,ALD)和代谢相关脂肪肝(Metabolic dysfunction-associated steatotic liver disease,MASLD)患者的肝组织样本,发现:
-疾病早期:HSCs高表达RSPO3,WNT信号活跃,肝脏功能尚可维持。
-晚期纤维化:RSPO3表达骤降,伴随代谢紊乱和再生能力衰竭。
这表明RSPO3水平可作为肝病预后的生物标志物,高表达患者生存率显著提升。
三、从实验室到临床:肝病治疗的新靶点
1. 修正HSCs的“污名”:从促纤维化到促修复
传统抗纤维化策略聚焦于抑制HSCs活化,但新研究表明,恢复HSCs的“静息状态”可能更有效:
-TGF-β抑制剂:阻断HSCs活化信号,恢复RSPO3分泌。
-RSPO3替代疗法:通过基因递送或重组蛋白补充RSPO3,直接激活WNT通路。
2. 精准干预肝病进程
-酒精性肝病:补充RSPO3可增强肝细胞解毒能力,减少脂肪堆积。
-脂肪肝与肝癌:激活WNT信号可抑制脂质沉积,延缓纤维化向肝癌转化。
动物模型中,RSPO3过表达显著改善了高脂饮食诱导的脂肪肝和肿瘤形成。
3. 挑战与展望
-平衡之道:过度激活WNT信号可能促进肝癌,需精准调控。
-递送技术:如何靶向HSCs或肝细胞仍是难点,纳米载体或病毒载体可能是突破口。
四、改写教科书:肝脏微环境的“三重奏”
此前认为,肝脏分区由内皮细胞(ECs)分泌的WNT蛋白主导。新研究提出“HSCs-ECs-肝细胞”三方协作模型:
-ECs:分泌WNT2/9b,维持中央区高WNT活性。
-HSCs:通过RSPO3放大WNT信号,调控大部分肝细胞功能。
-肝细胞:通过LGR4/5接收信号,决定代谢与再生命运。
这种协作如同交响乐,HSCs担任“指挥”,确保各区域和谐运转。
结语:重新定义HSCs的使命
这项研究打破了“HSCs=纤维化”的刻板印象,揭示其在肝脏稳态中的核心地位。未来,针对HSCs-RSPO3轴的治疗策略,不仅有望逆转纤维化,更能从根源恢复代谢与再生功能。正如研究者所言:“HSCs不再是‘敌人’,而是需要被重新招募的’盟友’”。
引证本文
Sugimoto, A., Saito, Y., Wang, G. et al. Hepatic stellate cells control liver zonation, size and functions via R-spondin 3. Nature (2025).
https://doi.org/10.1038/s41586-025-08677-w

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












肝脏是人体最大的代谢器官,承担着解毒、合成、储存等关键功能
2
#肝星状细胞# #RSPO3#
3