【Blood】How I Treat:异基因移植后复发的AML
2025-01-01 聊聊血液 聊聊血液 发表于陕西省
Dana-Farber癌症研究所Robert Soiffer教授等通过三个具体病例,讨论了早期、晚期和初发(incipient)复发的管理,并构建了针对移植后复发的治疗原则。
AML移植后复发
异基因造血干细胞移植(allo-HCT)是治疗急性髓系白血病(AML)的主要方法之一,但移植后复发仍预后不良, 1 年总生存率(OS)仅为 23%。
尽管对于移植物抗白血病效应的免疫生物学以及导致移植后复发的免疫逃逸机制的理解不断深入,但过去三十年间复发率仍保持不变。移植后复发的治疗高度个体化,取决于疾病生物学和基因组学,以及患者复发时的临床状况和复发与移植之间的间隔。
《Blood》近日发表的一篇文章中,Dana-Farber癌症研究所Robert Soiffer教授等通过三个具体病例,讨论了早期、晚期和初发(incipient)复发的管理,并构建了针对移植后复发的治疗原则。

患者 1:
患者为70 岁、身体状况良好的男性,诊断为AML,初步检查显示白细胞计数(WBC)为 67000,成髓细胞(myeloblasts) 85%。骨髓活检(BMBx)显示正常的 46,XY 染色体核型。二代测序(NGS)检测显示携带 FLT3-ITD 变异等位基因,变异等位基因频率(VAF)为 47%(等位基因比例为 0.89),同时伴有 DNMT3A 和 WT1 突变。根据ELN风险分类,从遗传学角度归为中危。接受强化诱导化疗,方案为阿糖腺苷和柔红霉素(7+3)联合midostaurin,并获得完全缓解(CR)。患者接受两个周期的中剂量阿糖腺苷治疗,随后进行单倍体相合减低强度预处理(RIC)HCT,预处理方案为Flu/Cy/TBI,预防移植物抗宿主病(GVHD)的方案为 PTCy/Tac/MMF。最初从第+60 天开始服用索拉非尼维持治疗,但由于耐受性差,一个月后停药。移植四个月后复发,穿刺物涂片显示原始细胞23%。NGS检测panel重新表明为最初的 FLT3-ITD 克隆,VAF为 11%。
治疗考虑:
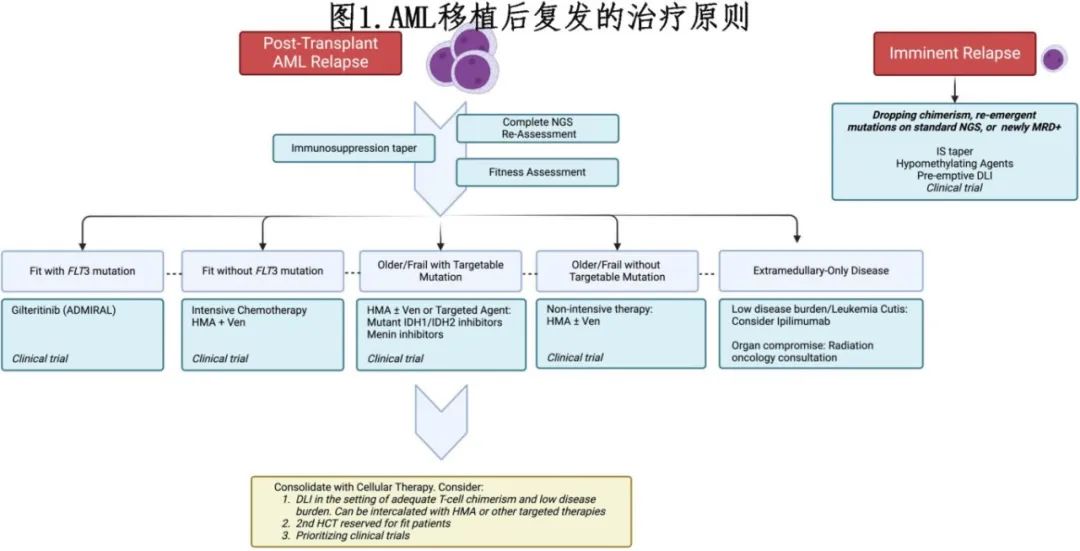
HCT后早期复发的考虑因素包括:(1)如果仍在服用免疫抑制剂,则逐渐减少免疫抑制(IS);(2)根据fitness和完整的基因组再评估结果,用化疗或靶向药物处理白血病本身;(3)以供者淋巴细胞输注(DLI)或二次移植的形式进行细胞治疗巩固。
(1) 对于仍在使用免疫抑制剂且无活动性移植物抗宿主病的复发患者,初始干预通常为迅速减少免疫抑制剂的用量,从而通过重新激活供者T 淋巴细胞来产生移植物抗白血病(GVL)效应。一项回顾性分析显示,仅进行免疫抑制剂减量,而未进行其他治疗干预(化疗、DLI或二次HCT),即可导致部分患者出现临床反应,且RIC中较MAC中的反应更为频繁(32.7% vs 4.5%,p=0.0007)。大多数(97%)反应伴随着GVHD爆发(flare)。单纯IS减量在约 80%的患者中不成功,并且在面对增殖性疾病时也不够充分,因此可能需要同时或在IS减量后很快使用靶向或非靶向化疗药物,随后进行巩固性细胞治疗。当出现即将复发的临床迹象(如髓系或 T 细胞嵌合度下降或分子突变重新出现)但尚未出现明显形态学复发时,也可使用 IS 减量。
患者 1(续):
该患者逐渐减量并停用他克莫司,停用免疫抑制剂三周后患者报告出现与GVHD相符的皮疹,经局部皮质类固醇治疗后控制良好。开始每日服用 120mg吉瑞替尼,后达到CR并接受 3 次DLI巩固治疗。由于转氨酶升高,担心肝脏 GVHD而暂停DLI。
(2) 在这种情况下,化疗药物的选择取决于许多因素,包括可靶向突变的存在、疾病负担和速度(tempo),以及患者fitness。目前有许多靶向药物可用,且在某些情况下治疗复发性AML中优于化疗。ADMIRAL 试验在FLT3+(ITD AR≥0.05)复发/难治性(R/R)AML 中对比FLT3 抑制剂吉瑞替尼(靶向 ITD 和 TKD 突变)与研究者选择的挽救化疗;包括 20%的患者为HCT后复发。缓解率(34% vs 15.3%)和中位OS (9.3 个月 vs 5.6 个月)均有利于吉瑞替尼。真实世界证据表明在接受过 FLT3 抑制剂治疗的患者中吉瑞替尼也存在临床活性,就像上述患者一样。与研究究者选择的化疗相比,Quizartinib在 FLT3-ITD(变异等位基因频率≥3%)突变R/R AML中也更优。因此如果存在 FLT3 突变,FLT3 抑制剂(通常为吉瑞替尼)可作为初始化疗策略的一部分。上述患者在复发前还接受了多激酶抑制剂索拉非尼维持治疗,这是基于两项随机试验显示无复发生存期(RFS)和OS获益。此外小鼠模型表明,索拉非尼可以通过 FLT3-ITD 突变白血病细胞产生off-target白细胞介素-15 来增强GVL,与异基因 CD8+T 细胞的 GVL 反应具有协同作用。有趣的是,最近报道的 MORPHO 试验(使用吉瑞替尼维持治疗)表明,维持治疗可能只对移植前或移植后MRD阳性患者有必要,尽管该结果可能仅适用于该药。与上述患者一样,SORMAIN 试验中治疗中断最常见的原因为不良事件,这是一个反复出现的现实问题。
对于不适合诱导化疗或作为细胞毒化疗辅助治疗的患者,有越来越多的靶向药物可供选择,包括 IDH1 和 IDH2 抑制剂。目前尚无专门针对移植后复发的前瞻性研究,这一人群在R/R临床试验中往往只占少数,因此药物的选择和预期疗效往往是推断自 R/R 试验结果。有关 R/R AML关键临床试验的总结见表 1 。
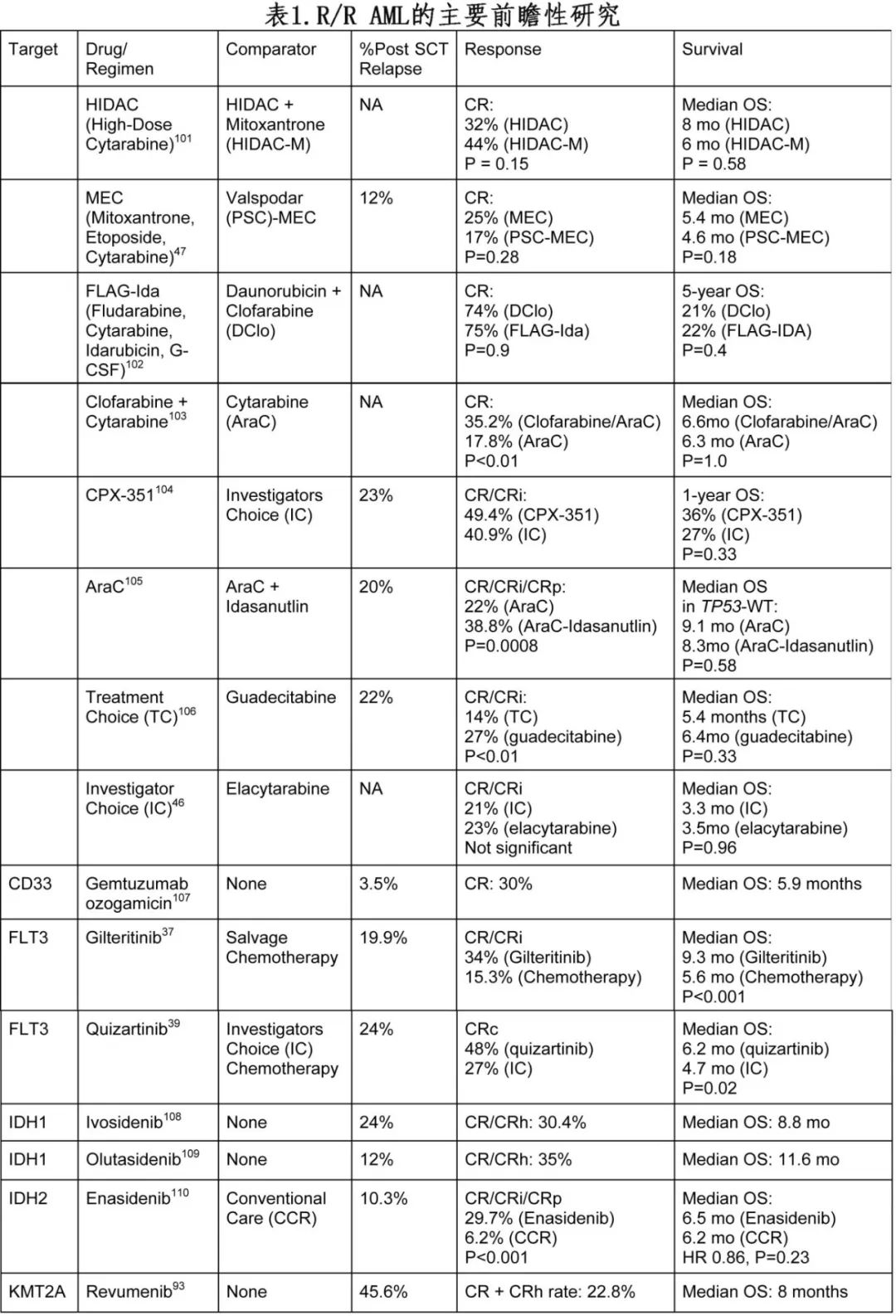
对于特定年轻和fit的化疗敏感患者,可以给予细胞毒性化疗,但缓解率较低且毒性可能较大。在前瞻性随机试验中,单独细胞毒化疗的缓解率为10-40%,中位OS在3-6个月之间,而低强度治疗(如去甲基化药物)单药治疗的结果同样不佳。联合维奈克拉(Ven)治疗彻底改变了老年AML患者的一线治疗,特别是对于非TP53突变患者,并且越来越多地用于R/R患者,其缓解率与细胞毒化疗相似,尽管没有随机证据。在大剂量化疗的基础上加入维奈克拉可能是某些患者的有用策略,因此选择高强度或低强度治疗主要基于患者因素、既往治疗以及哪些疾病亚型可能对基于维奈克拉的治疗或细胞毒化疗最敏感。
(3) 以DLI或二次HCT的形式进行巩固性细胞治疗,可以在部分HCT后复发的患者中实现持续缓解。DLI 包括输注未经处理的供体外周血 T 淋巴细胞,通常以连续递增的剂量分几个等分输注,并密切监测GVHD(最常见的毒性反应)。DLI 最初被证明对接受去除 T 细胞移植的慢性粒细胞白血病(CML)患者有效,但随后应用于其他血液恶性肿瘤也获得不同程度的成功。在AML中,一项回顾性研究纳入 399 例HCT后首次血液学复发患者,显示DLI 治疗的 2 年OS为 21%,而未DLI的为 9%;DLI 组的多因素分析显示,在缓解/良好核型时进行 DLI 治疗的 2 年OS为 56%,而复发或伴有骨髓衰竭时进行 DLI 时为 15%。DLI 时低疾病负荷也是生存的独立预后因素。因此,尽管 DLI 有获益,但患者选择对于其成功也至关重要。在CML中,总核细胞(TNC)剂量为 1×107细胞/千克有效且GVHD可接受。后来在AML中进行的一项研究表明,剂量>10×107与 GVHD 风险增加有关,但反应相似。因此对于HLA相合供者,作者从 1×107开始,并根据耐受情况逐渐增加至最大 3-4 次给药,同时建议在单倍体移植中或如果以抢先或预防的方式使用 DLI,则采用稍低剂量(1x106) 。虽然 DLI 有效的确切机制仍不清楚,但在成功DLI 几个月后,T 细胞受体(TCR)多样性有显著改善;也有研究在复发性 CML 中表明,对 DLI 的反应与既往存在的骨髓浸润性 CD8+ T 细胞以及T 细胞耗竭局部逆转有关。AML中 DLI 的机制基础仍不完全理解,作者单位最近表明,DLI 应答者中存在ZNF683+ GZMB+ CD8+ 细胞毒 T 淋巴细胞 (CTL),DLI无应答者中存在表达TIGIT的CTL。更好地理解过继细胞治疗产品与骨髓微环境之间的相互作用,或许可以解释CML和AML中DLI临床反应的差异。
DLI 的替代方案为二次HCT,详见第二例患者。目前没有前瞻性研究来帮助决定二次HCT 还是 DLI作为巩固性细胞治疗。然而多项大型回顾性分析表明,两种干预措施的 2 年OS都在 25%左右,且在 HCT后>6 个月复发以及在细胞治疗前实现低疾病负荷的患者预后更好。回顾性数据表明,不同供者类型可获得相似的结果,但单倍体相合供者的NRM略高。随着越来越认识到未共享单倍体的丢失是单倍体相合移植免疫逃逸的重要机制,评估 HLA 丢失的检测方法也正在开发中。如果单亲二倍体(uniparental disomy)确实是复发的机制,那么来自原始供者的DLI预计无效,而二次移植可能是更好选择。目前这些检测方法大多处于研究阶段。总之,如果复发发生在 6 个月内,如果存在一定程度的供者 T 细胞嵌合,并且疾病负担不是过大,则作者倾向于DLI;而对于fit且复发时间>6 个月的患者,则考虑二次HCT,最好在MRD阴性缓解期。
患者 2:
患者为34 岁女性,白细胞计数为 17 万,伴有皮肤病变。骨髓活检显示de novo AML(正常核型伴 NPM1、DNMT3A 和 NRAS 突变)。皮肤病变活检显示白血病皮肤(leukemia cutis.)。接受7+3 诱导化疗,通过检测达到形态学缓解伴NGS panel阴性,但通过流式细胞术检测到MRD。随后接受一个周期大剂量阿糖腺苷巩固治疗,并在MAC HCT后转为流式MRD阴性,HLA相合无关供者伴Tac/MTX预防GVHD。在移植 16 个月后出现胸膜炎性胸痛,胸部 CT 显示左侧胸壁前下壁、左侧胸膜、左心室心尖和房间隔有多处新的软组织肿块,PET/CT 扫描显示广泛的 FDG摄取髓外(EM)病变。右腋窝肿块活检显示为伴有 NPM1 突变的髓系肉瘤,同时进行的骨髓活检显示没有形态学复发的证据,但 NGS panel再次证实诊断性 NPM1 突变。立即接受米托蒽醌/依托泊苷/阿糖腺苷再诱导治疗,并发严重的真菌性肺炎和去适应(deconditioning)。由于无供者而不适合DLI,且根据 ECOG 评分 3 级,也不适合二次HCT。缓解3 个月后再次复发,出现白血病皮肤。随后在试验中接受ipilimumab(Ipi)治疗,皮损消退 6 个月,之后骨髓进展,最终死于疾病复发。
治疗考虑:
孤立性 EM 复发是异基因HCT后复发的一种独特模式,在各种研究中的发病率在 4-10%之间,且HCT 后至复发的间隔明显长于骨髓复发。预后的预测因素包括不良风险细胞遗传学、HCT 前既往 EM 病变以及 AML FAB M4 和 M5 疾病。3年OS在 20-30%之间,总体上优于骨髓复发。其与骨髓复发的差异表明存在不同的免疫逃逸机制,最终导致预后的差异。
晚期复发发生时通常已经停用IS,因此逐渐减少 IS 使用并非常见选择。在晚期 EM 复发的情况下,关键的考虑因素包括:(1)存在可靶向的突变;(2)评估疾病负担,将决定需要立即进行化疗还是考虑免疫疗法(如检查点抑制剂);(3)是否需要局部放疗或CNS治疗;(4)
考虑巩固性DLI或二次HCT。由于该情况下并无FDA批准药物的可靶向突变,且患者复发侵袭性EM疾病损害终器官功能,因此采用细胞毒化疗进行减瘤是合适的,并在需要的时候辅以局部放疗以保持终器官功能或提供症状缓解。
化疗后巩固性细胞治疗,尤其是二次HCT是合理的,因为 HCT 与复发之间的间隔时间较长。然而患者的体能状况可能不佳,这在真实世界复发中并非罕见,并且二次 HCT 通常比首次移植更具毒性。一项回顾性研究纳入3356例患有各种血液恶性肿瘤的二次移植患者,显示2年OS为 38%,PFS为 28%,NRM为 22%,复发率为 50%,这些结果比之前更令人鼓舞。高龄、体能评分低、疾病风险指数高、首次 HCT 后早期复发(<6个月)、无关/单倍体相合供者、二次移植前发生GVHD以及移植时疾病负担与预后相关。一项以AML为重点的研究中发现,供者类型、年龄和二次 HCT 时的疾病状态、体内去除T细胞和Karnofsky指数与 NRM 相关。有研究表明,对于EM复发,DLI的效果较差。
该病例有一个奇怪特征,那就是在EM病变缓解及使用Ipi治疗后白血病皮肤复发。T 细胞上的细胞毒性 T 淋巴细胞相关蛋白 4(CTLA-4) 和程序性死亡 1(PD-1) 受体通过其各自的配体 (B7-1/B7-2) 和 (PD-L1/PD-L2) 参与肿瘤细胞,抑制 T 细胞效应功能,理论上可导致免疫逃逸和复发。在小鼠模型中的实验表明,在HCT后的晚期复发中,使用 Ipi(人类 IgG1 κ单链抗体)阻断 CTLA-4 可导致GVL增强,且不引起GVHD。这在一项 1/1b 期剂量递增研究(n=28)中得到应用,该研究使用 Ipi 治疗HCT后的复发。4 例EM AML患者获得CR,其中 3 例存在白血病皮肤。21%的患者出现免疫不良影响,14%的患者出现GVHD,通常对皮质类固醇有反应。虽然作者不在EM复发(除临床试验外)中常规使用免疫疗法,但检查点阻断在白血病性皮肤中的增强疗效很有意义,表明肿瘤微环境的组织特异性影响,这应成为未来工作的重点。
患者 3:
患者为68 岁男性,有前列腺癌病史,曾接受放疗和化学去势治疗,在一次常规的术前检查中发现全血细胞减少。骨髓活检显示AML,原始细胞 21%,伴有显著的发育不良。染色体核型分析显示复杂核型,包括 17p 缺失。NGS检测显示 TP53 突变和 NRAS 突变。接受两个周期的地西他滨/ Ven(DEC/Ven)治疗后达到CR,随后接受HLA相合无关供者RIC HCT,使用氟达拉滨/白消安预处理,以及Tac/MTX预防GVHD。移植三个月发现供者嵌合体减少,通过临床NGS发现初始 TP53 突变复发,以及复杂细胞遗传学,从而提示免疫抑制(IS)逐渐减少。不久之后,供体嵌合体持续减少促使进行了及时的预防性治疗,包括HMA和DLI。不幸的是患者疾病进展并在两个疗程后死亡。
治疗考虑:
对于HCT后的分子学复发,目前没有标准治疗;但人们现在普遍认识到,一旦出现复发性突变或 T 细胞嵌合体水平下降,预后就会很差,从而强调了针对这些情况采取新方法的必要性。作者优先考虑将高复发风险患者(HCT前MRD+,高危基因组学)纳入预处理强化、移植后维持、使用围移植期过继细胞治疗或新型移植物工程化的临床试验,以使 GVL最大化,但 FLT3抑制剂维持治疗除外,期待随机试验的数据,以最终证明这些方案中哪个有生存获益。对于维持治疗策略,很大程度上要么是对高危患者的预防性治疗,要么是在发现嵌合体水平下降、MRD 检测或分子学复发时采取的预防性措施,无论使用靶向药物还是突变诊断策略。移植后MRD评估的频率尚未明确界定,建议在移植后每月监测嵌合状态,每三个月监测MRD,遵循ELN MRD 工作组的指导、专家共识和机构指导。在临床试验之外,对于嵌合状态下降、检测到 MRD 或分子学复发的患者,作者一般逐渐减少IS并在可行的情况下联合去甲基化药物和DLI,这些方法在不同程度上均取得成功。值得注意的是,EBMT 的最佳实践建议包括在预防性/抢先性治疗中使用较低剂量DLI。
在 TP53 突变AML中,一旦检测到形态学复发,采用HMA(DEC 或阿扎胞苷/AZA)嵌入DLI可作为选择,不过既往接触过这些药物的患者中疗效尚不清楚。在HCT前,TP53 突变的寡细胞性 AML 和MDS患者接受 HMA 治疗后CR率为 15-20%,与野生型 TP53 患者相似,但缓解通常短暂,中位总生存期在 5-12 个月。在一项 II 期随机研究中,发现 10 天与 5 天的 DEC 治疗方案并无显著差异。根据这些数据推断,作者更倾向于采用 5-7 天的 HMA 作为初始治疗,并在每个周期后添加 DLI,完成 4-5 个周期的 DLI。如果疾病负担较低则添加 DLI 最有可能成功,因此患者通常会在添加 DLI 之前单独接受几个周期的 HMA治疗。如果通过 HMA加 DLI 实现 CR,则根据医生判断继续进行 HMA维持治疗;建议至少治疗 2 年。
在HMA中添加第二种药物的尝试取得了不同程度的疗效。维奈克拉与低强度化疗方案的联合已成为老年unfit成人AML的标准一线治疗;此外,DEC/Ven 联合在高危 AML 中也有效。然而维奈克拉在 TP53 突变髓系疾病中疗效不佳。
未来方向/前景
移植后急AML复发在病理生物学方面仍存在许多未解决的问题,包括如何将对复发生物学和白血病免疫逃逸的理解转化为临床检测和治疗干预措施。HCT后复发的重要早期步骤包括确定fitness以及通过NGS对疾病进行全面重新评估,同时还要认真讨论患者的偏好和质量目标。未来发展方向可分为以下几类:
1. 预后和复发预测。在不久的将来,NGS MRD检测的标准化和解读方面的进步将使几乎所有AML亚型能够检测到早期复发,并有可能进行干预。对于老年患者,移植前的 NGS-MRD 往往反映出诊断时的化疗耐药生物学(例如MDS相关和 TP53 突变),正在进行的工作旨在阐明如何应对移植前的MRD,以及何时监测和干预移植后的分子学复发。此外,MRD检测对复发风险的敏感性并不完美,而功能性检测方面的进步可能会提供额外的预后和治疗信息。人们对于使用靶向或低强度治疗作为移植后维持治疗以降低复发风险很感兴趣,也希望基于MRD或其他因素确定可能确定可获益于移植后维持治疗的患者亚群。
2. 新型药物:预计获批用于治疗复发性AML的靶向药物数量将继续增加,包括小分子药物和基于抗体的策略。menin制剂revumenib现已获批用于治疗R/R KMT2A重排AML,并在 NPM1 突变白血病中进行研究,在移植后患者中也有一些经验。TP53 突变AML仍存在是重大挑战。APR-246(eprenetapopt)是一种假定的 TP53 稳定剂,在移植后与阿扎胞苷联合使用时显示出良好疗效,然而由于美国FDA无限期暂停导致该药物无法使用。在开发基于抗体和CAR-T的疗法用于髓系恶性肿瘤时,确定优先存在于原始细胞而非健康造血祖细胞上的抗原靶点一直是挑战。靶向CD3 和 CD123 的双特异性抗体正在研发中。
3. 过继细胞疗法的创新。目前尚无明确数据表明在移植后复发中应采用DLI、二次HCT还是两者联合。这些方法中的任何一种的生存率均有限,促使人们努力优化过继细胞治疗平台。细胞因子诱导的记忆样(CIML)NK细胞是异基因供者来源的NK细胞,经过细胞因子处理后,在移植前具有抗白血病活性,移植后数据也在逐渐增加。其他调整包括在Treg细胞耗竭的DLI中添加免疫检查点抑制剂(NCT03912064)、HMA联合来那度胺、更好地阐明次要组织相容抗原(mIHA)作为GVL抗原靶点、自体CAR或使用异基因供者来源的T细胞受体工程化T细胞(分别针对HA-1和HA-2血细胞抗原,两者均在HLA-A*02:01上表达,这是一个有前景的新前沿)。
总之,HCT后AML的复发是一个重大挑战,预后不良。在相对较小的一部分病例中,采用IS减量联合化疗/靶向治疗,以及巩固性过继细胞治疗(DLI 和/或二次HCT)可带来长期缓解,并保持良好的生活质量。作者提出的治疗原则见图 1,但其受限于移植后治疗中缺乏前瞻性数据。出于这个原因,应优先登记参加临床试验,并就治疗目标进行谨慎讨论,特别是对于衰弱患者或高度耐药的患者(可能最适合接受以安慰为重点的治疗),这些都是普遍原则。
参考文献
Mahasweta Gooptu, H. Moses Murdock, Robert J. Soiffer; How I Treat AML relapse after allogeneic HCT. Blood 2024; blood.2024025705. doi: https://doi.org/10.1182/blood.2024025705
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#AML# #异基因造血干细胞移植#
15