Mol Cell:PI3Kb通过促进细胞蛋白O-GlcNAcylation和乙酰辅酶A生成推动肿瘤生长
2025-03-29 MedSci原创 MedSci原创 发表于陕西省
该研究揭示了PI3Kb在肿瘤生长中的新作用机制,即通过磷酸化OGT增强细胞蛋白O-GlcNAcylation,进而促进ACLY活性和乙酰辅酶A生成,为肿瘤生长提供能量和物质基础。
磷脂酰肌醇 3-激酶(PI3K)在肿瘤发展中发挥着关键作用,其传统认知是作为一种脂质激酶,通过磷酸化磷脂酰肌醇 4,5-二磷酸(PI(4,5)P2)产生磷脂酰肌醇 3,4,5-三磷酸(PI(3,4,5)P3),从而激活 AKT 等下游效应蛋白,促进细胞生长、增殖、迁移和存活等过程。然而,PI3K 是否存在与 PI(3,4,5)P3 生成无关的其他功能,对于肿瘤发展同样至关重要,目前尚不明确。
本研究聚焦于胶质母细胞瘤(GBM),这是一种常见的恶性脑肿瘤,具有高度的侵袭性和致死性。既往研究表明,PI3K 信号通路在 GBM 中异常激活,是重要的治疗靶点。然而,针对 PI3K 的传统抑制剂在临床应用中效果有限,提示可能存在其他尚未揭示的调控机制。
近日,国际权威期刊Molecular Cell上在线发表了题为“PI3Kb functions as a protein kinase to promote cellular protein O-GlcNAcylation and acetyl-CoA production for tumor growth”的最新研究成果,该研究揭示了PI3Kb在肿瘤生长中的新作用机制,即通过磷酸化OGT增强细胞蛋白O-GlcNAcylation,进而促进ACLY活性和乙酰辅酶A生成,为肿瘤生长提供能量和物质基础。这一发现不仅拓展了对PI3K功能的认识,还为开发新型抗癌疗法提供了理论依据。

研究发现,在高葡萄糖条件下,己糖激酶 1(HK1)从线粒体转位至细胞质,磷酸化 OGT 的 Y889 位点,促进 p85a 的招募,进而介导 PI3Kb(p110b)与 OGT 的结合。这一过程不依赖于 PI3K-AKT 信号通路激活增强的糖酵解和己糖胺生物合成途径(HBP),而是通过一种新的机制增强细胞内蛋白 O-GlcNAcylation 水平。
PI3Kb 不仅是一种脂质激酶,还能够作为蛋白激酶直接磷酸化 OGT 的 T985 位点,显著增强 OGT 的活性。这种磷酸化修饰是 PI3Kb 促进 O-GlcNAcylation 的关键步骤,且不依赖于其传统的脂质激酶活性。
激活的 OGT 通过 O-GlcNAcylation 修饰 ACLY 的 T639 和 S667 位点,增强 ACLY 的活性,进而促进乙酰辅酶 A 的生成。乙酰辅酶 A 是脂肪酸合成和组蛋白乙酰化的重要前体,其增加有助于肿瘤细胞的增殖和生存。
研究团队通过细胞实验和动物模型证实,PI3Kb 介导的 OGT 磷酸化以及 OGT 介导的 ACLY O-GlcNAcylation 对 GBM 细胞的增殖和肿瘤生长具有重要促进作用。抑制这一信号轴的关键节点(如 PI3Kb、OGT、ACLY),可以显著抑制肿瘤生长,并延长裸鼠的生存期。
免疫组化分析显示,OGT Y889 和 T985 磷酸化水平在人 GBM 标本中呈正相关,且与蛋白 O-GlcNAcylation 水平和组蛋白 H3 乙酰化水平正相关,而与患者的生存期负相关。这表明 PI3Kb 通过蛋白激酶活性介导的 OGT 激活和乙酰辅酶A生成在GBM进展中具有重要的临床意义。
综上所述,本研究揭示了PI3Kb在肿瘤发展中的新功能,即作为蛋白激酶磷酸化 OGT,促进细胞蛋白 O-GlcNAcylation 和乙酰辅酶A生成,从而推动肿瘤生长。这一发现不仅丰富了对 PI3K 功能的认识,还为开发针对PI3K的新型抗癌疗法提供了理论依据。
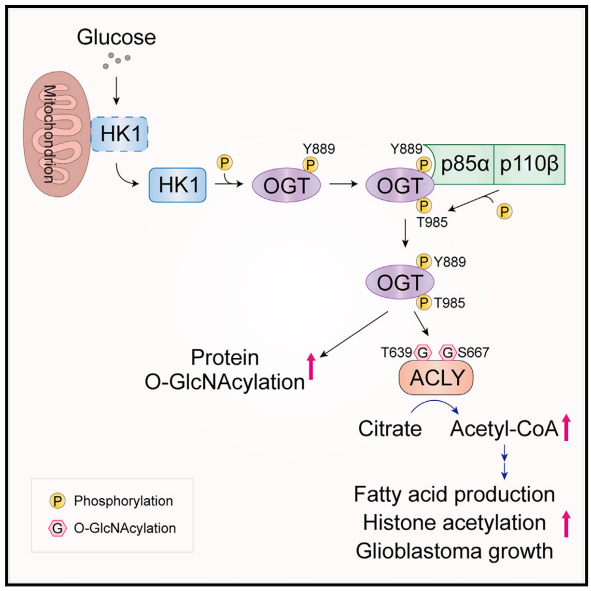
图 本研究模式图
原始出处:
PI3Kβ functions as a protein kinase to promote cellular protein O-GlcNAcylation and acetyl-CoA production for tumor growth. Mol Cell. 2025 Mar 19:S1097-2765(25)00186-8. doi: 10.1016/j.molcel.2025.02.024. Epub ahead of print. PMID: 40132583.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#胶质母细胞瘤# #乙酰辅酶A# #O-糖基化#
7