南开大学齐迹、史洋AFM:分级靶向材料用于NIR-II光声成像引导的胶质瘤协同免疫治疗
2025-03-31 BioMed科技 BioMed科技
胶质母细胞瘤侵袭性强、治疗难,南开大学齐迹和史洋团队设计分级靶向平台,将 NIR-II 光声成像与光化疗协同免疫治疗结合,为其诊疗提供新策略。
胶质母细胞瘤(GBM)是最具侵袭性的恶性脑肿瘤,其特点是预后差、复发率高、多种治疗耐药性。目前GBM的治疗方法包括手术、放疗和化疗。然而,这些方法存在局限性。值得注意的是,免疫治疗因其高效、特异性和低毒性而已成为一种很有前途的治疗选择。然而,肿瘤浸润淋巴细胞水平低和高免疫抑制的脑肿瘤微环境显著阻碍了GBM的免疫治疗的有效性。
早期精准诊断GBM对于及时治疗和改善患者预后至关重要。NIR-II光激发PA成像可以提供更高的信噪比(SNR)和增强的组织穿透深度。这些特征使NIR-II PA成像成为诊断深部原位脑肿瘤的一种极具前景的方法。然而,实现GBM的高效和靶向的NIR-II PA成像仍然是一项具有挑战性的努力,这主要是由于缺乏同时具有高光吸收能力和光声转换效率的高性能NIR-II PA成像剂。此外,迫切需要开发治疗诊断平台,不仅能够促进GBM的NIR-II PA成像,而且能够激发强有力的抗GBM免疫反应,以同时进行GBM治疗。
近日,南开大学齐迹和史洋教授等设计了一种NIR-II光声(PA)成像引导的光化疗协同免疫治疗GBM的分级靶向平台。这一诊疗一体化纳米平台将NIR-II区光声成像肿瘤诊断与自协同精准免疫治疗相结合,为推进胶质母细胞瘤(GBM)等深位难治性肿瘤的诊断与治疗提供了前景广阔的新策略。研究成果以“Hierarchical Targeting Nanoplatform for NIR-II Photoacoustic Imaging and Photo-Activated Synergistic Immunotherapy of Glioblastoma”为题发表《Adv. Funct. Mater.》期刊。这项工作为攻克深部低免疫原性脑肿瘤的诊断与治疗难题提供了一种新策略。

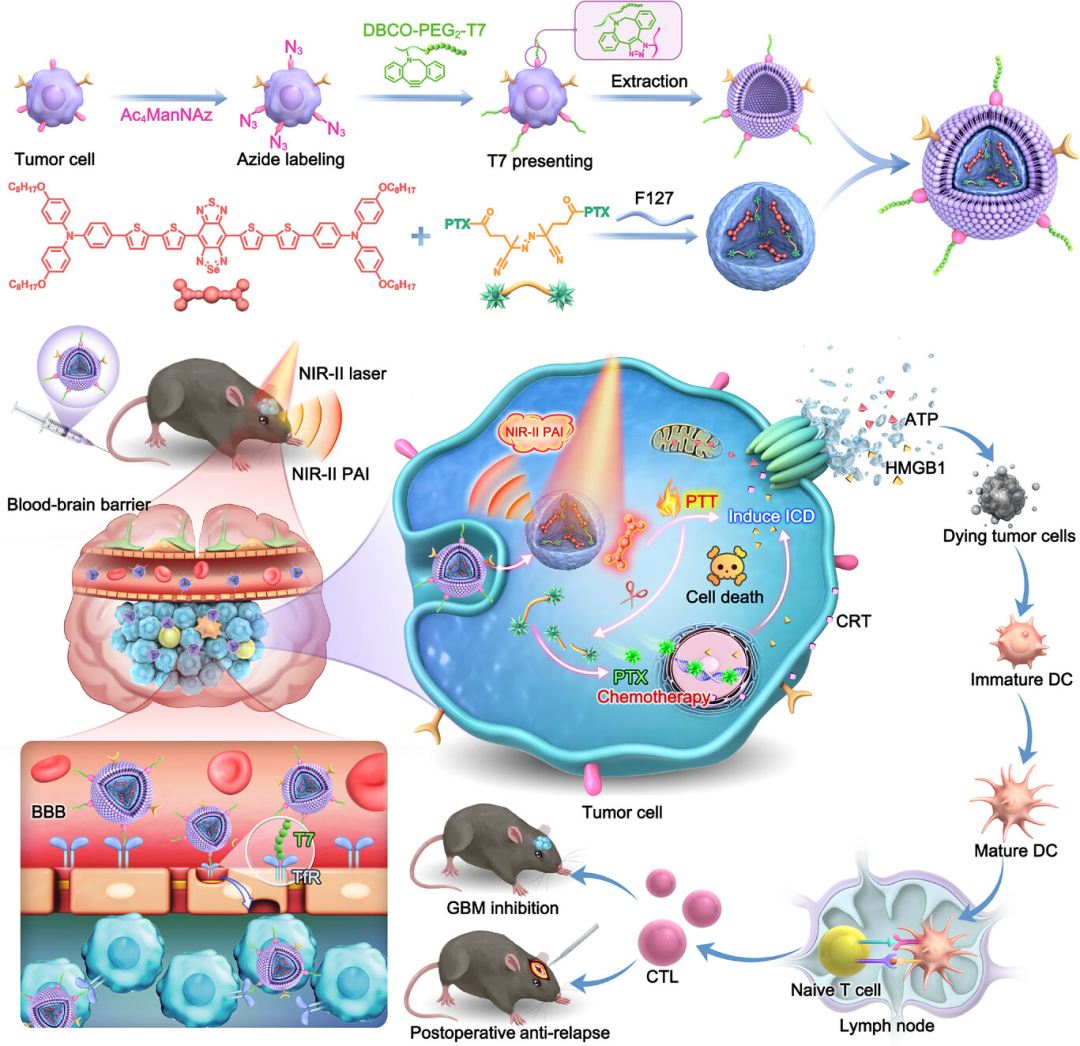
研究设计与研究示意图
作者设计并合成了两种"供体-受体-供体"(D-A-D)型分子。通过密度泛函理论(DFT)计算深入分析分子结构。最高占据分子轨道(HOMO)和最低未占分子轨道(LUMO)电子云的分离表明其具有高效的分子内电荷转移(ICT)特性。计算结果显示, TTBSe的电子带隙(0.90 eV)小于硫取代分子TTBS(0.97 eV),这归因于硒原子具有更强的亲电性。
TTBS和TTBSe在近红外区均表现出强吸收特性。为了使疏水分子具有水溶性,将TTBS和TTBSe封装成NPs,分别得到S NPs和Se NPs。Se NPs具有更高的光热转换效率。TTBSe的强NIR-II吸收和高PCE使其成为NIR-II光热及相关应用的理想候选材料。与溶液状态相比,TTBS和TTBSe的光致发光强度都有所降低。TTBSe的猝灭效果比TTBS更明显。这表明TTBSe的光激发态能量主要指向非辐射衰减途径,使其在PA和PTT的应用中特别有利。此外,为了开发一种光热激活前药,偶氮基团被设计为在热刺激下分裂,从而释放PTX。
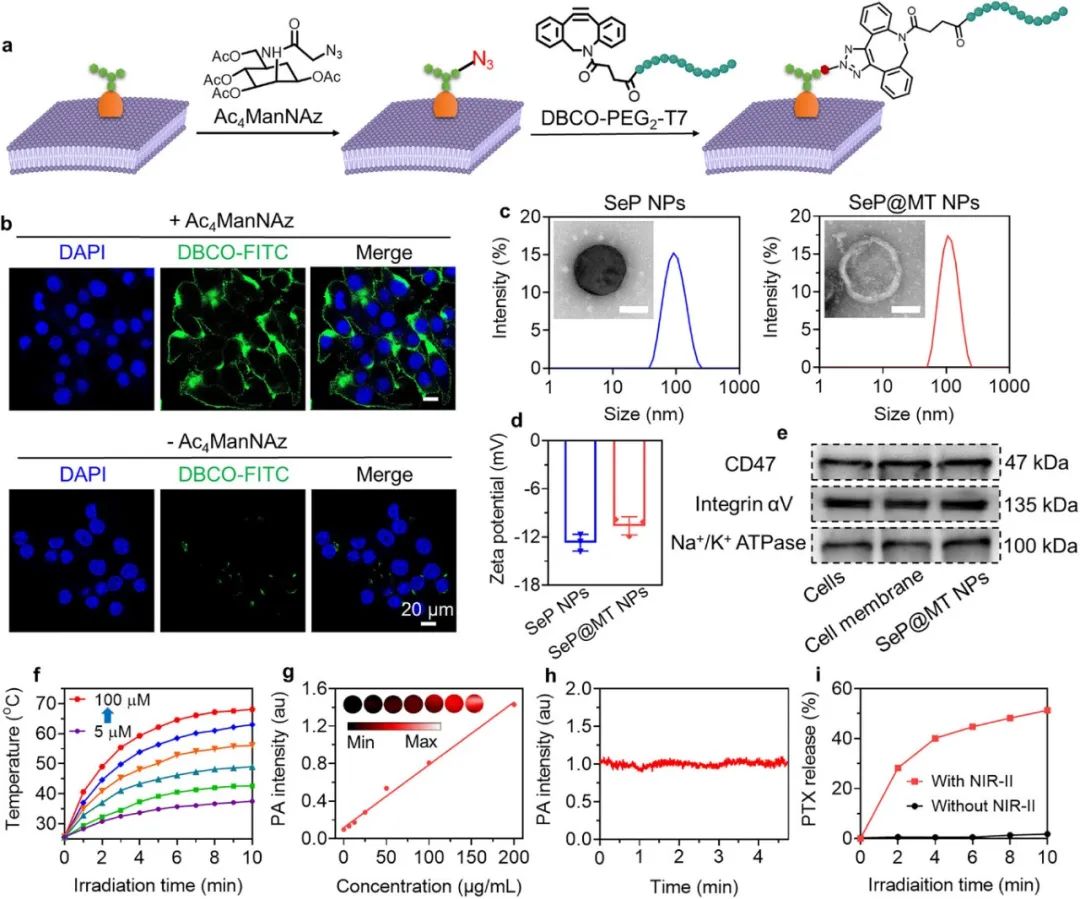
纳米制剂的制备和表征
采用纳米沉淀法,将TTBSe和PTX-Azo制备成水溶性纳米粒(SeP NPs)。为增强其对GBM的靶向性,用胶质瘤细胞膜进行了伪装修饰。为突破脑胶质瘤诊疗中的血脑屏障限制,通过生物正交化学反应将转铁蛋白模拟肽T7偶联至细胞膜表面。最终成功构建了SeP@MT纳米粒。采用动态光散射(DLS)和透射电子显微镜(TEM)对纳米制剂的尺寸与形貌进行表征。SeP@MT NPs展现出卓越的光热与光声性能。此外该探针具有光热触发活化特性。SeP@MT NPs中的PTX-Azo前药能在NIR-II激光照射下实现高效激活。

体内抗GBM的疗效
作者使用原位GBM模型评估体内胶质瘤靶向光免疫治疗的疗效。 “SeP@MTNPs+L”治疗显著延缓了肿瘤生长。体内治疗结果表明,SeP@MT NPs + L治疗由于其强大的抗肿瘤特性,有效地减轻了脑胶质瘤的有害作用。用苏木精和伊红(H&E)染色染色结果表明使用SeP@MT NPs + L对肿瘤生长的抑制最为显著。TUNEL染色检测不同处理后体内GBM细胞凋亡情况。用SeP@MT NPs + L处理在脑肿瘤组织中产生了强烈的绿色荧光,表明肿瘤细胞内存在广泛的凋亡。这些结果强烈暗示了SeP@MT NPs在光照射下具有强大的肿瘤杀伤作用。
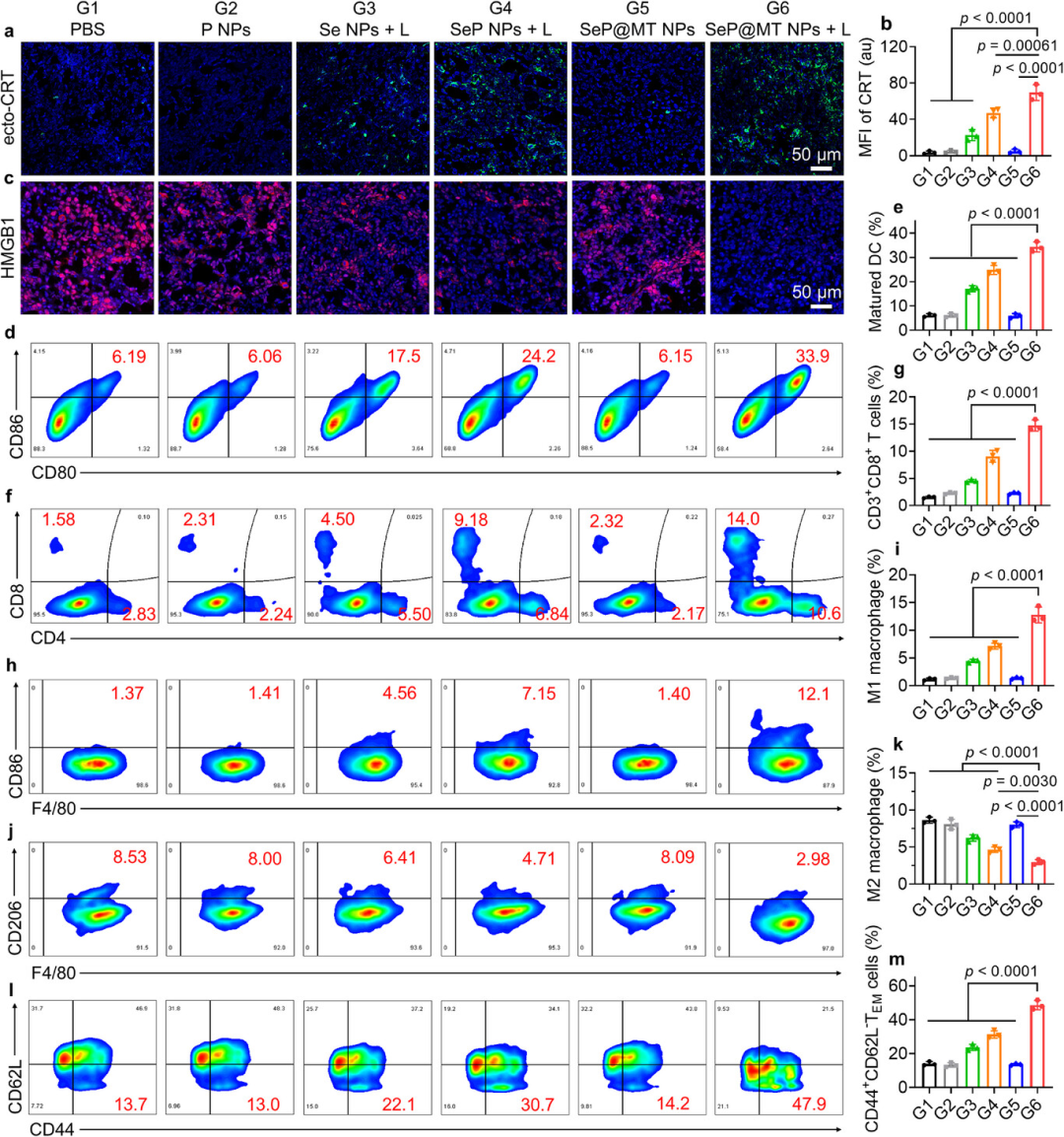
体内抗肿瘤免疫激活性质研究
作者开发了一种多功能的分级靶向纳米平台,用于NIR-II PA成像引导的GBM光化学串联免疫治疗。在静脉注射GBM小鼠模型后,纳米制剂有效地定位于肿瘤病变,发出明亮的NIR-II PA诊断信号,具有高信噪比和深组织穿透的特征,允许精确描述肿瘤的位置和大小,并为后续治疗干预提供可靠的指导。在NIR-II光照射下,轻度PTT和肿瘤特异性前药激活协同增强肿瘤细胞的破坏,放大抗肿瘤免疫反应。这一过程模拟了一个“热的”的肿瘤免疫生态位,重塑巨噬细胞表型,刺激肿瘤特异性T细胞免疫。联合免疫治疗效果可显著抑制GBM肿瘤,显著减少切除后胶质瘤的复发,并延长了治疗动物的生存期。该诊疗一体化纳米平台为深部低免疫原性肿瘤(如GBM)的诊断与治疗难题提供了全新解决方案。
原文链接:
https://advanced.onlinelibrary.wiley.com/doi/abs/10.1002/adfm.202419395

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#免疫治疗# #胶质母细胞瘤#
9