首次复发的AML,立即移植还是再诱导后移植?
18小时前 聊聊血液 聊聊血液 发表于陕西省
《Haematologica》近日发表“PROS AND CONS EDITORIAL”文章,以辩论的形式讨论了AML首次复发后是否立即移植的问题。
首次复发AML
急性髓系白血病(AML)预后不佳,异基因造血干细胞移植是唯一治愈手段。但部分患者在首次组织学完全缓解时未进行异基因造血干细胞移植,对于这部分患者,首次复发后应该选择移植还是再诱导治疗后移植?目前尚有争议。《Haematologica》近日发表“PROS AND CONS EDITORIAL”文章,以辩论的形式讨论了AML首次复发后是否立即移植的问题。

正方
40多年前,Appelbaum等人于《Blood》发表文章, 建议对于在首次组织学完全缓解时未进行异基因造血干细胞移植的AML患者,复发后应尽快进行移植。该建议是基于几个考虑因素,包括移植前因试图达到第二次组织学完全缓解而导致的不良事件而失去移植资格。
后续在供者选择、移植前预处理方案、预防移植物抗宿主疾病(GvHD)和支持治疗方面取得了重要进展,提高了AML患者移植的安全性和有效性(包括缓解和未缓解患者)。来自国际血液和骨髓移植研究中心(CIBMTR)的大型回顾性分析和观察性数据报告,第二次组织学完全缓解时接受移植的结局优于未缓解时接受移植,但这些数据并未说明移植前强化再诱导化疗是否能提高复发患者的生存率,也未考虑到接受再诱导治疗但因各种原因(如毒性妨碍移植、撤回同意和死亡)而未进行移植的患者,也未区分未经治疗的首次复发患者与再诱导失败后接受移植的患者或从未实现首次组织学完全缓解的患者;此外许多研究关注的是结果的点估计值,而未报告置信区间,而后者通常较大。
尽管有这些考虑,大多数移植中心要求在进行移植前达到第二次组织学完全缓解或可测量残留病(MRD)阴性状态,而未经治疗的首次复发期进行移植很少被考虑或提及。因此大多数在复发时移植的患者为再诱导失败,越来越多的患者在第二次完全缓解期移植。比较这些队列的结果显然忽略了强烈的选择偏差。
有几个因素可能解释这种做法,并影响目前的专家建议和临床实践指南。作者曾报告过对共识指南的看法。如果移植后长期生存的可能性较低,即使预后比其他选择更好,医生和/或患者也可能选择不冒险面对移植的毒性和潜在死亡。其他医生可能使用再诱导疗法来评估疾病敏感性和移植治愈的可能性。许多患者在再诱导治疗失败后接受了移植,表明无论如何都可能进行移植。值得注意的是,再诱导治疗和移植的毒性是累积的,甚至是协同的。中心特定结果的公开报告也会影响医生选择哪些患者具有最佳的预估移植结局。有人认为移植最佳候选者会带来更好的结局,但这种看法忽略了用于预测预期结局的多因素分析的结果,这些分析可以解释已知的不两风险协变量。然而多因素分析可能忽略与患者和移植相关的协变量(如衰弱、社会经济地位和MRD),这些问题可能导致移植前需要再诱导治疗的错误结论和建议。
最近发表的III期ETAL-3-ASAP试验研究了移植前再诱导治疗对移植结果的影响,证实再诱导队列没有获益,且住院时间更长,不良事件更多,详见【柳叶刀血液病学】诱导治疗后移植对比立即异基因移植治疗复发性或缓解不佳AML的3期研究。
作者回顾的大多数数据支持在复发后尽快进行移植,而不要尝试移植前再诱导治疗。可能确定患者在再诱导治疗后可能达到组织学完全缓解的共变量(如首次缓解持续时间长、低危细胞遗传学、低ECOG体能评分和低血原始粒细胞浓度),无法帮助确定哪些患者可能从复发后治疗中受益,因为它们也可确定复发时移植可能有良好结局的患者。对移植前再诱导治疗的反应可识别出对疾病反应更强的患者,因此可作为预测性协变量或更好移植结局的生物标志物;但这最好看作是一种联系,而非因果关系。
对于首次完全缓解AML患者的复发,作者并不建议都直接进行移植,必须在个人的基础上做出决策。对于首次组织学完全缓解较短或具有其他不良风险共变量的患者,以及具有重要合并症的老年人,决策通常较为复杂。然而对许多人患者说,不进行进一步治疗就进行移植是合理的。此外任何决定都应该考虑拟进行的移植预处理方案。
总之,作者建议,目前对所有复发性AML患者进行移植前再诱导治疗的做法缺乏强有力的科学依据,可能弊大于利。其他学者也有类似结论(Leukemia. 2024;38(8):1663-1666)。
反方
改编一下托尔斯泰的《安娜·卡列尼娜》(Anna Karenina)的开场白“Happy families are all alike; every unhappy family is unhappy in its own way”( 幸福的家庭都是相似的,不幸的家庭各有各的不幸):“AML患者获得持久缓解的情况都是一样的;但每个复发/难治性患者都有自己独特的进展方式”。在过去,考虑到预后极差和治疗选择有限,临床试验设计主要集中在复发或难治性疾病上,几乎没有空间考虑分子谱异质性、复发时间、首次缓解前的治疗强度和类型。对于未在缓解期移植的复发或难治性患者,30年前的历史生存数据极差,只有25%的总生存率;这些结果导致了长期坚持的标准治疗,即在移植前尝试实现第二次缓解或最大反应。
德国ETAL-3-ASAP随机研究对这种范式提出挑战,患者随机分配接受再诱导(挽救)化疗(基于大剂量阿糖胞苷)序贯个性化预处理方案vs立即移植,后者使用FLAMSA-RIC序贯方案,包括强化疗(包括阿糖胞苷)和减低强度预处理。虽然立即移植未达到非劣效性,但两组几乎相同的结局为采用立即移植方法留下了空间。
正方将立即移植作为一种新标准,但他们也认识到目前的实践并非基于证据的大型前瞻性随机研究,而是基于可靠的科学原理和大量观察性和回顾性数据。该实践可能存在风险,尤其是增加移植毒性,特别是如果没有取得显著缓解(ASAP试验的数据似乎并未排除这种风险)。此外,两组实际移植的高比率(疾病对照组96%,缓解诱导组93%)在意向治疗试验中是相当罕见的,表明患者选择方面有一定问题,要么选择有立即可用供者的患者(这不太可能,因为只有15%的患者有相合同胞供者),要么选择惰性疾病生物学从而可以等待移植。ASAP试验报告的数据反映了最近移植技术的进步和后续方案的发展。此外,对于复发的AML患者,目前的治疗选择并非二选一(单独强化疗或立即移植)。在ASAP试验中使用的强化挽救治疗——米托蒽醌和阿糖胞苷(HAM),已经使用了30多年。令人失望的是,在采用HAM方案后,报告的缓解率仅从上世纪90年代的44-53%略微增加到目前的51-58%。
不能忽视移植前达到MRD阴性的重要性,这在多个研究和共识报告中都有报道。而ASAP试验中使用的FLAMSA-RIC方案包括在减低强度预处理之前进行缓解诱导化疗(小剂量阿糖胞苷或单剂量米托蒽醌10mg/m²),因此很可能在大量患者中也达到了MRD的目标(尽管未记录)。在类似的治疗方案中,移植后复发率的降低与诱导后外周细胞清除有关。
对于诱导失败或复发性AML,必须提出更个性化的治疗。20年前,Sing和Lipton建议,在特定患者中,基于fitness(年轻,无合并症)和预后因素(如早期复发和细胞遗传学),可以给予复发患者移植,即使没有缓解。该建议背后的基本原理在于,通过给予更有可能在移植后存活的患者立即移植,将移植相关死亡风险降到最低。在过去的25年里,移植方案和预后也有了显著的改善。ASAP的方案设计是基于对大多数患者可接受移植的信心,因此用于挽救化疗。即使再诱导失败也可以考虑移植,并且这类患者中有很大一部分最终在活动性白血病的情况下移植。立即移植使用序贯(FLAM-SA样)方案,包括强化诱导,与低治疗相关死亡率相关。
移植如今应视为大多数复发或难治性患者的目标,但也不能否认,在疾病负荷最小的情况下移植的预后更好。事实上在ASAP研究的诱导治疗组,移植前获得缓解的患者的预后明显好于诱导失败的患者(图1)。
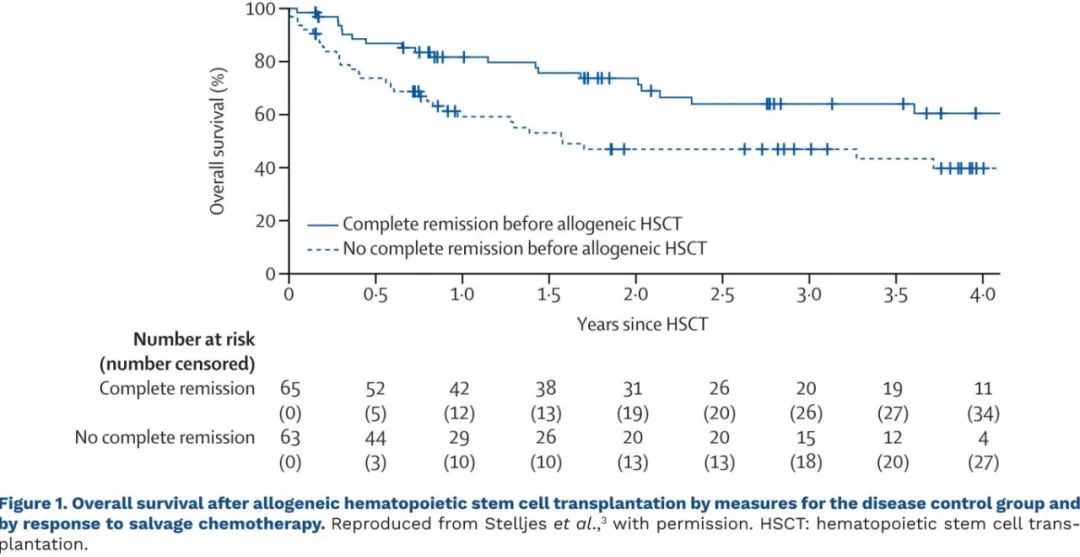
作为较为实际的建议,似乎不应该选择统一的立即移植方案,而应该努力寻找更好的诱导方案,从而在移植前获得更高的深度反应率,并实现部分患者无需移植。再诱导治疗的反应对预后和治疗至关重要,有助于确定哪些患者应该继续移植,哪些可能不需要移植,哪些患者移植可能无效(图2)。
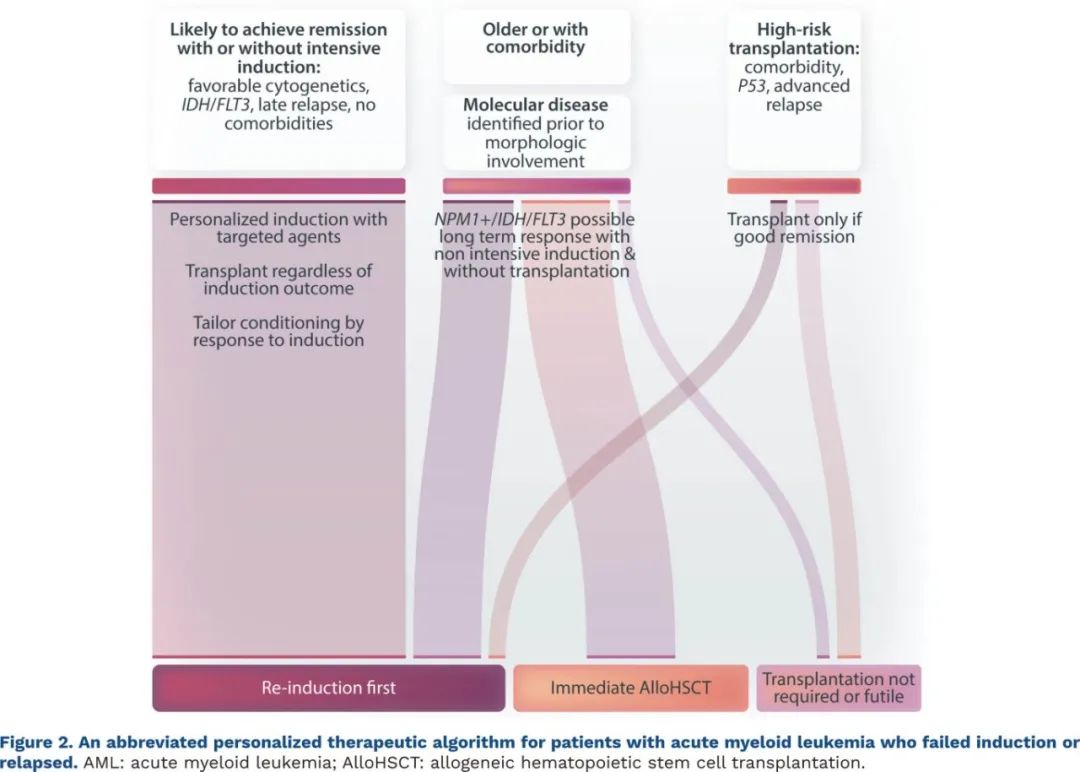
通过一线诱导可以在移植前获得MRD状态,并为可能从中受益的患者提供清髓性预处理。与正方提出的立即移植作为新的标准治疗策略以及Sing和Lipton强调最小化移植相关死亡率不同,重点应该是相反的:为强化挽救治疗不太可能获得高质量反应的患者保留立即移植。
最近的研究表明,在强化挽救治疗中加入维奈克拉可以显著提高完全缓解率。如果将诱导作为成功移植的潜在有益步骤,则可以选择最佳诱导方案。结合维奈克拉或任何相关的靶向药物,可能会增加在最佳条件下接受移植的患者比例。例如,一方面,应该鼓励对FLAG-Ida方案非常有反应的患者(例如晚期复发、健康和年轻的细胞遗传学低危患者)接受这种强化再诱导方案,而另一方面,可能无法忍受非常强化的挽救治疗或长期中性粒细胞减少的患者可能确实是立即移植的候选者。
立即移植与晚期移植的问题涉及到有疾病形态学证据的患者,然而分子学复发的患者还存在额外的考虑因素。关于NPM1阳性患者的分子学复发的治疗,可靠数据显示,非强化治疗方案(甚至不进行移植)都有很好的效果。
虽然前瞻性随机研究至关重要,但考虑到符合条件的患者较少而很难开展这些研究,即立即获得供者的患者,通常为相合同胞供者。在缺乏明确的前瞻性研究的情况下,目前在移植前用化疗治疗复发患者的做法(除了明显的例外情况)仍是合理的标准策略,其基于健全的理论基础,并得到大量回顾性研究的支持。
参考文献
1. Copelan E, Gale RP. Hematopoietic cell transplantation soon after first relapse in acute myeloid leukemia – the PROS. Haematologica 2025;110(1):4-6; https://doi.org/10.3324/haematol.2024.285784.
2. Ofran Y, Rowe JM. Hematopoietic cell transplantation soon after first relapse in acute myeloid leukemia – the CONS. Haematologica 2025;110(1):7-10; https://doi.org/10.3324/haematol.2024.286780.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#AML# #急性髓系白血病#
4