Nat Cancer | 靶向 ZMYND8 抑制前列腺癌神经内分泌转分化,破解耐药难题
2025-03-20 MedSci原创 MedSci原创 发表于陕西省
部分患者在接受去势治疗后会出现神经内分泌前列腺癌的转分化现象,其具有侵袭性且预后极差。该研究揭示了ZMYND8在NEPC发展中的关键作用,开发了小分子抑制剂iZMYND8-34,破解了前列腺癌耐药难题
前列腺癌(Prostate Cancer, PCa)是全球男性中最常见的恶性肿瘤之一,去势治疗(Androgen Deprivation Therapy, ADT)是其标准治疗手段。然而,部分患者在接受 ADT 后会出现神经内分泌前列腺癌(NEPC)的转分化现象,这是一种更具侵袭性且预后极差的亚型。
近期,Nature Cancer杂志发表了一项突破性研究,揭示了锌指 MYND 型结构域蛋白 8(ZMYND8)在 NEPC 发展中的关键作用,并开发了小分子抑制剂 iZMYND8-34,为破解前列腺癌耐药难题提供了新思路。题目为“Targeting the histone reader ZMYND8 inhibits antiandrogen-induced neuroendocrine tumor transdifferentiation of prostate cancer”。

研究者通过 CRISPR-Cas9 筛选技术,结合单细胞 RNA 测序(scRNA-seq),追踪肿瘤细胞在 ADT 诱导下的转分化过程。他们构建了一个针对 NEPC 相关基因的 sgRNA 文库,并将其导入 Pten/Trp53/Rb1 三敲除(TKO)小鼠前列腺类器官中。通过比较 NEPC 细胞与非 NEPC 细胞的基因表达差异,研究者发现 ZMYND8 在 NEPC 细胞中显著高表达,并且其缺失显著抑制了 NEPC 的发展。这表明 ZMYND8 是 NEPC 发展的关键调控因子。
研究者分析了 ZMYND8 在多种前列腺癌细胞系中的表达水平,发现其在 NEPC 细胞系(如 NE1.3 和 144-13)中表达最高,而在腺癌细胞系(如 LNCaP 和 LAPC4)中表达较低。通过对前列腺癌患者样本的免疫组化(IHC)分析,研究者发现 ZMYND8 在 NEPC 样本中的表达显著高于 CRPC-腺癌和激素敏感性前列腺癌(HSPC)样本。此外,ZMYND8 的高表达与患者的不良预后密切相关,其表达水平与神经内分泌标志物(如 SYP、NCAM1 和 NSE)呈正相关,而与 AR 下游靶基因(如 PSA 和 NKX3.1)呈负相关。这些结果表明,ZMYND8 的高表达是 NEPC 发展的一个重要标志。
研究者进一步探讨了 ZMYND8 的调控机制,发现 achaete-scute 同源物 1(ASCL1)能够显著上调 ZMYND8 的表达。ASCL1 是一种已知的神经内分泌标志物,其在 NEPC 发展中发挥重要作用。通过染色质免疫沉淀(ChIP)和荧光素酶报告基因实验,研究者证实了 ASCL1 能够直接结合到 ZMYND8 基因启动子区域,激活其转录。这表明 ASCL1 通过上调 ZMYND8 的表达,促进了前列腺癌细胞向 NEPC 的转分化。
研究者发现,ZMYND8 与叉头盒蛋白 M1(FOXM1)之间存在直接的相互作用,并且这种相互作用对于 NEPC 的发展至关重要。FOXM1 是一种转录因子,参与细胞周期调控和肿瘤进展。通过免疫共沉淀(co-IP)和体外结合实验,研究者证实了 ZMYND8 与 FOXM1 之间的直接相互作用,并且这种相互作用依赖于 ZMYND8 的 N 端结构域。此外,研究者还发现,FOXM1 能够稳定 ZMYND8 在 H3K4me1-H3K14ac 修饰的染色质区域的结合,从而促进 NEPC 相关基因的表达。这些结果表明,ZMYND8 与 FOXM1 协同作用,通过调控染色质重塑和基因表达,推动前列腺癌细胞向 NEPC 的转分化。
研究者进一步探讨了抗雄激素治疗如何影响 ZMYND8 和 FOXM1 的功能。他们发现,抗雄激素治疗(如恩杂鲁胺,ENZ)能够释放 SWI/SNF 染色质重塑复合物,使其从雄激素受体(AR)中解离出来,并促进其与 ZMYND8-FOXM1 复合物的结合。通过染色质免疫沉淀(ChIP)和基因组学分析,研究者发现,ENZ 治疗显著增强了 ZMYND8 和 FOXM1 在 NEPC 相关基因启动子区域的结合,从而激活了这些基因的表达。这表明,抗雄激素治疗通过改变染色质重塑复合物的分布,促进了 ZMYND8-FOXM1 复合物的形成,进而推动了前列腺癌细胞向 NEPC 的转分化。
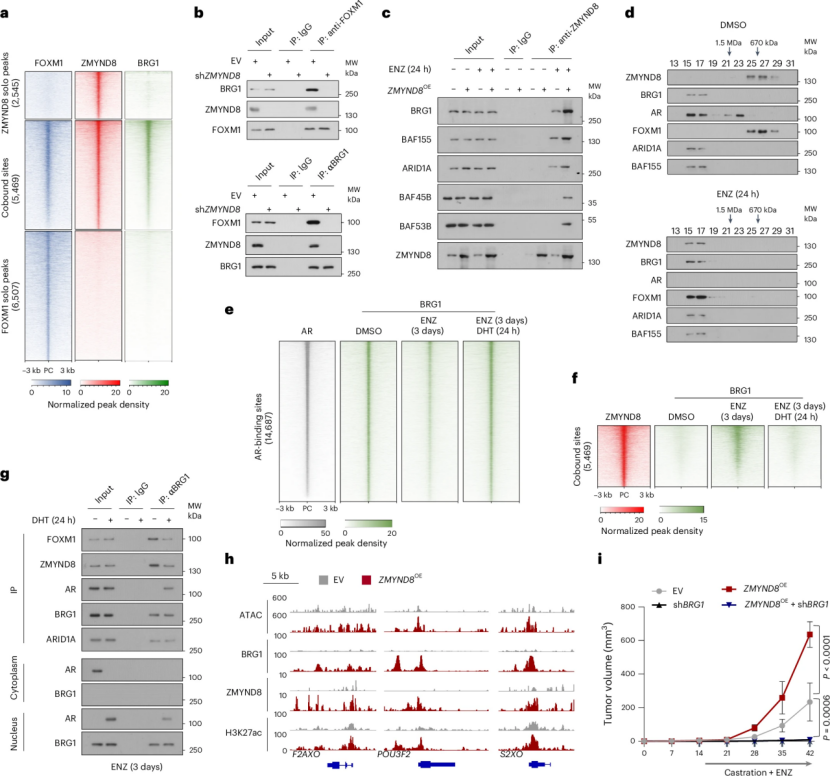
图ADT 通过释放 SWI/SNF 复合物触发 NEPC
基于 ZMYND8 在 NEPC 发展中的关键作用,研究者开发了一种小分子抑制剂 iZMYND8-34,用于靶向 ZMYND8 的组蛋白识别功能。通过虚拟筛选和分子对接实验,研究者从大量化合物中筛选出 iZMYND8-34,并通过一系列实验验证了其对 ZMYND8 的抑制效果。实验结果表明,iZMYND8-34 能够显著抑制 ZMYND8 与 H3K4me1-H3K14ac 修饰的组蛋白的结合,从而抑制 NEPC 相关基因的表达。在体外实验中,iZMYND8-34 显著抑制了 NEPC 细胞的增殖和神经内分泌标志物的表达。在体内实验中,iZMYND8-34 显著抑制了 NEPC 小鼠模型的肿瘤生长,延长了小鼠的生存时间。这些结果表明,iZMYND8-34 作为一种潜在的治疗药物,能够有效抑制 NEPC 的发展。
综上所述,本研究通过 CRISPR-Cas9 筛选和单细胞 RNA 测序技术,揭示了 ZMYND8 在前列腺癌去势抵抗性神经内分泌转分化中的关键作用,并发现了其与 FOXM1 的协同作用机制。研究还开发了一种小分子抑制剂 iZMYND8-34,能够有效抑制 ZMYND8 的功能,从而抑制 NEPC 的发展。这一发现不仅为理解前列腺癌的耐药机制提供了新的视角,也为开发新的治疗策略提供了潜在的靶点。
原始出处:
Targeting the histone reader ZMYND8 inhibits antiandrogen-induced neuroendocrine tumor transdifferentiation of prostate cancer. Nat Cancer. 2025 Mar 18. doi: 10.1038/s43018-025-00928-z. Epub ahead of print. PMID: 40102673.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#前列腺癌# #小分子抑制剂# #ZMYND8#
0