西米普利单抗单药治疗作为PD-L1表达≥50%的晚期非小细胞肺癌患者一线治疗的五年随访结果:EMPOWER-Lung 1研究
2025-03-23 daikun MedSci原创 发表于陕西省
该研究旨在报告EMPOWER-Lung 1研究的五年随访结果,研究结果显示,西米普利单抗单药治疗在PD-L1表达≥50%的晚期NSCLC患者中显示出持久的临床益处。
非小细胞肺癌(NSCLC)是全球范围内最常见的肺癌类型,约占所有肺癌病例的85%。尽管近年来在NSCLC的治疗方面取得了显著进展,但晚期NSCLC患者的预后仍然较差,尤其是那些无表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)或ROS1重排的患者。免疫检查点抑制剂(ICIs)的出现彻底改变了这类患者的治疗格局,特别是针对程序性细胞死亡蛋白-1(PD-1)及其配体程序性细胞死亡配体-1(PD-L1)的抑制剂。PD-1/PD-L1通路在肿瘤免疫逃逸中起关键作用,通过抑制这一通路可以增强机体对肿瘤细胞的免疫应答。西米普利单抗是一种全人源化的PD-1抑制剂,已被批准用于多种癌症的治疗,包括NSCLC。EMPOWER-Lung 1研究是一项多中心、开放标签、随机、全球性的III期临床试验,旨在评估西米普利单抗单药治疗与铂类双药化疗在PD-L1表达≥50%的晚期NSCLC患者中的疗效和安全性。EMPOWER-Lung 1研究之前的结果表明,西米普利单抗在无进展生存期(PFS)和总生存期(OS)方面优于化疗。然而,长期随访数据对于评估免疫治疗的持久疗效和安全性至关重要。本研究旨在报告EMPOWER-Lung 1研究的五年随访结果,以进一步了解西米普利单抗在晚期NSCLC患者中的长期疗效和安全性。

方法
EMPOWER-Lung 1研究是一项多中心、开放标签、随机、全球性的III期临床试验,旨在评估西米普利单抗单药治疗与研究者选择的铂类双药化疗在PD-L1表达≥50%的晚期NSCLC患者中的疗效和安全性。研究在全球24个国家的138个研究中心进行,共纳入712例患者,按1:1的比例随机分配至西米普利单抗组或化疗组。西米普利单抗组的给药方案为每三周一次静脉注射350 mg,持续两年或直至疾病进展。化疗组的患者接受研究者选择的铂类双药化疗,具体方案包括顺铂或卡铂联合紫杉醇(鳞状细胞组织学)或培美曲塞(非鳞状细胞组织学),随后可选择培美曲塞维持治疗。患者在疾病进展后可交叉至西米普利单抗治疗。研究的主要终点为OS和PFS,次要终点包括客观缓解率(ORR)、缓解持续时间(DOR)和安全性。
研究结果
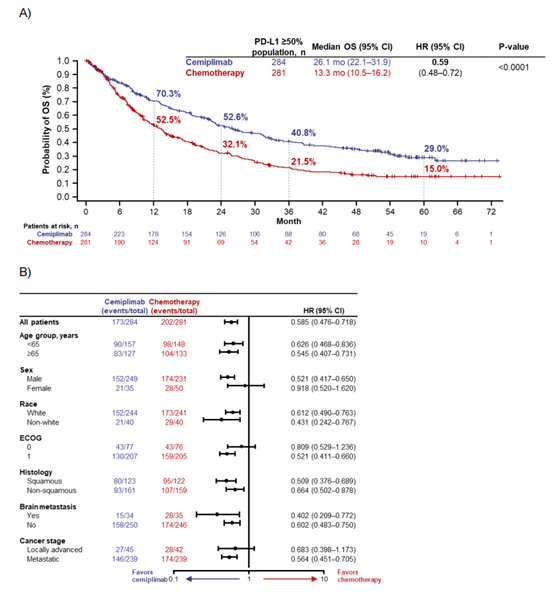
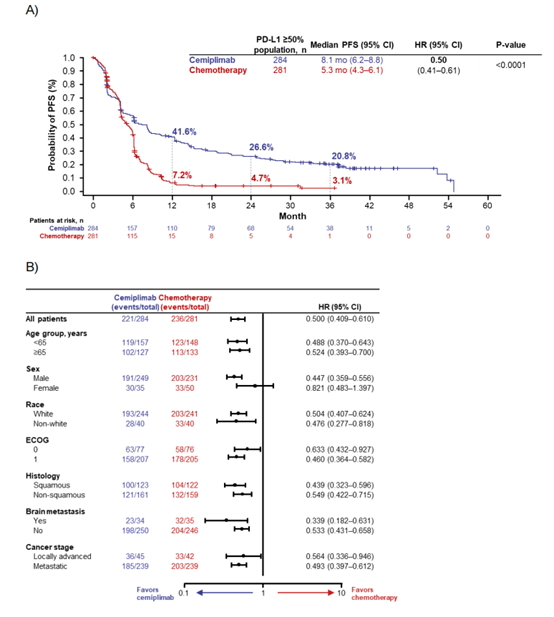
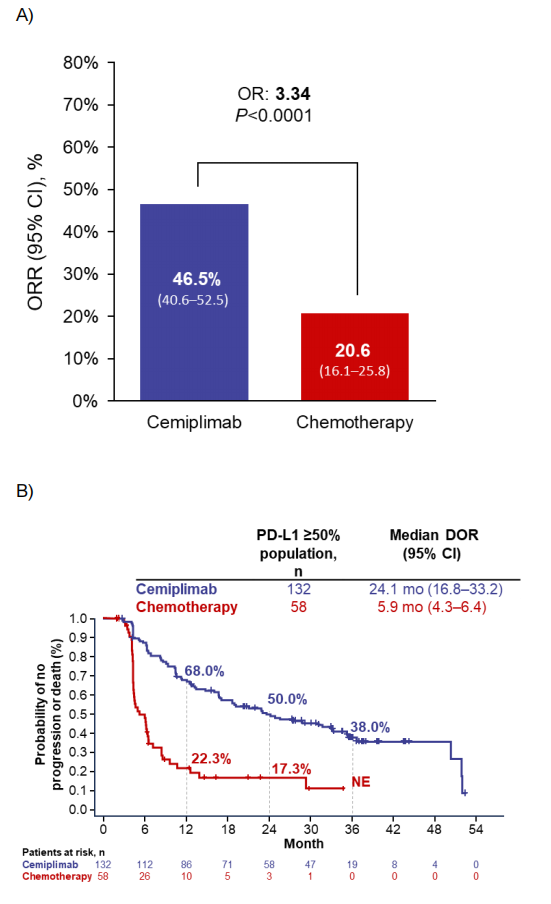
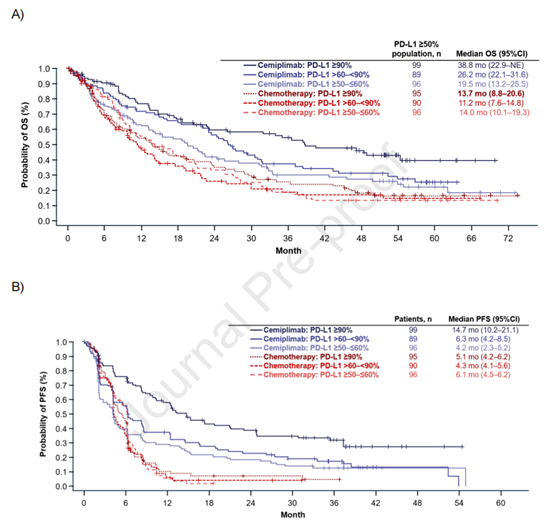
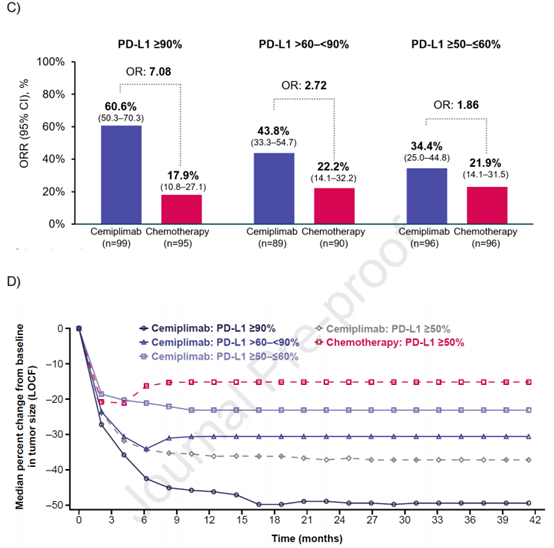
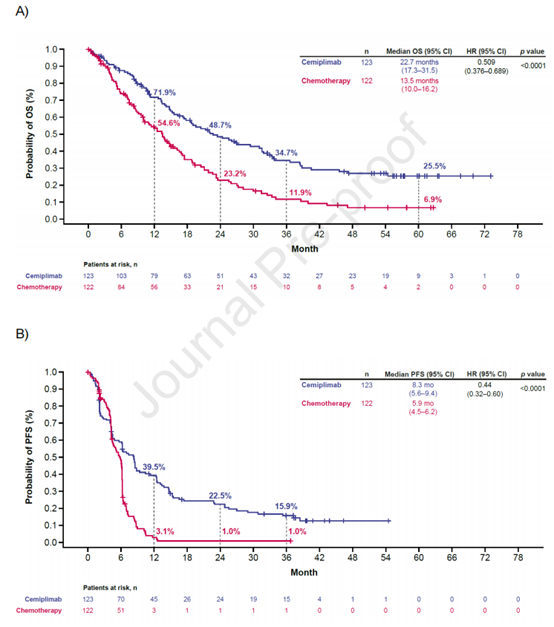
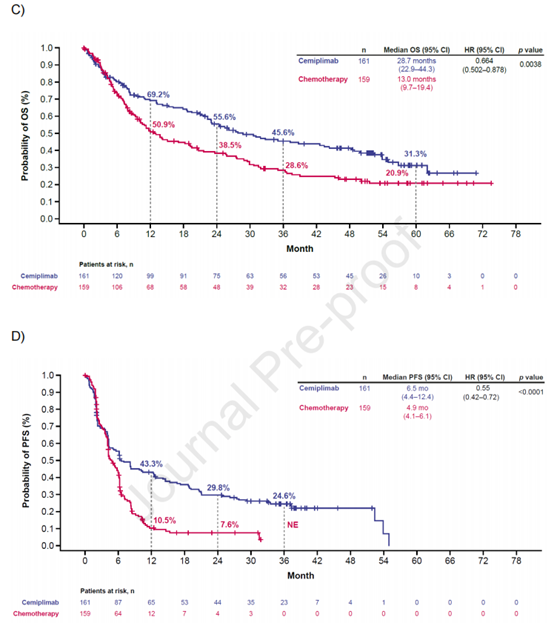
在PD-L1表达≥50%的患者中,西米普利单抗组的中位OS为26.1个月,而化疗组为13.3个月,风险比(HR)为0.59(95% CI: 0.48-0.72),p<0.0001。西米普利单抗组的五年OS概率为29.0%,而化疗组为15.0%。这些结果表明,西米普利单抗在长期随访中显示出显著的生存优势。在PFS方面,西米普利单抗组的中位PFS为8.1个月,而化疗组为5.3个月,HR为0.50(95% CI: 0.41-0.61),p<0.0001。ORR方面,西米普利单抗组为46.5%,而化疗组为20.6%,OR为3.34,p<0.0001。这些数据表明,西米普利单抗在缓解率和无进展生存期方面均优于化疗。此外,研究还发现西米普利单抗在不同PD-L1表达水平的患者中表现出不同的疗效。在PD-L1表达≥90%的患者中,西米普利单抗的中位OS为38.8个月,五年OS概率为39.8%,显示出最强的疗效。这表明PD-L1表达水平与西米普利单抗的疗效密切相关。在组织学亚组分析中,西米普利单抗在鳞状和非鳞状NSCLC患者中均显示出优于化疗的疗效。在鳞状NSCLC患者中,西米普利单抗的中位OS为22.7个月,而化疗组为13.5个月,HR为0.51(95% CI: 0.38-0.69)。在非鳞状NSCLC患者中,西米普利单抗的中位OS为28.7个月,而化疗组为13.0个月,HR为0.66(95% CI: 0.50-0.88)。
安全性分析
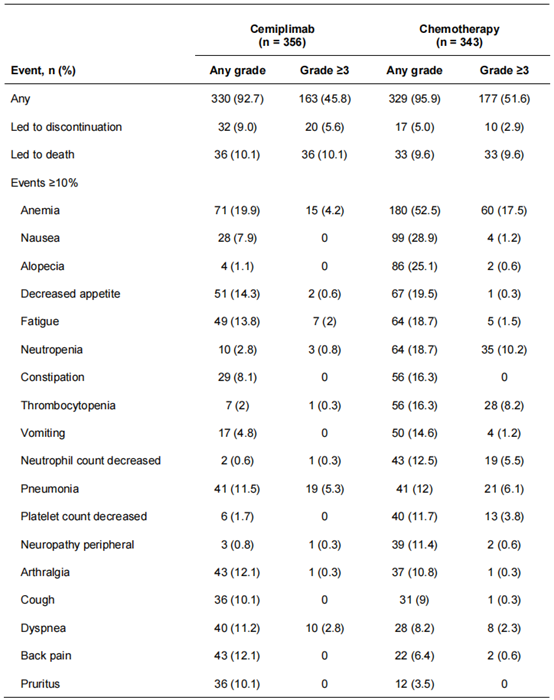
在安全性方面,西米普利单抗组和化疗组的不良事件(AEs)发生率分别为92.7%和95.9%,其中西米普利单抗组3级及以上AEs发生率为45.8%,而化疗组为51.6%。西米普利单抗组最常见的3级及以上AEs包括贫血(4.2%)、中性粒细胞减少(0.8%)和血小板减少(0.3%)。化疗组最常见的3级及以上AEs包括贫血(17.5%)、中性粒细胞减少(10.2%)和血小板减少(8.2%)。西米普利单抗组因AEs导致的治疗中断发生率为5.6%,而化疗组为2.9%。西米普利单抗组因AEs导致的死亡发生率为2.8%,化疗组为2.0%。西米普利单抗组报告了两例免疫相关死亡,分别为肾炎和自身免疫性心肌炎,这些结果与之前的三年随访结果一致。
结论
EMPOWER-Lung 1研究的五年随访结果显示,西米普利单抗单药治疗在PD-L1表达≥50%的晚期NSCLC患者中显示出持久的临床益处。与化疗相比,西米普利单抗在OS、PFS、ORR和缓解持续时间方面均表现出显著优势。此外,西米普利单抗在不同PD-L1表达水平和组织学亚组中的疗效一致,且随着PD-L1表达水平的增加,西米普利单抗的疗效也相应提高。安全性分析表明,西米普利单抗的安全性可接受,与之前的研究结果一致。尽管西米普利单抗组的AEs发生率略低于化疗组,但西米普利单抗组因AEs导致的治疗中断和死亡发生率较高,这可能与免疫相关AEs有关。总体而言,EMPOWER-Lung 1研究的五年随访结果进一步支持了西米普利单抗作为PD-L1表达≥50%的晚期NSCLC患者一线治疗的临床应用。未来需要进一步的研究来探索西米普利单抗与其他治疗策略的联合应用,以进一步提高患者的生存率和生活质量。
原始出处
Kilickap S, Baramidze A, Sezer A, et al. Cemiplimab Monotherapy for First-Line Treatment of Patients with Advanced NSCLC with PD-L1 Expression≥50%: 5-Year Outcomes of EMPOWER-Lung 1. Journal of Thoracic Oncology (2025), doi:https://doi.org/10.1016/j.jtho.2025.03.033.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#非小细胞肺癌# #西米普利单抗# #5年随访结果#
3