论文解读| Wenzhou Zhang/Xiaoman Li /Lufeng Zheng教授团队总结肿瘤微环境中的癌症干细胞
2024-10-29 Genes and Diseases Genes and Diseases 发表于上海
文章深入探讨了CSCs与TME之间复杂的相互作用,并讨论了针对这些相互作用的治疗潜力,为深入理解靶向癌症细胞干性以改善肿瘤治疗和预后提供了新的视角。
癌症干细胞(CSCs)或癌症干细胞样细胞(CSLCs)是具有干细胞特征的肿瘤细胞亚群,它们能够通过自我更新和无限制增殖来重建具有侵袭性等恶性生物学行为的肿瘤。CSCs的存在和活性依赖于一个复杂的肿瘤微环境(TME),其中包含多种细胞成分和非细胞成分,如免疫细胞、非免疫细胞、细胞因子、趋化因子和生长因子等。这些因素在信号传导中发挥关键作用,促进或维持CSCs的干性,并参与癌症的复发、转移和耐药性。
郑州大学附属肿瘤医院Wenzhou Zhang教授团队、中国药科大学的Xiaoman Li教授团队联合南京中医药大学的Lufeng Zheng教授团队在本刊发表了题为“Tumor microenvironment of cancer stem cells: Perspectives on cancer stem cell targeting”的综述。文章深入探讨了CSCs与TME之间复杂的相互作用,并讨论了针对这些相互作用的治疗潜力,为深入理解靶向癌症细胞干性以改善肿瘤治疗和预后提供了新的视角。
1、肿瘤微环境中的细胞成分
肿瘤微环境中的细胞成分,包括间充质干细胞、内皮细胞/内皮祖细胞、癌症相关成纤维细胞和肿瘤相关巨噬细胞,对CSCs的功能和形成具有重要影响。这些细胞通过分泌可溶性分子、细胞融合和细胞外囊泡与CSCs相互作用,支持CSCs的维持和发展(图1)。
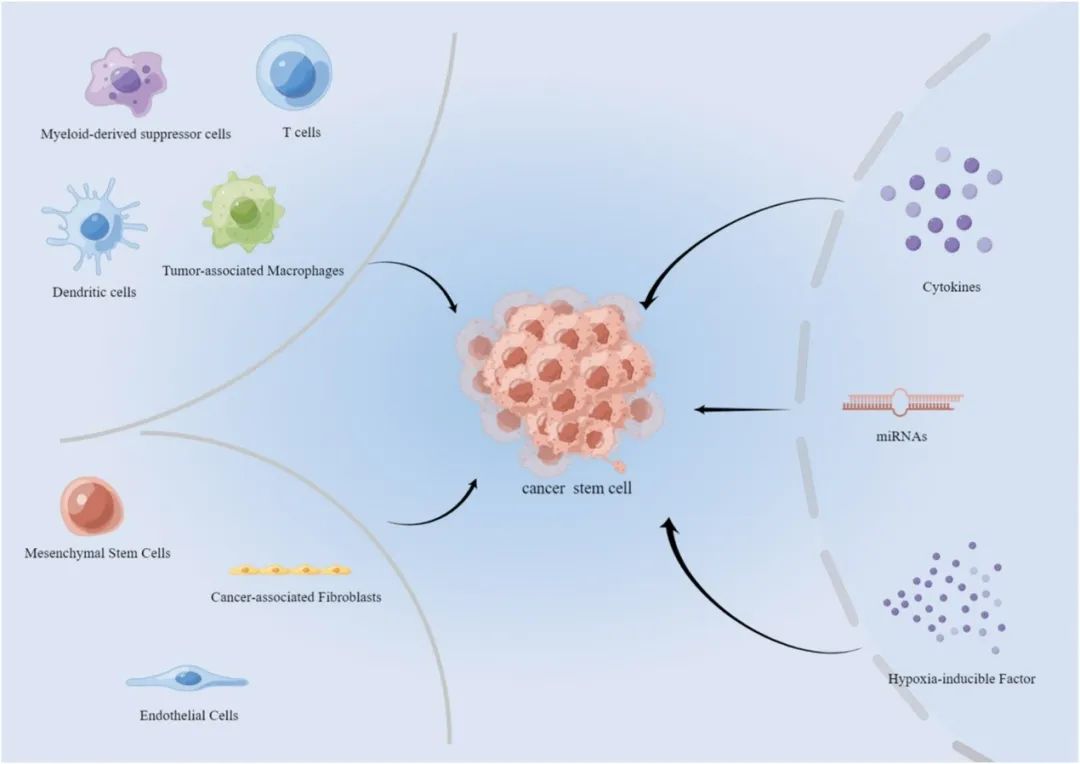
图1 CSCs 与 TME 三维网络之间的相互作用(原文中Figure 1)。
2、肿瘤微环境中的非细胞成分
CSCs通过其分泌的细胞因子,例如白细胞介素-6(IL-6)、IL-8、IL-17和IL-30,对肿瘤微环境(TME)进行精细调控,进而显著影响CSCs的自我更新与存活。此外, miRNA调控CSCs的自我更新、多能性、分化及肿瘤形成过程中扮演着至关重要的角色。因此,针对特定miRNA的策略性干预有望成为治疗癌症的高效手段。缺氧是TME的一个核心特征,它不仅是促进CSC表型和肿瘤发生的关键驱动力,而且通过调节与癌症进展相关的众多基因表达,缺氧环境及其诱导的缺氧诱导因子(HIFs)在促进和维持CSC特性方面发挥着重要作用。
3、靶向CSCs的治疗策略
文章还讨论了多种靶向CSCs及其微环境的治疗策略,包括靶向CSCs特异性标志物、干扰CSCs与微环境的相互作用、以及利用免疫细胞清除CSCs。这些策略为提高癌症治疗效果和减少复发提供了新的治疗途径。
总之,肿瘤微环境在CSCs的形成和维持中起着重要作用。CSCs可以重塑TME,而TME中的多种细胞成分和介质成分可以促进或维持CSCs的干性。针对CSCs及其微环境的靶向治疗可能成为克服癌症复发和耐药性的关键策略。未来的研究需要进一步探索CSCs的分子机制和微环境的特性,以实现更精准的癌症治疗。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304223003240
引用这篇文章:
Tumor microenvironment of cancer stem cells: Perspectives on cancer stem cell targeting. Genes Dis. 2024;11(3):101043.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#癌症干细胞# #肿瘤微环境#
46