指南更新 | 非小细胞肺癌NCCN(2025.V1):晚期疾病基因检测内容调整!
2024-12-31 e路新干线 e路新干线 发表于陕西省
2024年12月20日,非小细胞肺癌(NSCLC)NCCN指南更新至2025.V1,此次药物治疗更新的主要内容是晚期或转移性疾病新增靶点。

2025.V1-2024.12.20
非小细胞肺癌
NCCN指南
2024年12月20日,非小细胞肺癌(NSCLC)NCCN指南更新至2025.V1,此次药物治疗更新的主要内容是晚期或转移性疾病新增靶点:NRG1基因融合,推荐药物为zenocutuzumab-zbco;FGFR变异,推荐药物为厄达替尼;HER2阳性IHC3+,推荐药物为德曲妥珠单抗。同时其他致癌驱动变异患者一线和/或后续治疗方案进行了新增、删除或调整。免疫治疗方面,与PD-1/PD-L1抑制剂获益较小相关的致癌驱动变异增加了RET和ROS1重排,度伐利尤单抗巩固治疗增加“无EGFR ex19del/L858R突变”的限定条件。详细更新内容如下:
01 更新内容
初始评估和临床分期路径
🔹临床分期修改:
-
ⅢA期(T4浸润扩散,N0-1;T3,N1;T4,N0-1)
-
分散的肺结节(ⅡB、ⅢA、Ⅳ期)
ⅢA期同侧非原发性肺叶(T4, N0-1);Ⅳ期(对侧肺)
-
ⅣA期,M1b和ⅣB期,M1c(也适用于NSCL-15)
-
ⅣB期(M1c)胸膜转移或播散性转移

晚期或转移性疾病治疗路径
🔹生物标志物检测修改:
-
腺癌、大细胞癌、NSCLC非特指型(NOS):分子检测,包括:EGFR突变(1类)、ALK(1类)、KRAS、ROS1、BRAF、NTRK1/2/3、METex14跳跃、RET(1类)、ERBB2(HER2)、NRG1、HER2(免疫组化[IHC])
-
鳞状细胞癌:考虑分子检测,包括:EGFR突变、ALK、KRAS、ROS1、BRAF、NTRK1/2/3、METex14跳跃、RET、ERBB2(HER2)、NRG1、HER2(免疫组化[IHC])
🔹脚注mm修改:通过活检和/或血浆检测对EGFR、KRAS、ALK、ROS1、BRAF、NTRK1/2/3、MET、RET、ERBB2(HER2)和NRG1进行完整的基因分型。同时或先后进行组织和血浆检测是可接受的。同时检测可以缩短检测结果的时间,在适当的临床情况下应予以考虑。一种方法的阴性结果(意味着无明确的驱动突变)提示应使用补充方法。如果发现了临床上可操作的标志物,则根据确定的标志物开始治疗是合理的。根据现有结果指导治疗,如果结果未知,则将这些患者视为无驱动癌基因
🔹脚注oo新增:建议在进展过程中的某个时间点进行HER2免疫组化检测。时机应与组织保存相平衡

检测结果
🔹新增:NRG1基因融合阳性
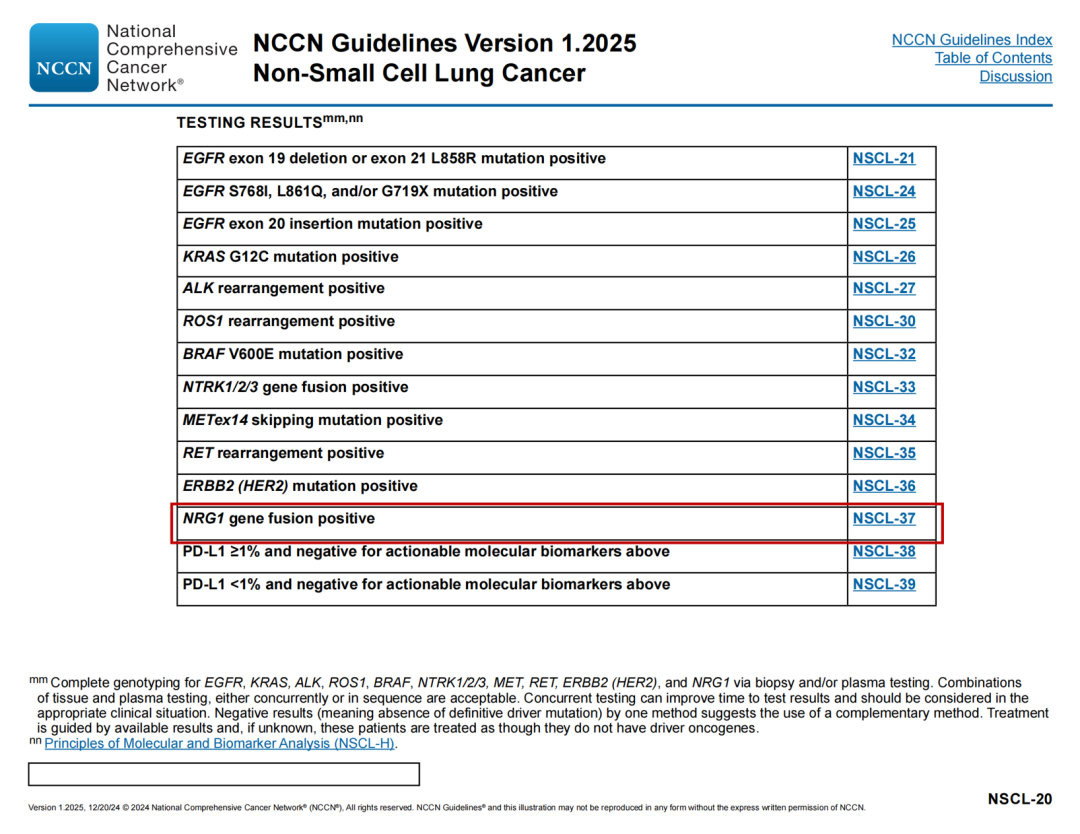
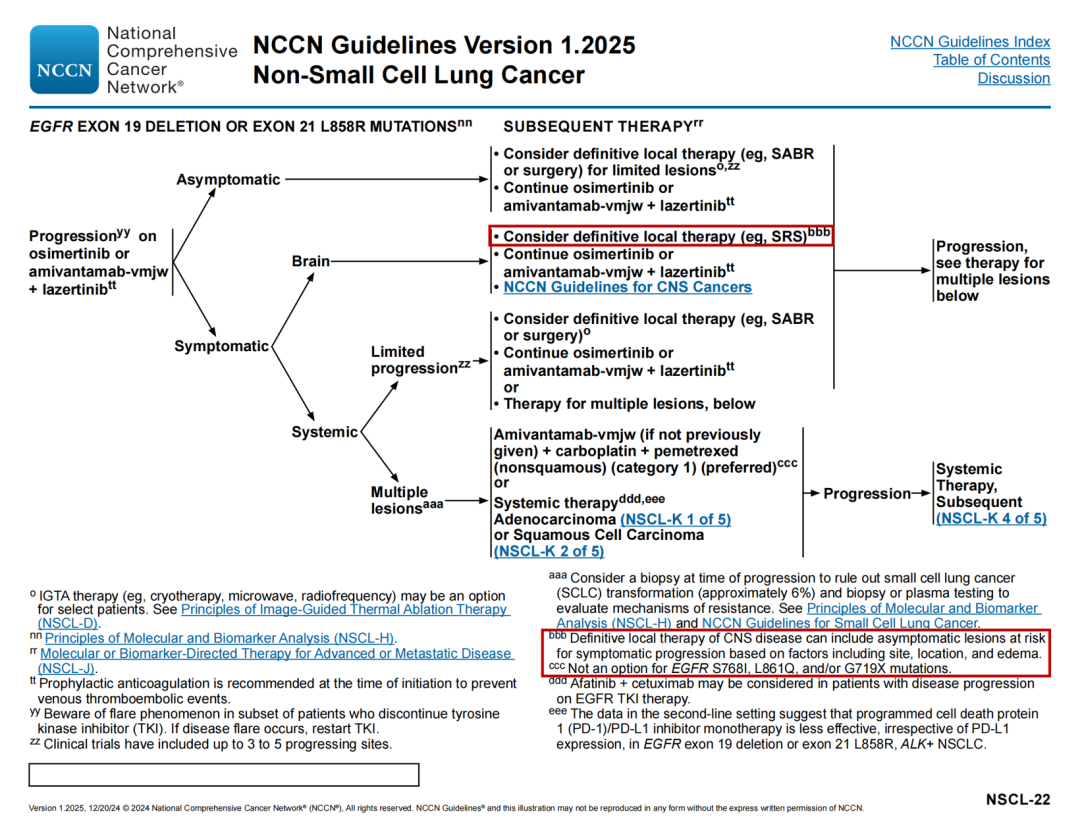
EGFR ex19del/L858R突变治疗路径
一线治疗
🔹在一线全身治疗中发现EGFR突变后续修改:完成计划的全身治疗,包括维持治疗在培美曲塞+(顺铂或卡铂)(非鳞状)的基础上加用奥希替尼或中断当前的治疗,并开始奥希替尼(首选)或埃万妥单抗+拉泽替尼或阿法替尼或达可替尼或厄洛替尼或厄洛替尼+贝伐珠单抗或厄洛替尼+雷莫西尤单抗或吉非替尼
🔹新增脚注xx:如果对当前治疗有良好应答,则继续治疗是合理的(也适用于NSCL-24、NSCL-27、NSCL-30、NSCL-33、NSCL-34、NSCL-35)

后续治疗
🔹奥希替尼或埃万妥单抗+拉泽替尼进展后,有症状,脑部后续修改:对于局限性病变,考虑根治性局部治疗(如SRS)(也适用于NSCL-23、NSCL-28、NSCL-29、NSCL-31)
🔹新增脚注bbb:CNS疾病的根治性局部治疗可包括根据部位、位置和水肿等因素表明有症状进展风险的无症状病灶(也适用于NSCL-23、NSCL-28、NSCL-29、NSCL-31)
🔹新增脚注ccc:不适用于EGFR S768I、L861Q和/或G719X突变
EGFR S768I、L861Q和/或G719X突变治疗路径
一线治疗
🔹在一线全身治疗中发现EGFR突变后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始阿法替尼(首选)或奥希替尼(首选)或达可替尼或厄洛替尼或吉非替尼

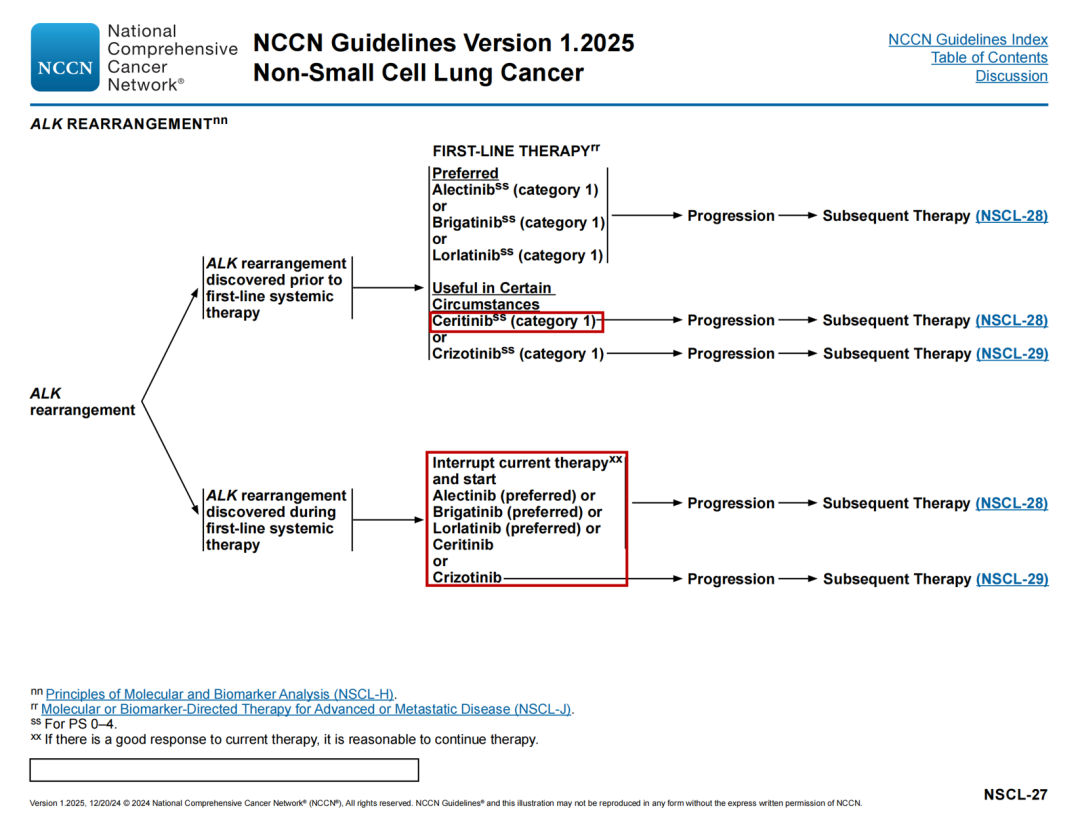
ALK重排治疗路径
一线治疗
🔹在一线全身治疗前发现ALK重排后续调整:塞瑞替尼(1类)从“其他推荐”移至“在某些情况下有用”
🔹在一线全身治疗中发现ALK重排后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始阿来替尼(首选)或布格替尼(首选)或洛拉替尼(首选)或塞瑞替尼或克唑替尼
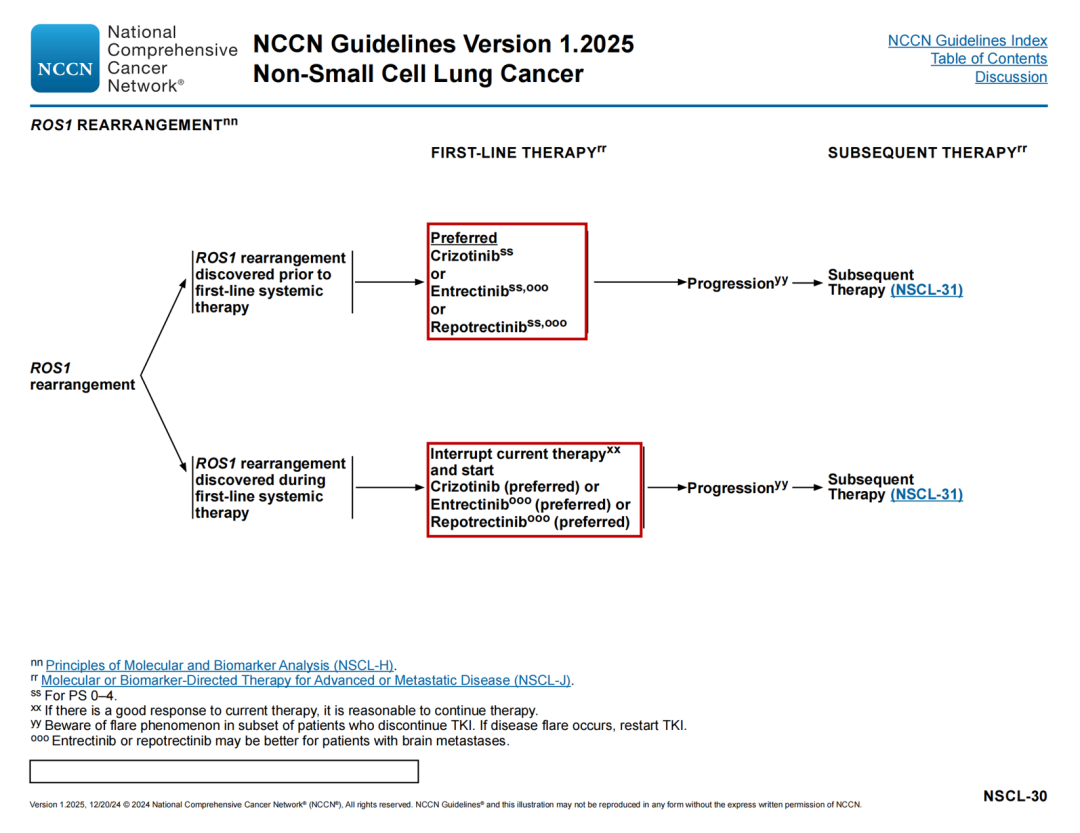
ROS1重排治疗路径
一线治疗
🔹在一线全身治疗前发现ROS1重排后续删除:塞瑞替尼(也适用于NSCL-J 1/6)
🔹在一线全身治疗中发现ROS1重排后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始克唑替尼(首选)或恩曲替尼(首选)或瑞普替尼(首选)或塞瑞替尼
后续治疗
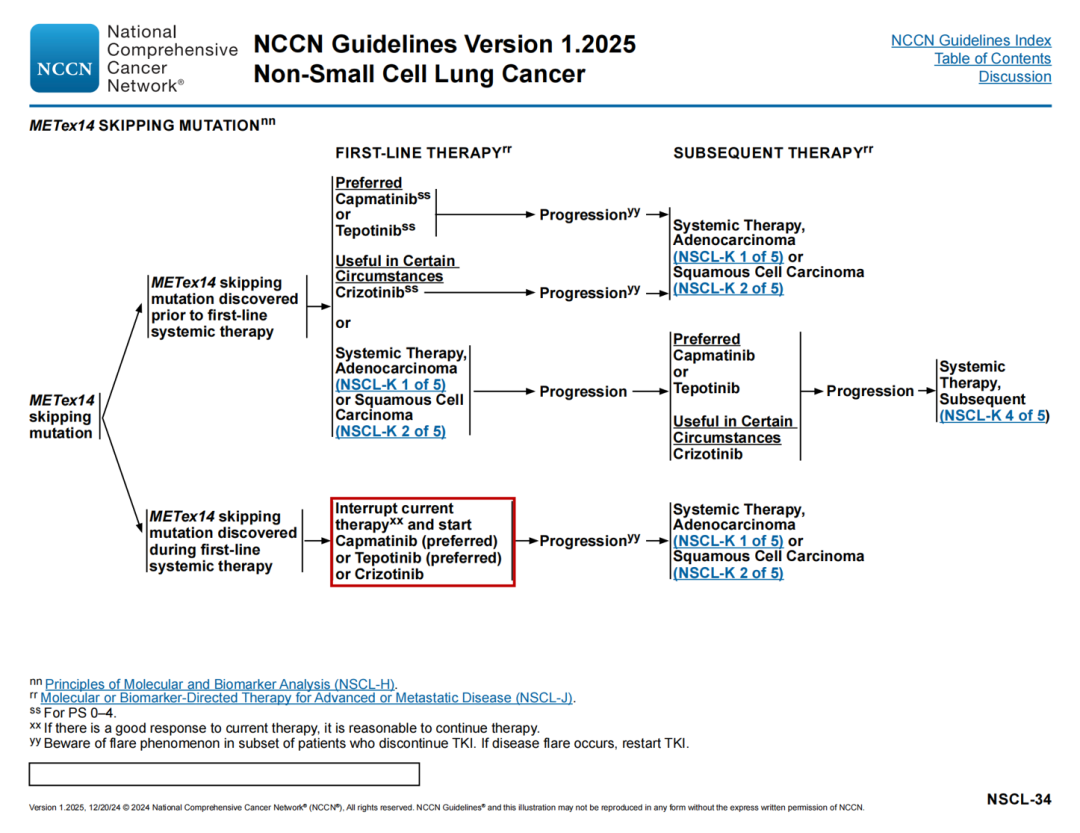
🔹克唑替尼、恩曲替尼或瑞普替尼进展后,有症状,脑部后续修改:瑞普替尼(如果之前接受过克唑替尼或塞瑞替尼或恩曲替尼治疗)或洛拉替尼(首选)或恩曲替尼(在某些情况下有用,如果之前接受过克唑替尼或塞瑞替尼治疗)或临床试验
🔹新增脚注ppp:瑞普替尼是耐药突变的一种选择,如ROS1 G2032R
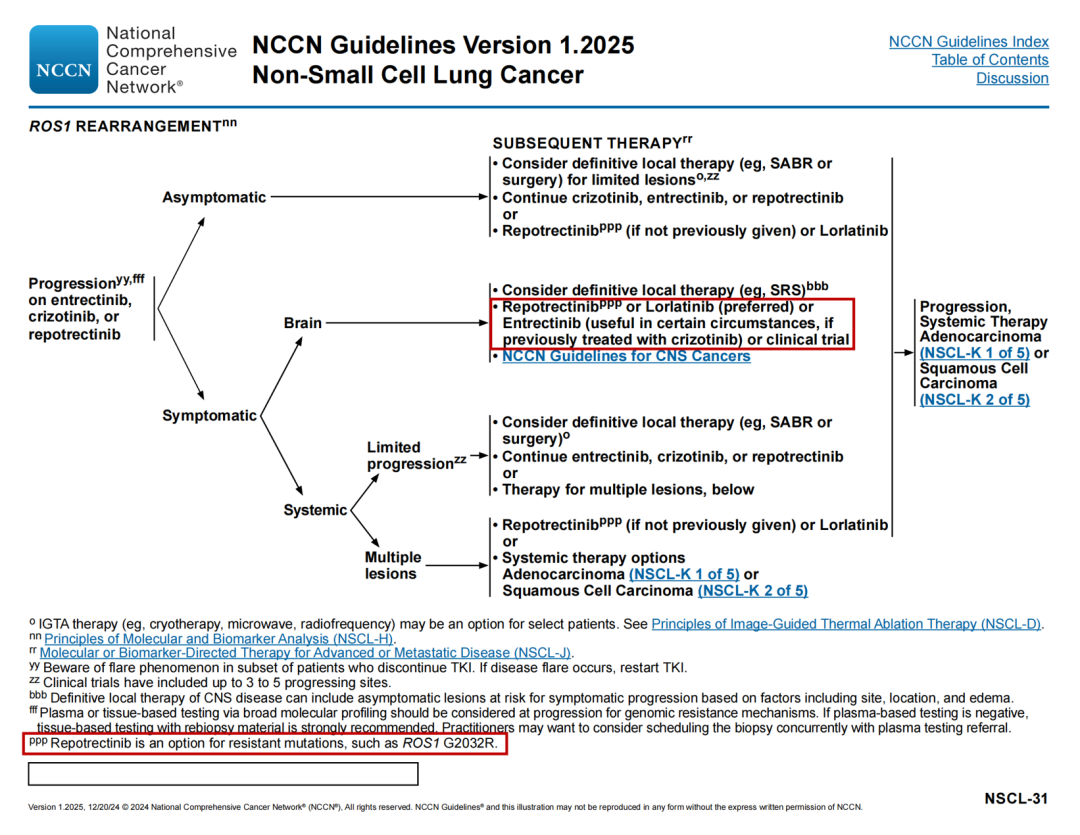
BRAF V600E突变治疗路径
一线治疗
🔹在一线全身治疗中发现BRAF V600E突变后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始达拉非尼+曲美替尼(首选)或康奈非尼+贝美替尼(首选)
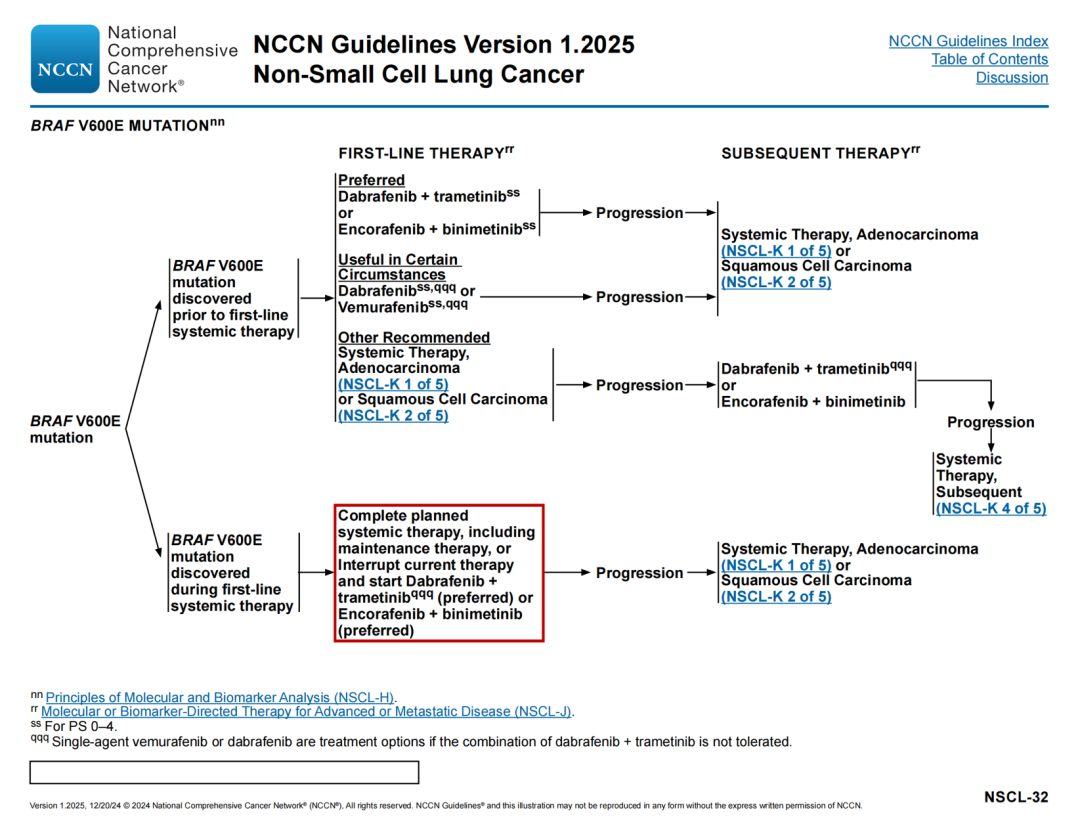
NTRK基因融合治疗路径
一线治疗
🔹在一线全身治疗中发现NTRK1/2/3基因融合后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始恩曲替尼或拉罗替尼或瑞普替尼
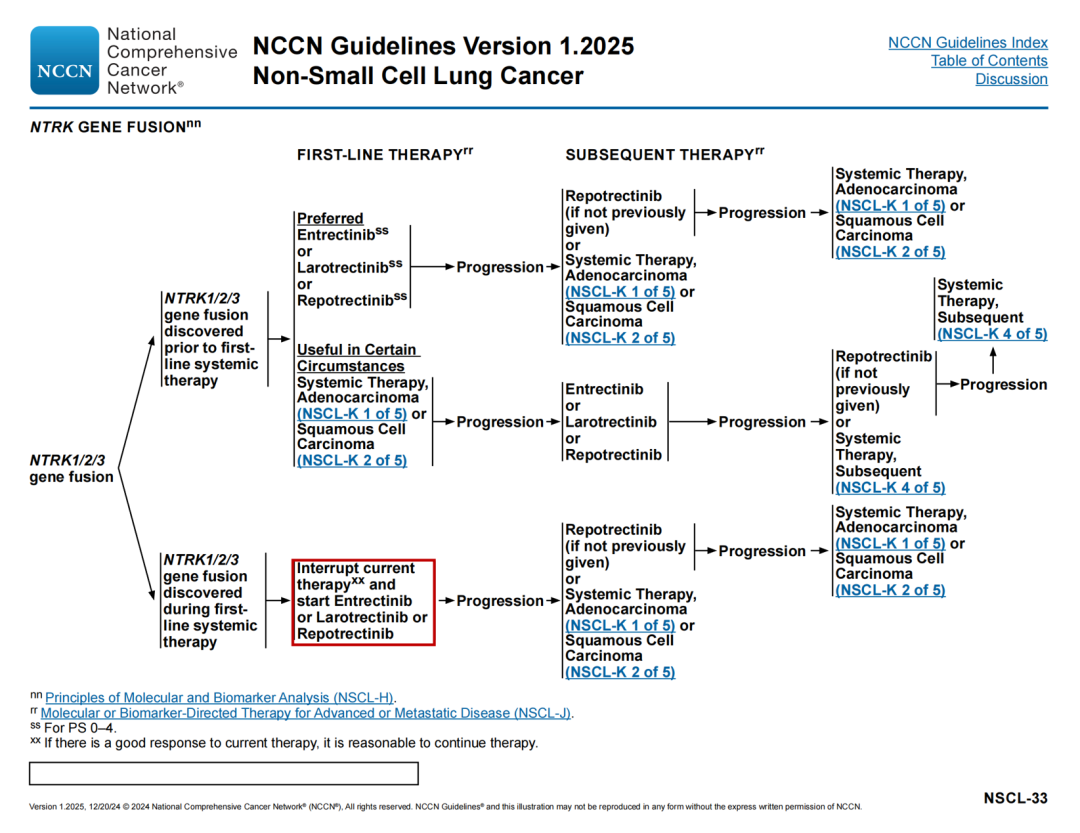
MET ex14跳跃突变治疗路径
一线治疗
🔹在一线全身治疗中发现MET ex14跳跃突变后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始卡马替尼(首选)或特泊替尼(首选)或克唑替尼
RET重排治疗路径
一线治疗
🔹在一线全身治疗前发现RET重排后续调整:首选方案塞普替尼从“2A类”推荐改为“1类”;删除:某些情况下有用:卡博替尼(也适用于NSCL-J 1/6)和其他推荐方案:全身治疗(NSCL-K)
🔹在一线全身治疗中发现RET重排后续修改:完成计划的全身治疗,包括维持治疗或中断当前的治疗,并开始普拉替尼(首选)或塞普替尼(首选)或卡博替尼
后续治疗
🔹普拉替尼或塞普替尼进展后新增:卡博替尼
🔹卡博替尼进展后新增:全身治疗,腺癌(NSCL-K 1/5)或鳞状细胞癌(NSCL-K 2/5)
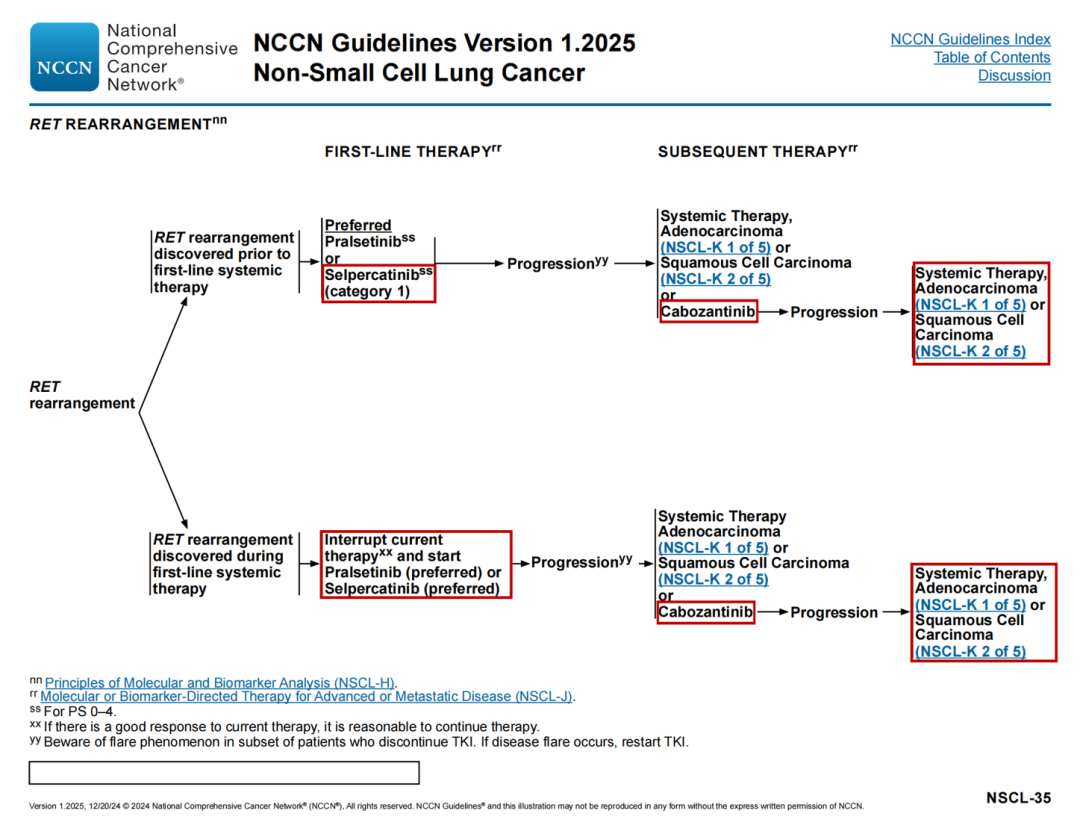
ERBB2(HER2)突变治疗路径
🔹新增脚注rrr:关于HER2蛋白过表达(IHC3+)的治疗方案,参见NSCL-K 4/5
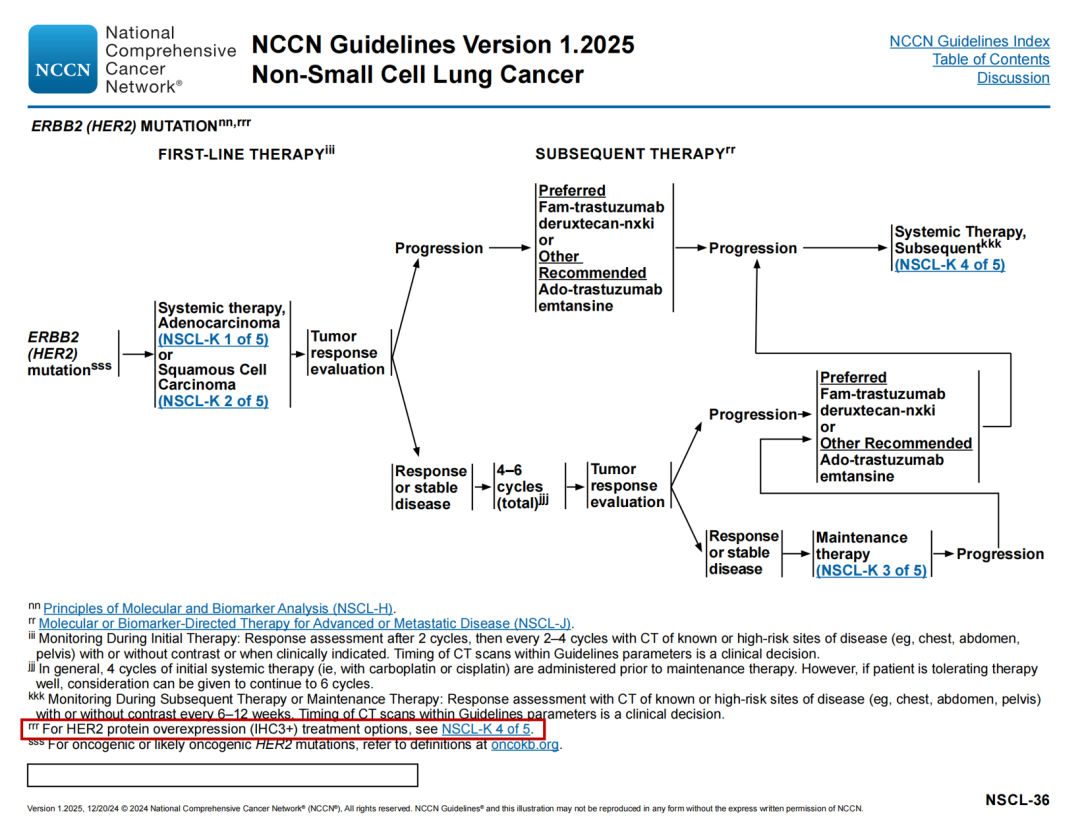
NRG1基因融合治疗路径
🔹本页新增
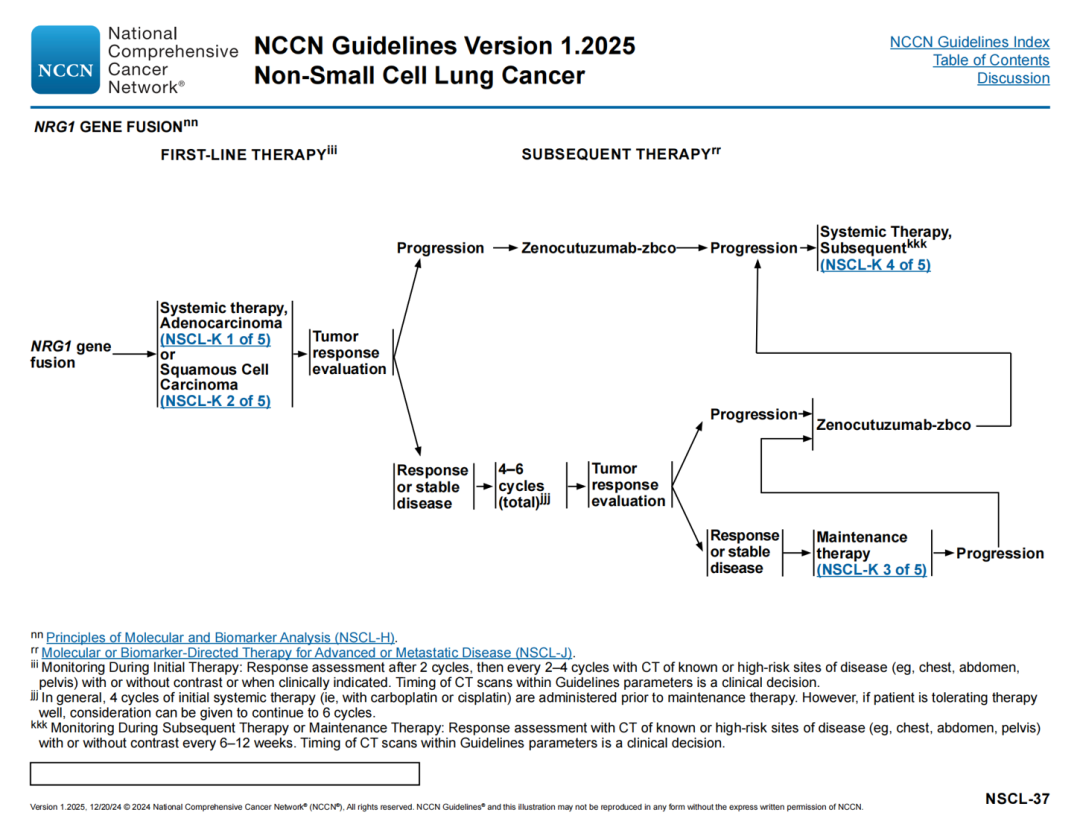
PD-L1阳性(≥1%)治疗路径
🔹移除体能状态,现体能状态按照NSCL-J和NSCL-K中描述(也适用于NSCL-39)
🔹脚注ttt修改:PD-1/PD-L1抑制剂治疗的禁忌症可能包括活动性或既往证实的自身免疫性疾病和/或目前使用免疫抑制剂;一些致癌驱动基因(如EGFR ex19del/L858R;ALK、RET或ROS1重排)已被证明与PD-1/PD-L1抑制剂获益较小相关(也适用于NSCL-E 1/6、 NSCL-E 2/6、NSCL-E 5/6的脚注a;NSCL-K 1/5、NSCL-K 2/5、NSCL-K 4/5的脚注d)。如有禁忌症,参见NSCL-K 1/5(腺癌)或NSCL-K 2/5(鳞状细胞癌)
🔹删除脚注:不论PD-L1状态如何,阿替利珠单抗单药治疗均是PS 3患者的可选治疗方案。阿替利珠单抗和hyaluronidase-tqjs皮下注射可能替代阿替利珠单抗静脉注射。与阿替利珠单抗静脉注射相比,阿替利珠单抗和hyaluronidase-tqjs皮下注射具有不同的剂量和给药说明(也适用于NSCL-39)
围手术期全身治疗
辅助化疗
🔹第一行修改:对于ⅠB期和ⅡA期(T2b,N0)和切缘阴性(R0)的高危患者,建议行辅助化疗
🔹第二行修改:对于ⅡB期(T1abc-T2a,N1)、ⅡB期(T3,N0;T2b,N1)、ⅢA期(T1-2,N2;T3,N1;T4,N0-1)、ⅢB期(T3-4、N2)和切缘阴性(R0),辅助化疗作为1类推荐
🔹新增第三行:以下列出的所有化疗方案均可用于序贯化疗/放疗
🔹第四行修改:检测PD-L1状态、EGFR突变和ALK重排(ⅡⅠB-ⅢA期、ⅢB期 [T3-4,N2])

手术切除后全身治疗
🔹第一行修改:检测PD-L1状态、EGFR突变和ALK重排(ⅠB-ⅢA期、ⅢB [T3-4,N2]期)
🔹新增第二行:肿瘤≥4 cm完全切除或淋巴结阳性的NSCLC患者应评估其他额外全身性治疗
🔹阿来替尼
-
修改:对于完全切除的Ⅱ-ⅢA期或ⅢB期(T3,N2)且ALK重排阳性的NSCLC患者(1类)
🔹 奥希替尼
-
修改:对于完全切除的ⅠB-ⅢA期或ⅢB期(T3,N2)且EGFR(EGFR ex19del/L858R)突变阳性的NSCLC患者,既往接受过辅助化疗或不适合接受铂类化疗(1类)
🔹阿替利珠单抗
-
修改:对于完全切除的ⅡB-ⅢA期、ⅢB期(T3,N2)或高危ⅡA期PD-L1 ≥1% NSCLC患者,且EGFR ex19del/L858R突变或ALK重排阴性,既往接受过辅助化疗且无免疫检查点抑制剂禁忌症(1类)
🔹帕博利珠单抗
-
修改:对于完全切除的ⅡB-ⅢA期、ⅢB期(T3,N2)或高危ⅡA期且EGFR ex19del/L858R或ALK重排阴性的NSCLC患者,既往接受辅助化疗且无免疫检查点抑制剂禁忌症,最长达1年(1类)。PD-L1 <1%患者的获益尚不清楚
-
修改:对于完全切除的Ⅱ-ⅢA期、ⅢB期(T3,N2)NSCLC患者,既往接受过新辅助帕博利珠单抗+化疗,最长达39周(1类)
🔹度伐利尤单抗
-
修改:对于肿瘤≥4 cm完全切除和/或淋巴结阳性NSCLC患者,既往接受新辅助度伐利尤单抗+化疗且无已知的EGFR突变或ALK重排(1类)
🔹纳武利尤单抗
-
修改:对于完全切除的Ⅱ-ⅢB期NSCLC患者,既往接受新辅助纳武利尤单抗+化疗且无已知的EGFR突变或ALK重排(1类)

同步放化疗方案
对于接受根治性同步放化疗后PS 0-1且无疾病进展的不可切除的Ⅱ/Ⅲ期NSCLC患者进行巩固治疗
🔹第一行修改:度伐利尤单抗10 mg/kg IV,每2周1次或1500 mg,每4周1次,最长达12个月(体重≥30 kg的患者)(Ⅲ期为1类;Ⅱ期为2A类)(EGFR ex19del/L858R突变阳性肿瘤除外)

分子和生物标志物分析原则
分子靶点分析
🔹新增HER2蛋白过表达:HER2由ERBB2编码,可在多种恶性肿瘤中过表达
-
HER2过表达定义为基于免疫组化,具有3+肿瘤细胞染色
-
目前,对于非小细胞肺癌中HER2染色的特异性免疫组化抗体克隆尚无建议
-
目前,抗HER2单克隆抗体/抗体药物偶联物(ADC)治疗的评分标准是基于最初应用于胃癌的标准,其使用的评分标准与用于乳腺癌的评分标准不同,对于小活检标本和切除标本,使用的评分标准也不同
🔹PD-L1修改:尽管PD-L1表达在有致癌驱动基因的患者中可能升高,但针对某些致癌驱动基因的靶向治疗应优先于使用免疫检查点抑制剂治疗

新增胚系检测
🔹如果在体细胞检测中怀疑发现胚系变异,则考虑转诊至遗传咨询

确定转移性NSCLC患者新疗法的新兴生物标志物
🔹基因变异新增:FGFR变异,可用的靶向药物为厄达替尼
🔹脚注a修改:高水平MET扩增的定义正在发展,可能根据用于测试的分析而有所不同。在NGS检测中,拷贝数大于≥10为高水平MET扩增
🔹新增脚注c:关于致癌或可能致癌的FGFR突变,参见oncokb.org上的定义

分子和生物标志物导向治疗晚期或转移性疾病
🔹EGFR S768I、L861Q和/或G719X,后续治疗删除:埃万妥单抗+卡铂+培美曲塞(非鳞状)
🔹新增NRG1基因融合,后续治疗:zenocutuzumab-zbco
🔹新增HER2阳性IHC3+,后续治疗:德曲妥珠单抗

晚期或转移性疾病的全身治疗
🔹将针对PS 2腺癌、大细胞癌、NSCLC NOS的推荐整合到PS 0-1的某些情况下有用的推荐中;现在所有的推荐均针对PS 0-2(也适用于NSCL-K 2/5)
🔹表格标题修改(也适用于NSCL-K 2/5):
-
无PD-1或PD-L1抑制剂禁忌症且无EGFR ex19del/L858R;ALK、RET或ROS1重排
-
具有PD-1或PD-L1抑制剂禁忌症或具有EGFR ex19del/L858R;ALK、RET或ROS1重排
🔹某些情况下有用调整:吉西他滨/多西他赛和吉西他滨/长春瑞滨从“1类”推荐改为“2A类”(也适用于NSCL-K 2/5)

晚期或转移性疾病的全身治疗——后续治疗 / 晚期或转移性疾病的全身治疗——进展后治疗
🔹修改:德曲妥珠单抗(HER2 IHC3+)

02 总结
各类靶点和对应治疗药物的出现改变了驱动基因异常晚期非小细胞肺癌治疗格局,靶向治疗前景巨大。本次指南更新,晚期疾病基因检测新增NRG1基因融合、FGFR变异和HER2阳性IHC3+靶点,丰富了驱动基因异常非小细胞肺癌患者靶向治疗选择。指南同时对其他驱动基因异常晚期患者的治疗推荐进行了调整和对免疫治疗的使用条件进行了更明确的说明,进一步促进非小细胞肺癌治疗迈向精准化、个体化。
参考文献:
1.NCCN指南:非小细胞肺癌(2025.V1).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#非小细胞肺癌##基因检测#
13
#非小细胞肺癌# #基因检测#
10