张小田教授深度解读:GEMSTONE-303研究如何重塑晚期胃癌一线治疗格局
2025-03-28 医悦汇 医悦汇 发表于陕西省
2025 年 3 月 23 日 CACA 前沿播会议上,北大肿瘤医院沈琳、张小田教授分享 GEMSTONE-303 研究,阐述舒格利单抗联合化疗一线治晚期胃癌的设计、成果,显著提升生存数据且安全性好。
编者按:2025年3月23日,中国抗癌协会主办的CACA前沿播第5期线上学术会议成功闭幕。北京大学肿瘤医院沈琳教授、张小田教授等分享了在JAMA发表的《舒格利单抗联合化疗一线治疗晚期胃癌(First-line Sugemalimab Plus Chemotherapy for Advanced Gastric Cancer)》研究。会议上,张小田教授从四个方面详细阐述了该研究的研究设计及成果。【医悦汇】特别整理,以供参考!
研究背景
GEMSTONE-303是一项随机、对照、双盲、多中心的Ⅲ期研究,其设计主要参考了GEMSTONE-101的Ⅰb期数据。在GEMSTONE-101中,针对CPS>5分的患者进行了富集,结果显示舒格利单抗联合奥沙利铂和卡培他滨化疗在晚期胃及胃食管结合部腺癌患者(N=29)中疗效良好且安全性可耐受,ORR为62.1%,中位PFS为8.3个月,中位OS为17.0个月,且亚组分析提示PD-L1表达CPS>5的患者效果更佳。鉴于以往胃癌临床研究多失败,该数据为研究团队带来信心。当时CheckMate-649结果未公布,团队只能参考KEYNOTE-062进行探索。因此,在GEMSTONE-303中,团队将关键入排标准设定为排除HER2阳性患者,以CPS>5分作为入选标准。这一理念不仅贯穿GEMSTONE-303研究,还在后续新辅助治疗中,以PD-L1 CPS评分>5分作为入组标准,持续应用于此类人群的管理。
研究设计
研究在疫情期间开展,精准筛选出不到500例样本,分为治疗组(舒格利单抗联合化疗)和对照组(安慰剂联合化疗)。随访期间,持续治疗直至疾病进展、毒性无法耐受、患者撤回知情同意或达到最长治疗时间。
研究基于CPS评分>5的患者,进行5~9分和>10分的分层,同时考虑ECOG评分0分和1分的分层因素。以无进展生存期(PFS)和总生存期(OS)作为双终点事件,综合考虑药物上市需求、一线和二线应用的临床研究终点以及这两个终点的重要性,匹配a值。
次要终点方面,对于CPS>5的患者,由盲态独立中心评审委员会评估PFS、ORR(客观缓解率)、DOR(缓解持续时间)以及12个月和24个月的总生存率;对于CPS>10分的患者,评估这些远近端点。
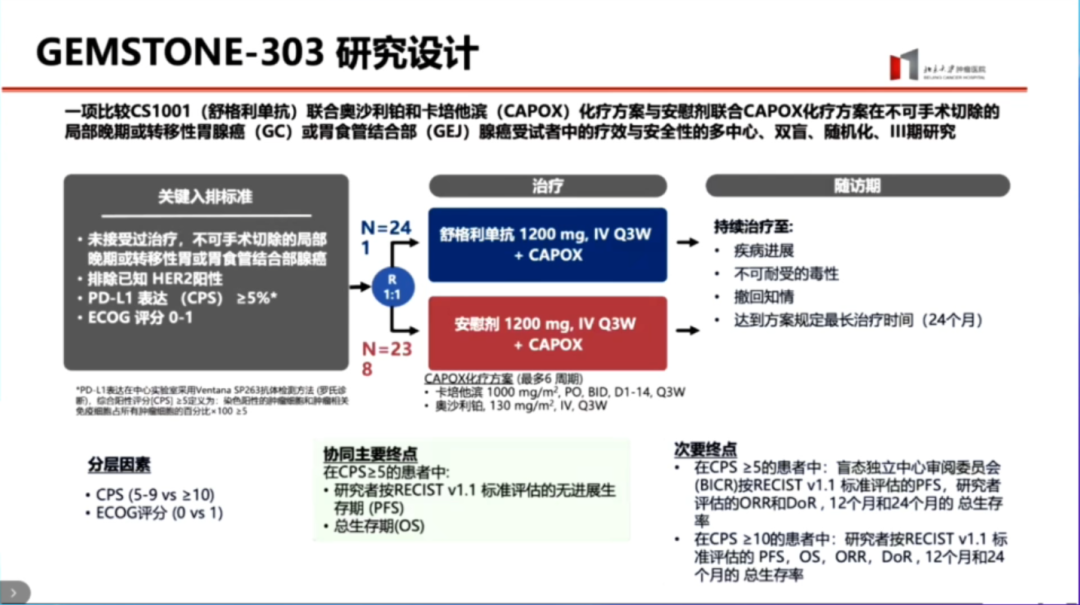
从统计学假设和样本量来看,本研究采用1:1对照,将两个协同终点PFS和OS的双侧显著性水平设定为0.05的α值,并分别分配0.01和0.04。若PFS结果显著,则将0.01的 α值传递给OS;若PFS不显著,则OS在0.04水平下检验。
本研究计划入组约480例患者,预期在发生约270例死亡事件时进行OS期中分析。PFS分析的P值边界为双侧α等于0.01,数据截止时间为2022年8月6日。经独立数据监测委员会(IDMS)审阅后,因PFS达到显著差异,OS结果也超过了P值边界。最终分析时间定在2023年7月9日,对OS进行最终分析,其P值边界为双侧α等于0.05,最终P值为0.0442。

研究结果
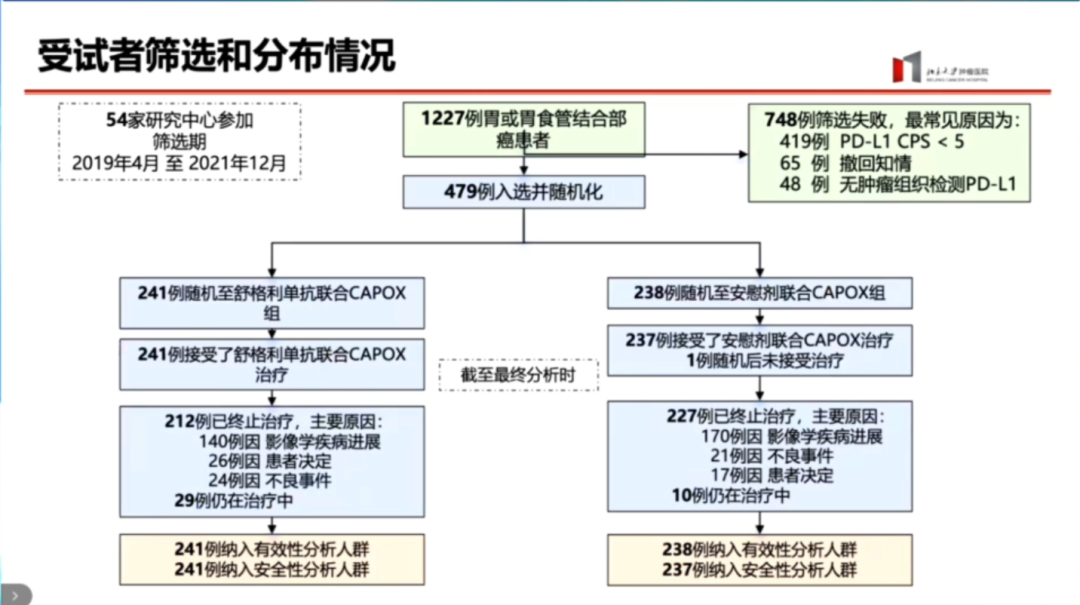
回顾受试者筛选情况,在疫情期间,54家中心共筛选了1227例患者,最终479例进行了随机分组,其中748例筛选失败,最常见的原因是CPS<5分,其他原因还包括撤回知情同意或无法提供PD-L1检测。两组的入组比例大致相当,分别为241例和238例。
截至最终分析时,相应患者分别有241例和238例纳入有效性分析人群和安全性分析人群。在治疗过程中,大部分患者因影像学疾病进展而终止治疗。在舒格利单抗组,有140例因影像学疾病进展终止治疗;在对照组的227例患者中,有170例因疾病进展终止治疗。
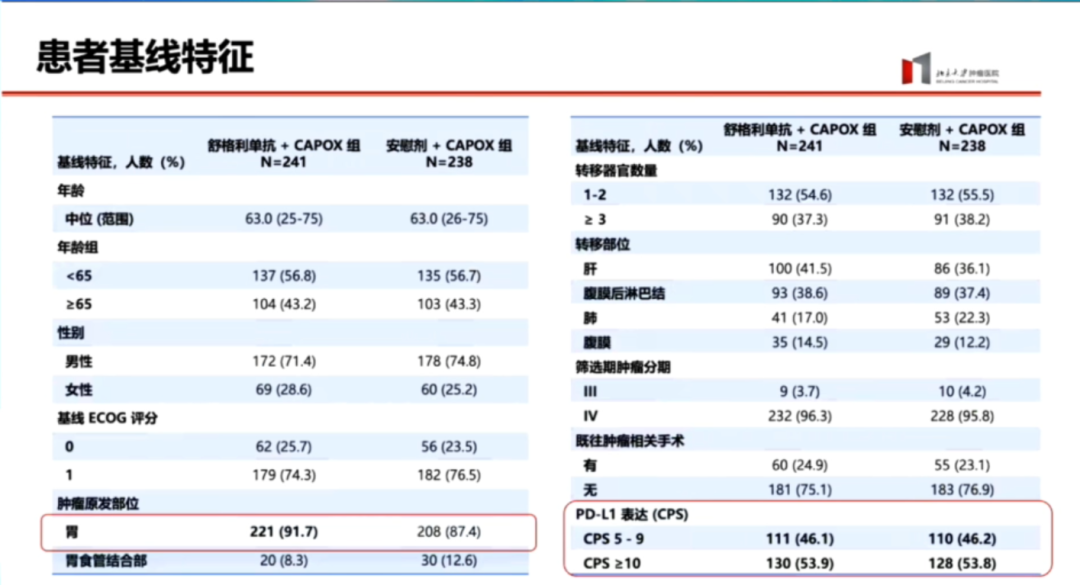
从患者基线特征来看,其非常符合东亚地区,尤其是中国地区晚期胃癌一线治疗的临床病理特征。患者人群平均年龄约63岁,以男性为主,体力状况评分0分和1分的比例大致为1/4和3/4,约90%的人群患有胃癌。从CPS评分表达来看,5~9分和10分以上的患者分别约占一半,这也是首次对中国人群中晚期胃癌PD-L1表达5~9分和10分以上表达区间的描述。
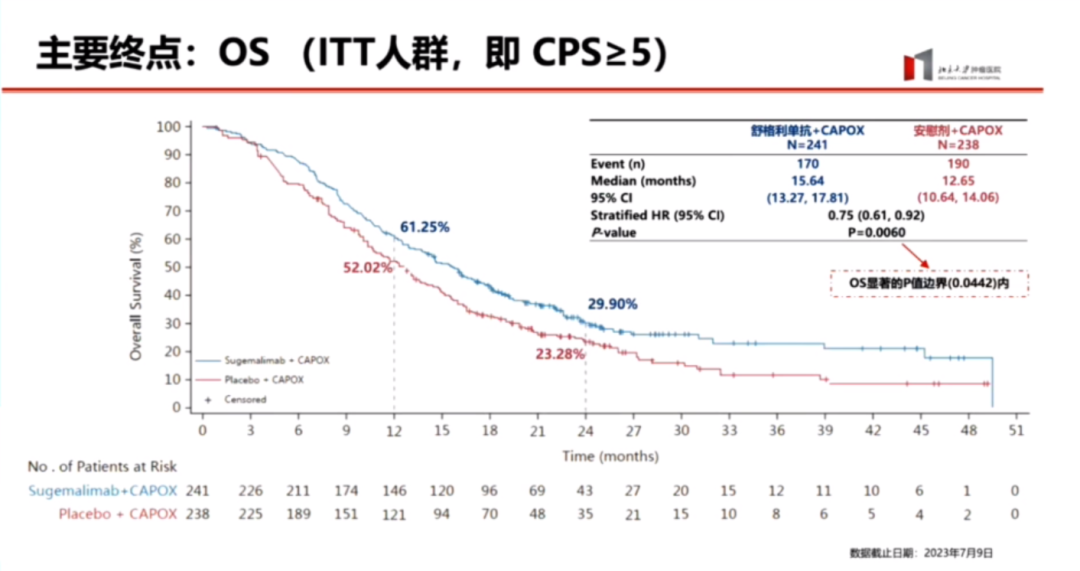
研究重点关注ITT(意向治疗)人群,即PD-L1 CPS≥5分的患者。主要终点结果显示,舒格利单抗组中位OS为15.64个月,安慰剂组为12.65个月,提升了3个月,P值为0.006,HR为0.75。生存曲线早期分离且清晰,未出现交叉或初期胶着,PFS曲线也呈现类似趋势。PFS差异为1.6个月,HR为0.66,复发风险降低34%,且PFS显著边界内生存曲线分离明确。
OS的亚组分析显示,CPS>10分的患者受益更显著,优于5分~9分的患者。
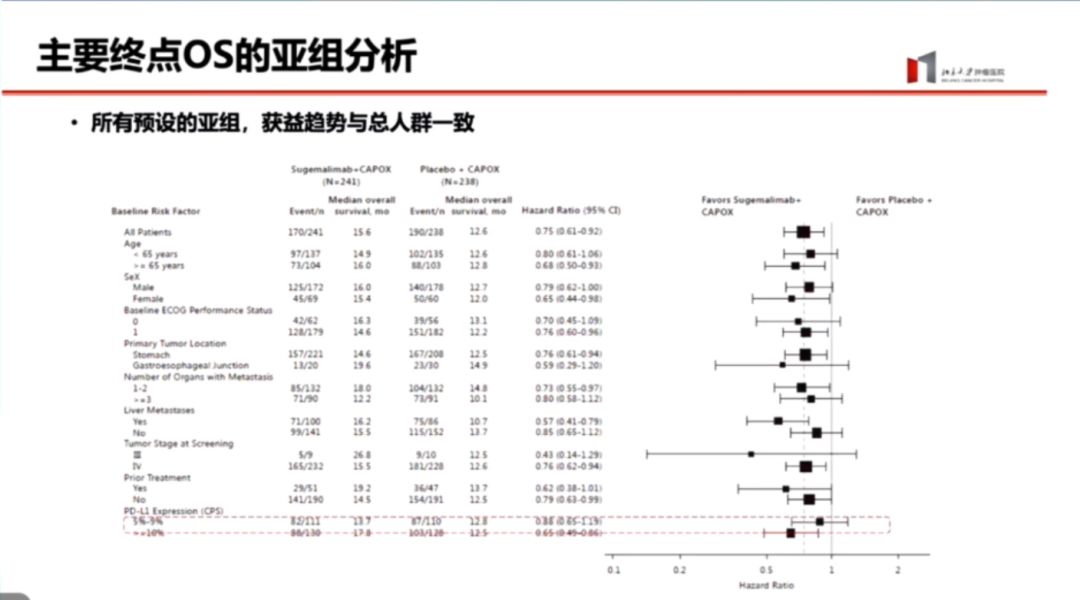
在CPS≥10分的亚组中,生存曲线从一开始就明确分离,呈现早分离状态。这对接受免疫治疗的患者至关重要,因为无法保证所有患者都不会出现免疫相关的不良事件(irAE)。早分离的生存曲线有助于明确区分受益人群,避免患者在治疗受益不明的情况下盲目参与治疗。
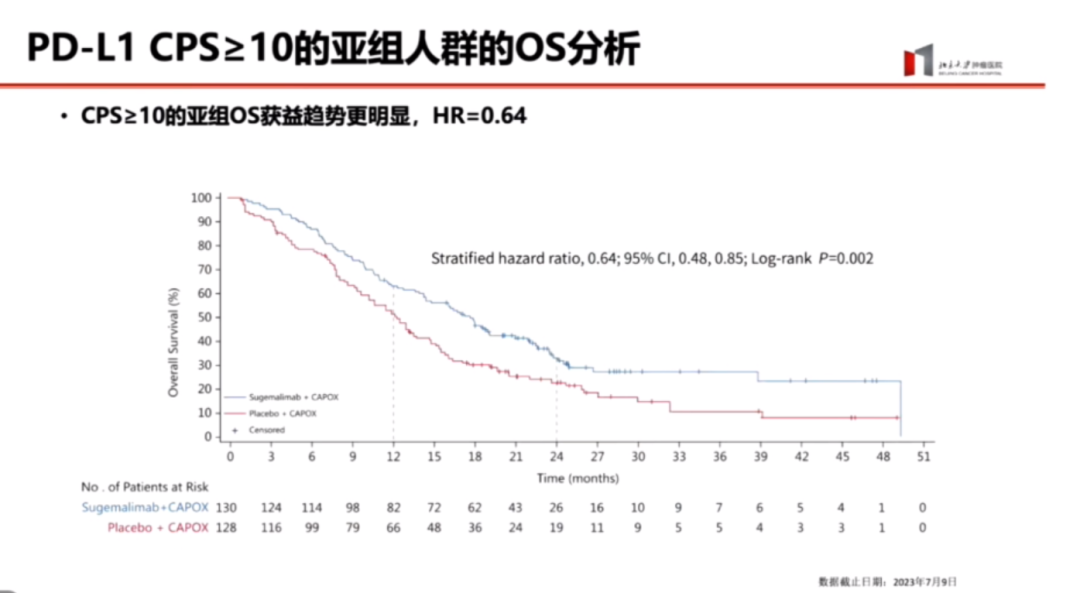
在主要终点PFS的亚组分析中,CPS≥10分的亚组受益也高于5分~9分的亚组,该亚组的PFS HR低至0.58,生存曲线分离明显。
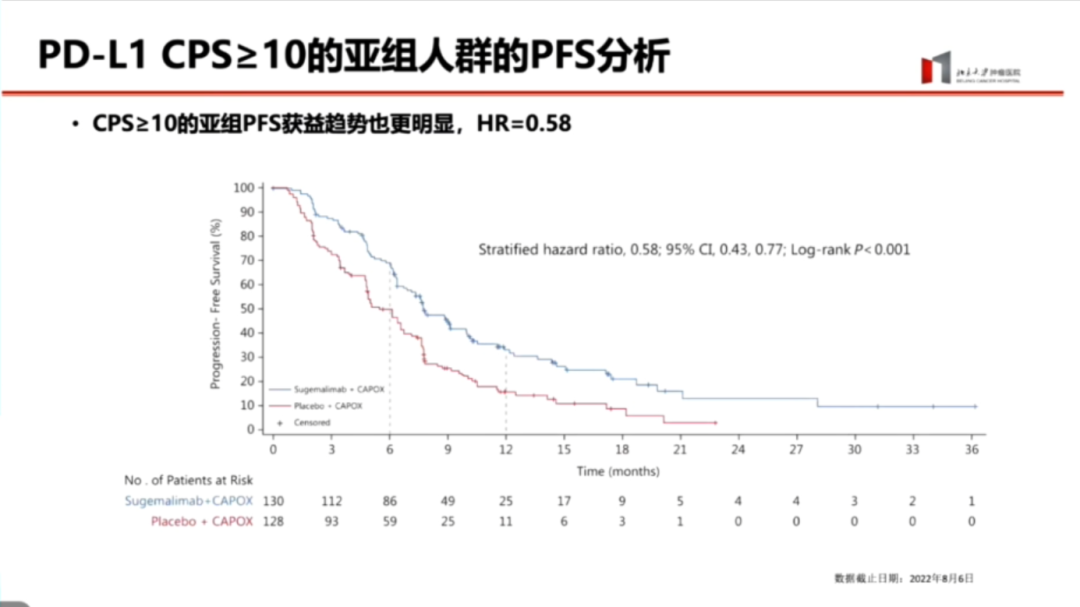
生存数据的延长对未来基于这些数据的分析至关重要,包括术前治疗、围手术期治疗,以及对这类患者进行精准筛选后的全流程管理,甚至在逆转耐药方面,都将对PD-L1 CPS作为一个人群筛选指标进行思考。然而,PD-L1 CPS评分只是众多生物标志物中的一个,其他如肿瘤突变负荷(TMB)和基于RNA的表达分析也在研究中。从肿瘤缓解率(ORR)来看,两组相差16个百分点,中位缓解持续时间(DOR)相差2.2个月。
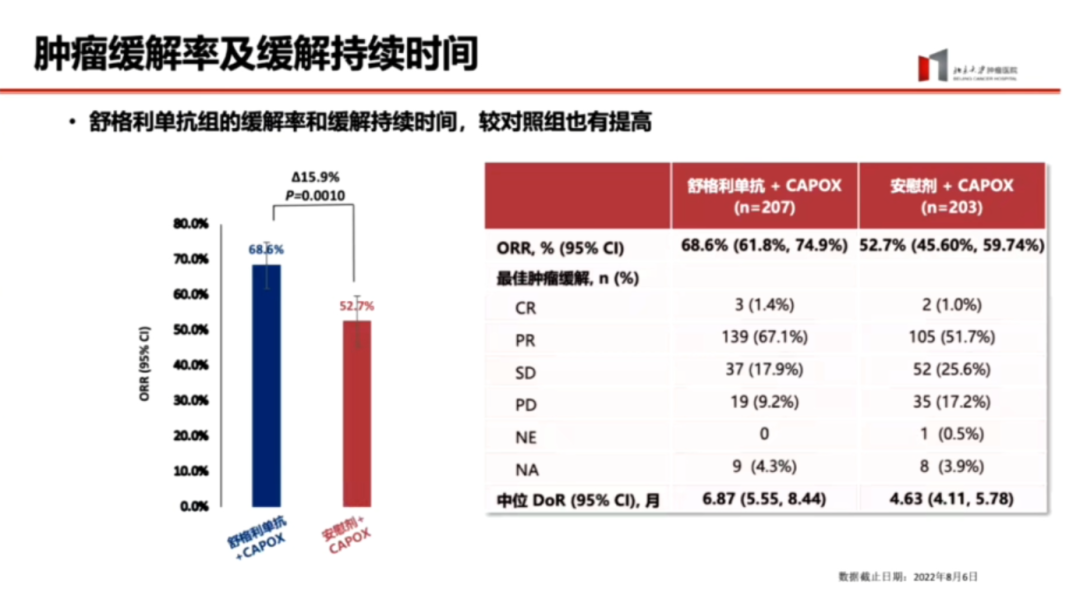
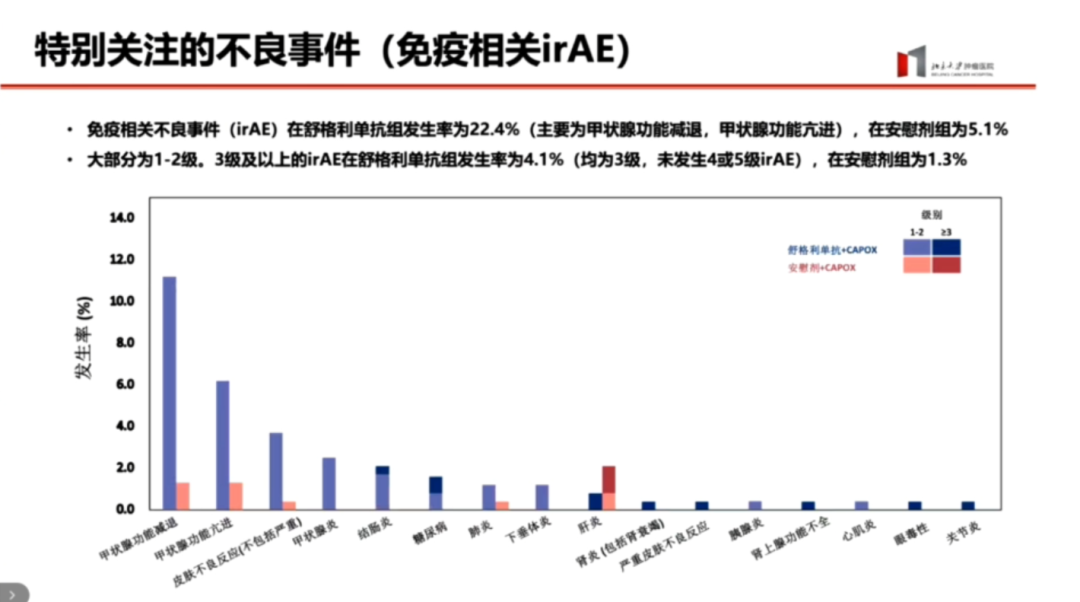
在不良事件方面,主要由化疗引起的血液学毒性和其他常见症状占主导,irAE总体发生率较低。在舒格利单抗组中,所有irAE的发生率为22%,主要为甲状腺功能异常,大部分为1~2级,三级及以上的irAE发生率为4.1%。这表明舒格利单抗的安全性较好,为未来PD-L1单抗在其他场景的应用提供了信心。
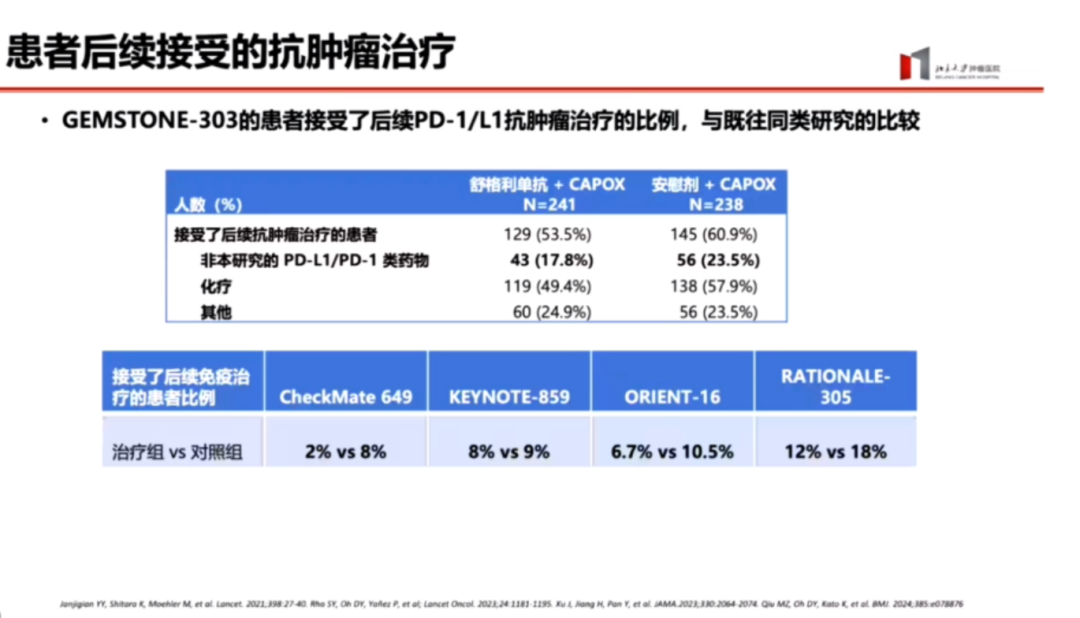
从后续接受其他非本研究的PD-L1单抗类药物的情况来看,两组的差别不大,分别为18%和23.5%。这与CheckMate-649、KEYNOTE-859、ORIENT-16以及RATIONALE-305等研究结果形成对比,这些研究中后续能接受PD-1单抗治疗的患者较少。这一现象为GEMSTONE-303研究的数据提供了重要补充。
本研究也得到了全国同行的认可,并于去年改写了CACA指南,作为晚期胃癌一线治疗推荐方案,优先推荐PD-L1 CPS评分≥5分的人群使用舒格利单抗联合XELOX治疗。

研究总结
本研究作为国际首个获批用于胃癌一线治疗的PD-L1单抗研究,成果令人自豪。其获批不仅基于Ⅲ期高级别循证医学依据,更凝聚了团队的临床智慧。在沈琳教授的带领下,北京大学肿瘤医院团队深入探讨了PD-L1 CPS评分筛选标准,结果显示,在CPS≥5分人群中,中位OS和中位PFS的死亡风险和复发风险分别降低25%和34%,在CPS>10分人群中,风险进一步降低10%,团队对CPS≥5分人群的疗效充满信心。
GEMSTONE-303研究的成功归功于精准的人群筛选和简洁的统计学设计。胃癌作为需精准治疗的肿瘤类型,其临床研究设计意义重大。未来,希望在全国同行支持下,北京大学肿瘤医院研究团队能进一步推进胃癌精准治疗及转化研究,以较小代价取得更大成果。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#晚期胃癌# #舒格利单抗# #CACA#
6