【Cancer Med】中国多中心研究探索骨髓瘤N新药时代诱导的结局和高危细胞遗传学数量的预后影响
2024-11-01 聊聊血液 聊聊血液 发表于上海
中国多中心研究分析不同诱导治疗对新诊断多发性骨髓瘤的效果及高危细胞遗传学异常数量对生存结局影响,发现双新药治疗有优势,双打击骨髓瘤预后差,需探索更有效疗法。
多发性骨髓瘤
在新药物时代,诱导治疗的临床结局和高危细胞遗传学异常(HRA)数量对新诊断多发性骨髓瘤(NDMM)的影响需要进一步探讨。因此中国多中心学者开展研究,旨在分析不同诱导治疗的有效性,并探讨不同数量HRA患者的生存结局,结果近日发表于《Cancer Medicine》。

研究结果
该研究共纳入中国7家中心2016-2023年的734例NDMM患者,337例患者接受免疫调节剂(IMiDs)+蛋白酶体抑制剂(PI)诱导治疗,134例患者接受达雷妥尤单抗为基础的诱导治疗,263例患者接受IMiDs或PI诱导治疗。在529例可获得FISH结果的患者中,327例患者没有HRA, 156例患者只有一个HRA, 37例患者有2个HRA, 9例患者有≥3个HRA。由于三打击MM患者数量较少,将2个HRA患者和≥3个HRA患者合并为≥2个HRA组。
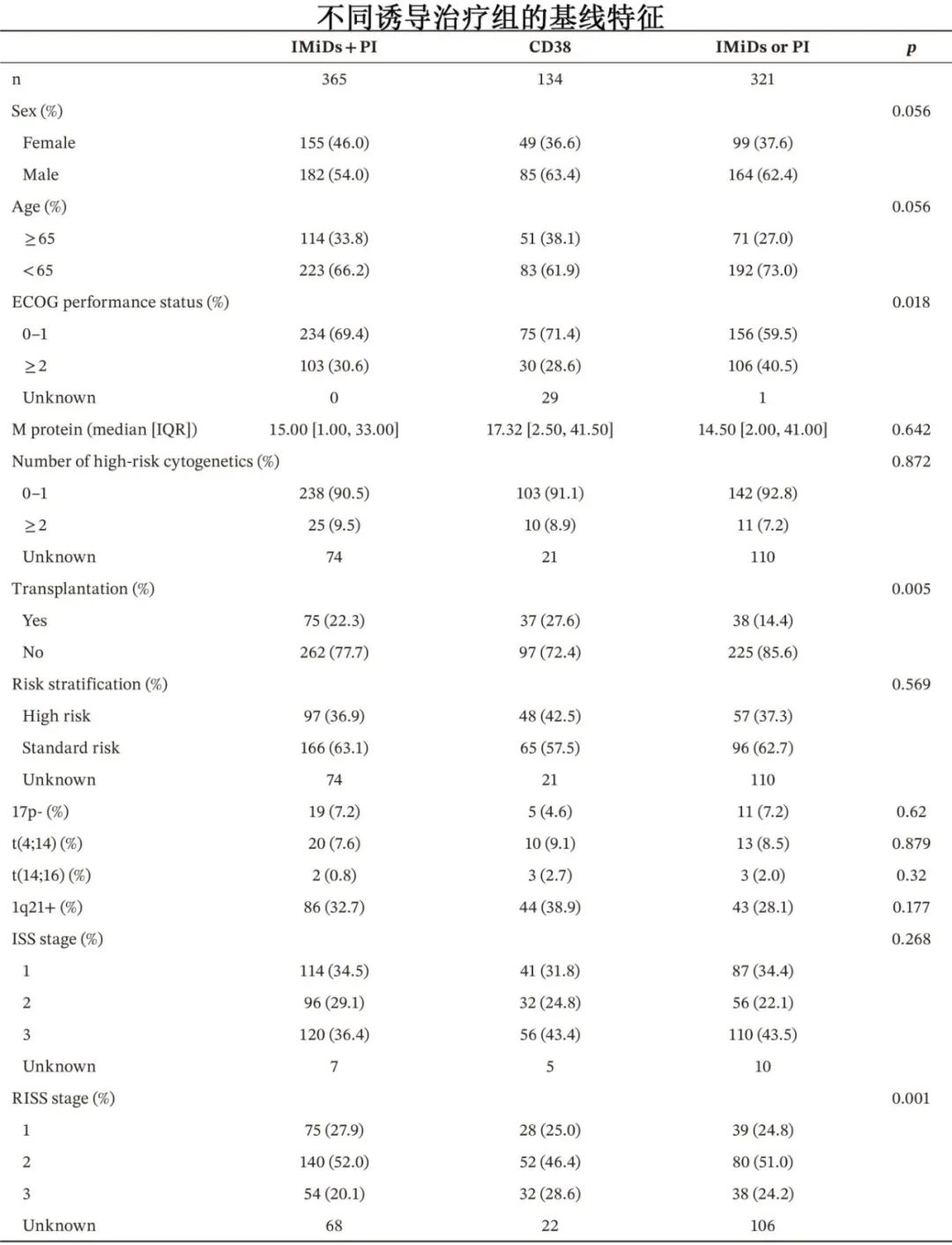
CD38单抗或IMiDs+PI组的完全缓解(CR)率和≥非常好的完全化解率(VGPR)均显著优于接受IMiDs或PI的患者,包括MRD(流式,10-5~10-4)阴性率同样如此。校正不平衡因素的多因素分析也发现,诱导治疗显著影响总缓解率。
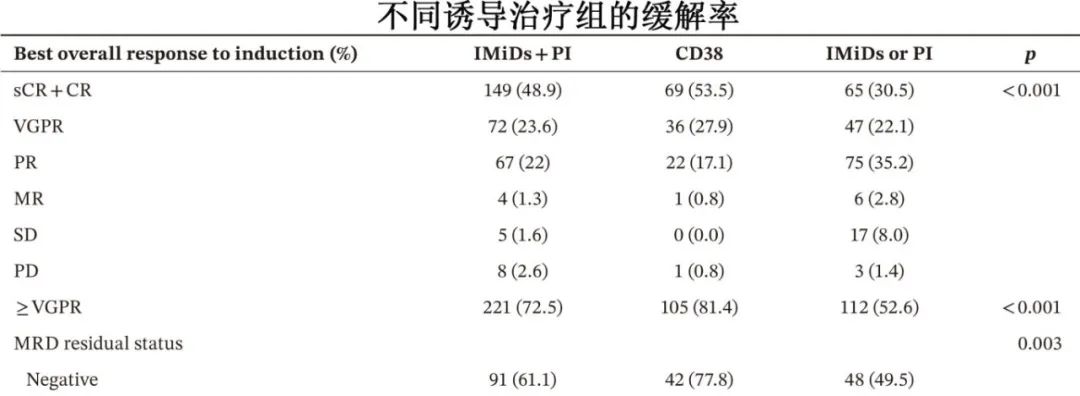
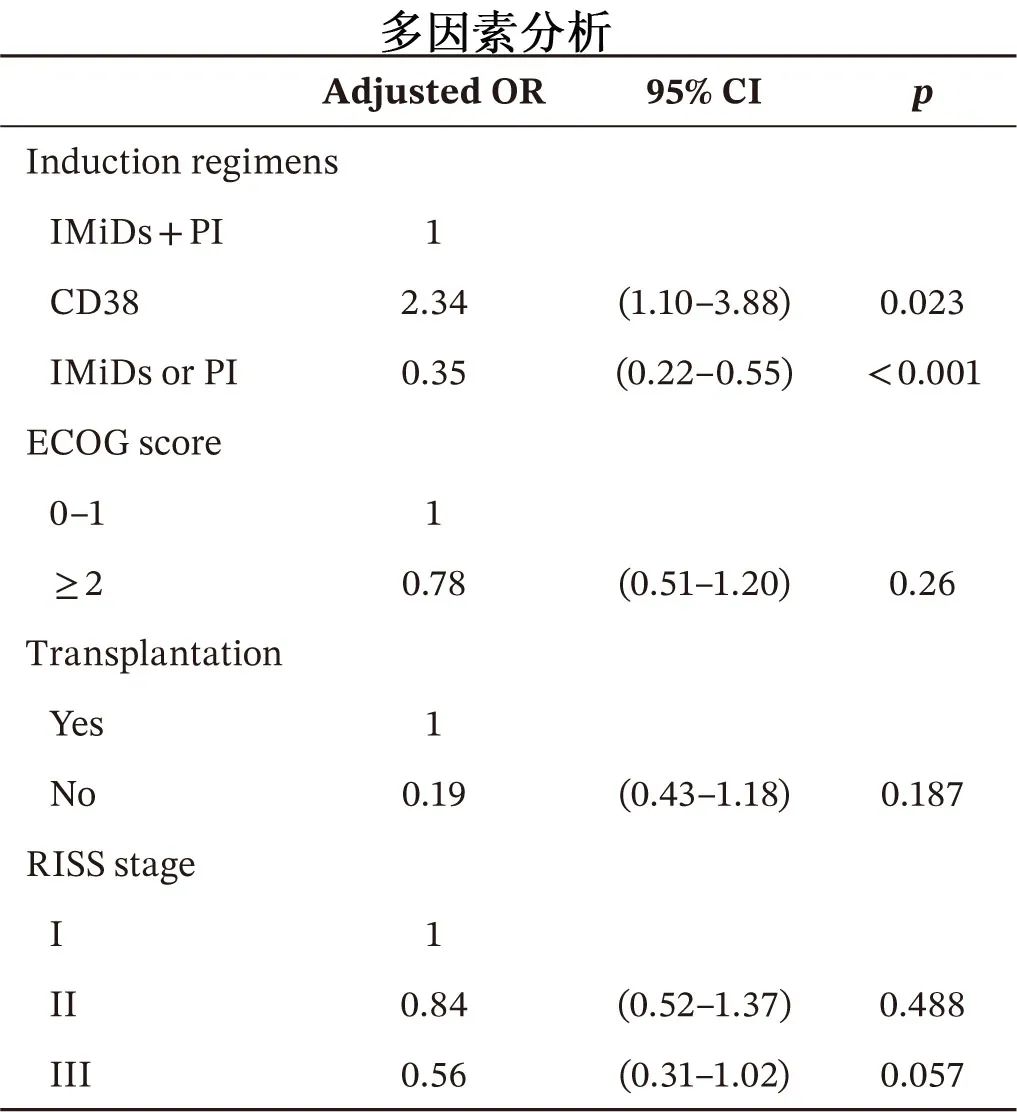
CD38单抗或IMiDs+PI组的总生存期(OS)和无进展生存期(PFS)均显著优于接受IMiDs或PI的患者,中位OS分别为未达到、70个月和67个月,PFS分别为54个月、44个月和44个月。此外,CD38单抗与IMiDs+PI相比具有PFS优势,但OS无统计学差异。
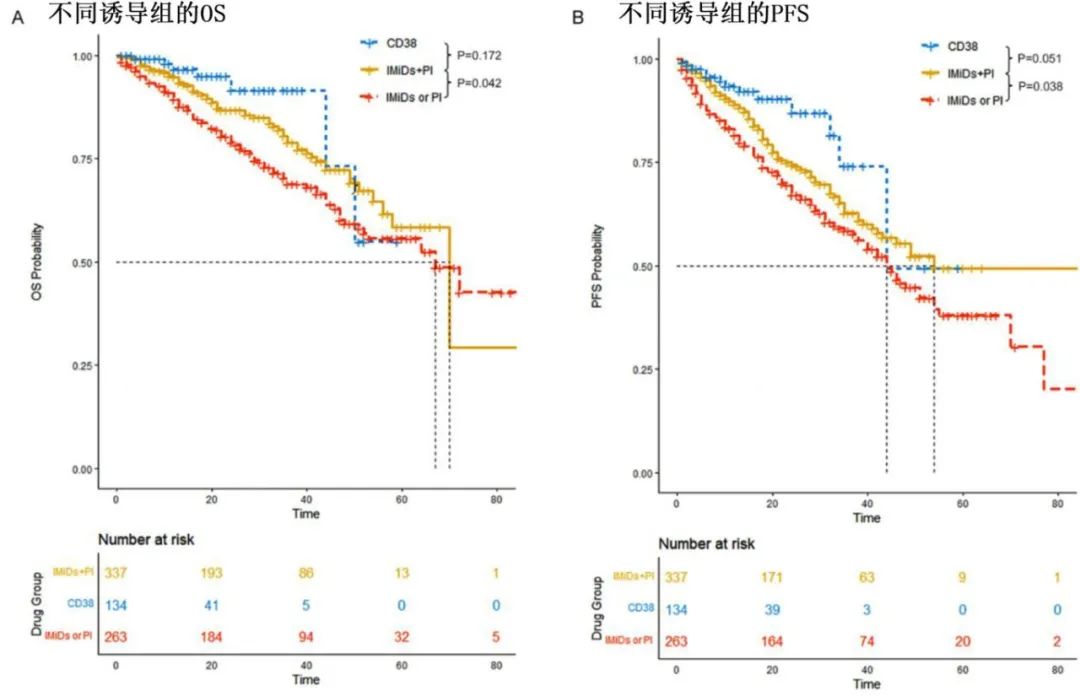
将患者根据HRA数量分为无HRA、1个HRA和≥2个HRA,中位OS分别为87、64和32个月,中位PFS分别为55、39和20个月。携带≥2个HRA的患者预后极差,应考虑为超高危。
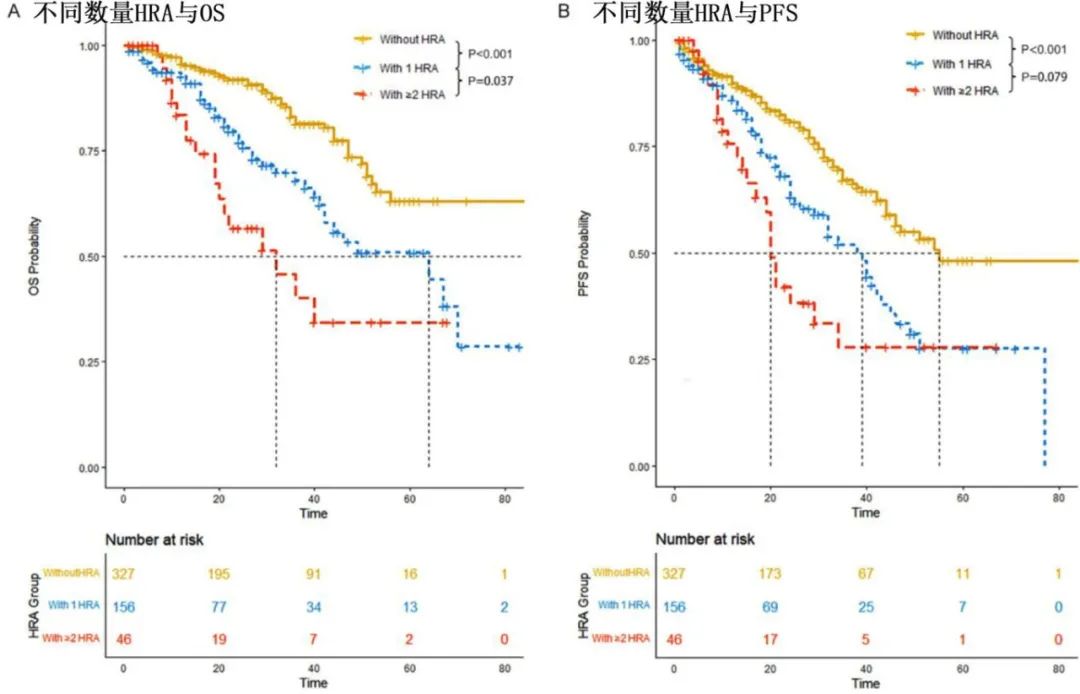
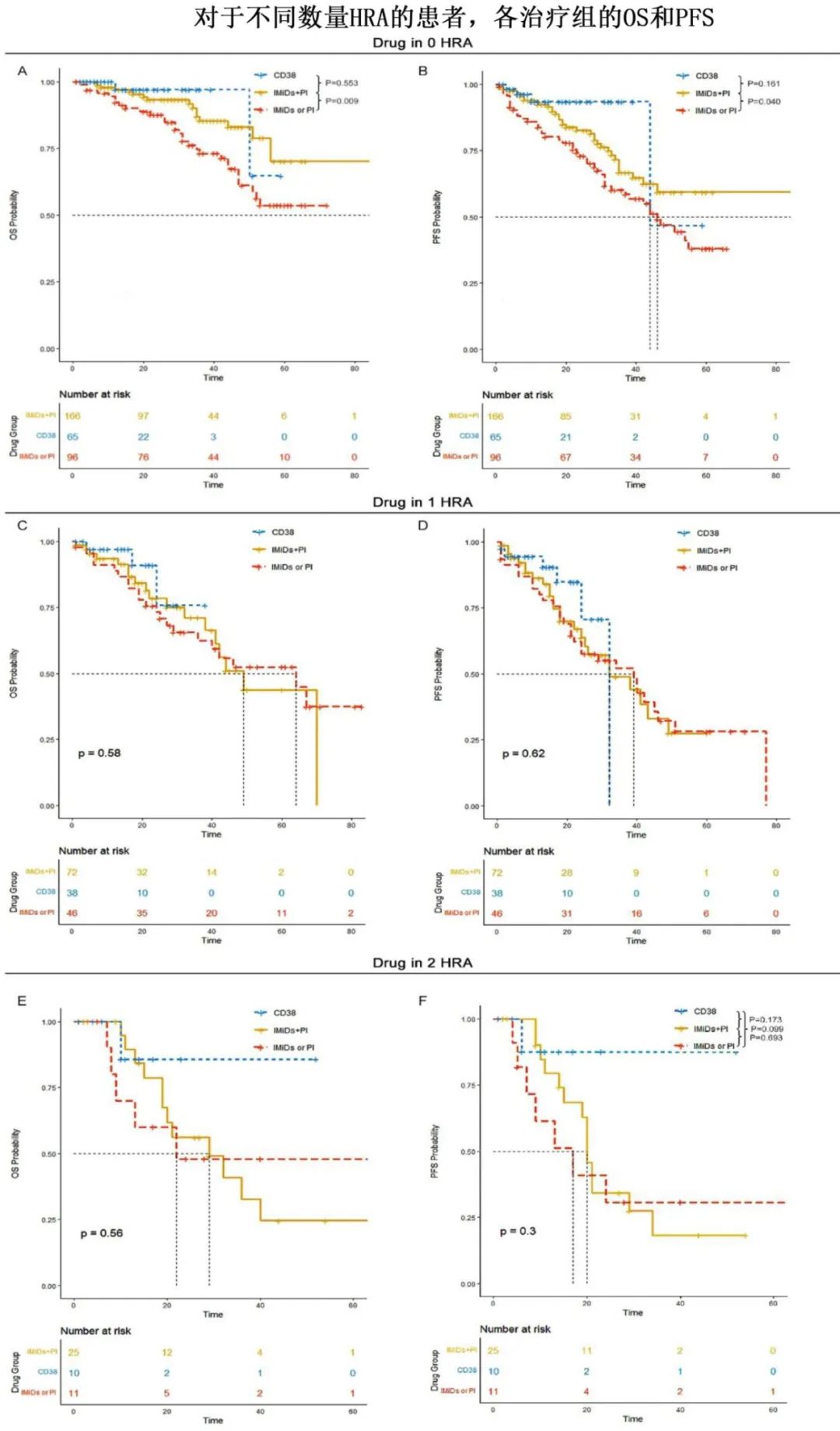
作者探讨了当前治疗模式对这些患者的疗效。在无HRA的患者中,CD38组或PI+IMiDs组的OS和PFS结果优于IMiDs或PI组;然而在1个HRA组,CD38组或IMiDs+PI组均无显著OS和PFS优势,表明目前的新型药物在克服HRA相关的不良预后方面疗效有限;同样,≥2个HRA患者的OS和PFS较短,CD38单克隆抗体和IMiDs+PI均未显著改善生存。进一步探索发现,移植和实现MRD阴性同样仅在无HRA组有生存获益,而在1个和≥2个HRA组均无显著影响,证实CD38单抗、移植和实现MRD阴性仅可部分减轻HRA患者的不良预后。
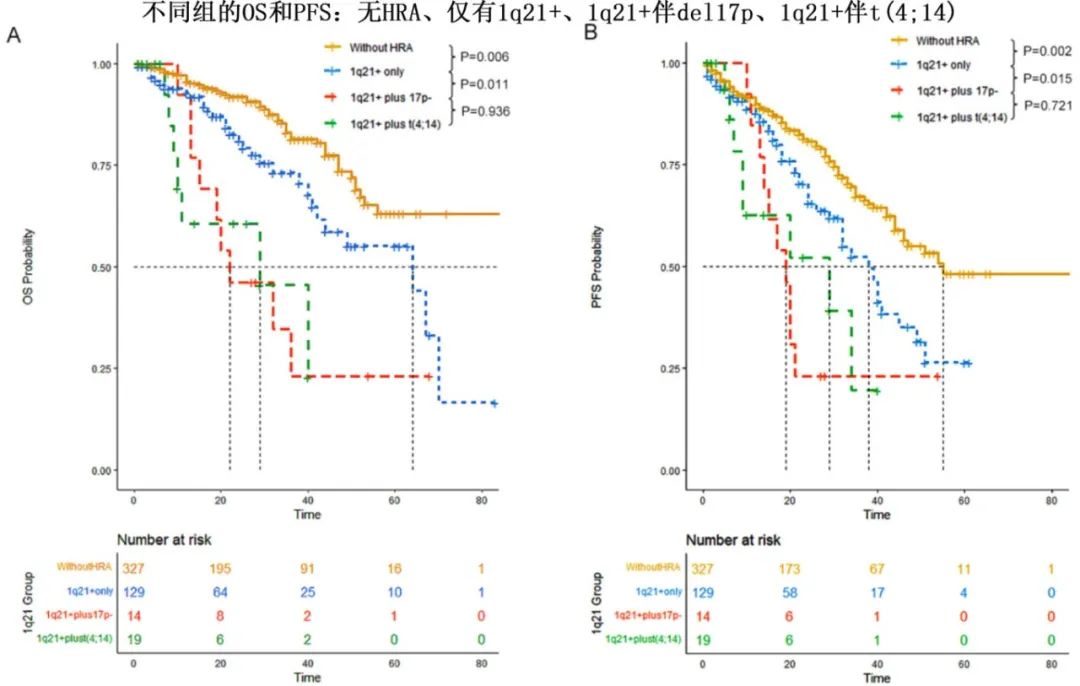
1q21获得/扩增(1q21+)是近些年的研究热点,与不良预后相关,1q21+与del17p和t(4;14)共突变较常见但其预后意义不明确。该研究发现,与没有HRA的患者相比,仅携带1q21+的患者预后明显更差,而与单独1q21+的患者相比,1q21+伴del17p或t(4;14)的患者预后也更差。
总结
该研究表明,两个及以上新药治疗多发性骨髓瘤具有优势,可提高缓解率和生存期。而双打击骨髓瘤与极差的生存结局相关,需要探索针对这种特殊亚型MM的更有效的治疗方法。
参考文献
Liang D, Li X,Bai S,et al.Clinical Outcome of Induction Treatment in the Era of Novel Agents and the Impact of the Number of High-Risk Cytogenetic Abnormalities (HRA) on Prognosis of Patients With Newly Diagnosed Multiple Myeloma (NDMM): Insights From a Multicenter Study. Cancer Med. 2024 Oct;13(20):e70270. doi: 10.1002/cam4.70270.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#多发性骨髓瘤# #高危细胞遗传学#
17