Nature Biotechnology:从“止血英雄”到“抗癌先锋”:血小板的惊人新用途
2024-12-05 生物探索 生物探索 发表于陕西省
Nature Biotechnol 研究开发 DePLTs 用于 TPD,阐述 TPD 原理问题,DePLTs 借血小板特性结合 HSP90 实现降解,在乳腺癌模型中效果显著且安全,具临床应用潜力。
引言
现代医学在癌症治疗领域取得了诸多进展,但术后癌症复发和转移仍然是患者面临的最大威胁。传统疗法如放疗、化疗和免疫疗法虽然能够在一定程度上延缓病情,但它们往往伴随严重副作用,且对隐匿的癌细胞残余和微小转移灶束手无策。如何在确保安全的前提下精准清除残余病灶,成为研究人员亟需攻克的难题。
靶向蛋白降解(Targeted Protein Degradation, TPD)是一项颠覆性的技术,通过消除疾病相关的蛋白质,从根本上阻断癌细胞的生长与扩散。与传统药物只能抑制蛋白功能不同,TPD能够彻底“拆解”问题蛋白,为难以药物化的靶点提供了解决方案。然而,这一技术在实际应用中面临两大核心难题:药物分布受限和潜在的脱靶毒性。现有TPD技术难以精准定位病灶,同时可能引发全身性的副作用,限制了其临床转化的进程。
在这种背景下,12月3日Nature Biotechnology的一项全新的研究“Engineered platelets as targeted protein degraders and application to breast cancer models”为TPD注入了革命性突破:工程化血小板(DePLTs)的开发。这种“生物导航载体”利用血小板天然的组织靶向性,能精准聚集于手术伤口或病变部位,将降解分子高效递送至目标区域。更令人振奋的是,DePLTs通过携带标记了目标蛋白配体的热休克蛋白90(HSP90),分别通过细胞内的泛素-蛋白酶体系统(UPS)和细胞外的溶酶体系统实现双重降解。这种创新不仅解决了药物分布的问题,还通过降低副作用风险显著提升了安全性。
在乳腺癌术后小鼠模型中,DePLTs展示了强大的疗效:不仅能显著抑制癌症复发,还成功阻止了癌细胞的肺部转移。同时,实验结果证明这一技术对机体的重要器官几乎“零干扰”,展现了其卓越的生物相容性。这种结合精准靶向、高效降解与安全性的技术,为癌症治疗带来了新的希望。
DePLTs的出现,不仅是TPD技术发展的重要里程碑,更为术后癌症治疗带来了颠覆性的解决方案。未来,这一技术有望成为医学界对抗癌症的新利器,让更多患者享受到精准医学带来的福祉。这场关于“降解”的医学革命,才刚刚拉开帷幕!

什么是靶向蛋白降解(TPD),它能解决什么问题?
靶向蛋白降解(Targeted Protein Degradation,TPD)是一项迅速发展的生物技术,它通过“拆除”疾病相关的蛋白质,直接针对疾病的根源。这种方法突破了传统药物治疗的限制,尤其是在癌症等复杂疾病中显示出巨大潜力。
TPD的基本原理:化学剪刀精准清除
简单来说,TPD利用一种特殊的“双头分子”(chimeric molecule)将目标蛋白(Protein of Interest, POI)送入细胞的“垃圾处理系统”,包括泛素-蛋白酶体系统(Ubiquitin-Proteasome System,UPS)和溶酶体(lysosome)。这种分子一端结合目标蛋白,另一端则与负责降解的效应蛋白结合,通过桥接两者形成“三元复合体”,启动降解过程。
传统药物通常只能“关闭”某些蛋白的功能,例如通过抑制酶活性或阻止蛋白与其他分子的结合。而TPD则不同,它能彻底消除问题蛋白。因此,TPD特别适用于那些被认为“不可药物化”的蛋白靶点,为众多疾病的治疗提供了新的可能性。
TPD的挑战:从实验室到人体的坎坷之路
尽管TPD概念诱人,但要将其成功应用于人体却充满挑战。当前TPD技术面临的核心问题包括药物分布和副作用风险。
药物分布受限:TPD分子通常体积较大、结构复杂,难以通过细胞膜渗透到目标部位。同时,药物可能在全身广泛分布,却难以集中于病变组织,从而降低治疗效率。
副作用风险:由于TPD分子需同时结合目标蛋白和降解系统,它们的活性高度依赖于“三元复合体”的精确形成。然而,稍有偏差便可能导致脱靶效应或非靶组织上的毒性反应,带来严重安全隐患。
技术突破:为TPD注入“定向导航”
为克服上述问题,研究人员不断尝试将TPD的潜力推向临床应用。该研究创新性地将血小板这一天然生物载体引入TPD,将目标蛋白的降解过程定向至特定组织。这种方法不仅改善了药物分布问题,还通过“靶向递送”大大降低了副作用风险。这样的技术创新让TPD更接近成为临床治疗的新工具。
工程化血小板:革命性的蛋白降解“工具”
血小板(platelets)通常被认为是止血与伤口修复的主力军。然而,该研究发现,它们还可以被改造成“精准打击”的武器,为靶向蛋白降解(TPD)开辟全新途径。这一创举不仅颠覆了人们对血小板的传统认知,也为解决TPD的分布问题提供了突破性思路。
血小板:天然的“导航员”
血小板之所以被选中,离不开其独特的生物学特性。血小板能主动识别损伤部位并快速聚集,这是其他药物载体难以比拟的天然优势。在癌症治疗中,手术后的残留肿瘤细胞常位于微小的出血区域,而血小板对这些部位的高度亲和性使其成为理想的药物递送载体。
更重要的是,血小板在激活后会释放出大量的血小板衍生微粒(platelet-derived microparticles, PMPs),这些微粒携带血小板内部的内容物并能够与靶细胞膜融合,将治疗分子直接传递到目标细胞。这种特性为蛋白降解药物的高效输送提供了“快车道”。
HSP90:从“分子伴侣”到“降解引擎”
该研究的核心创新在于,将靶向蛋白降解的关键分子——热休克蛋白90(Heat Shock Protein 90, HSP90)标记到血小板中。HSP90是一种天然的“分子伴侣”,负责帮助细胞内的蛋白质折叠和稳定。在这项技术中,研究人员通过化学方法将目标蛋白的配体(POI ligand)与HSP90结合,生成了一种“预装载”的降解分子。这种标记后的HSP90既能通过PMPs传递到靶细胞内部,也可以在血小板激活后直接释放到细胞外,从而启动两种降解机制:细胞内通过泛素-蛋白酶体系统(UPS)降解蛋白,细胞外则通过溶酶体途径清除目标蛋白。
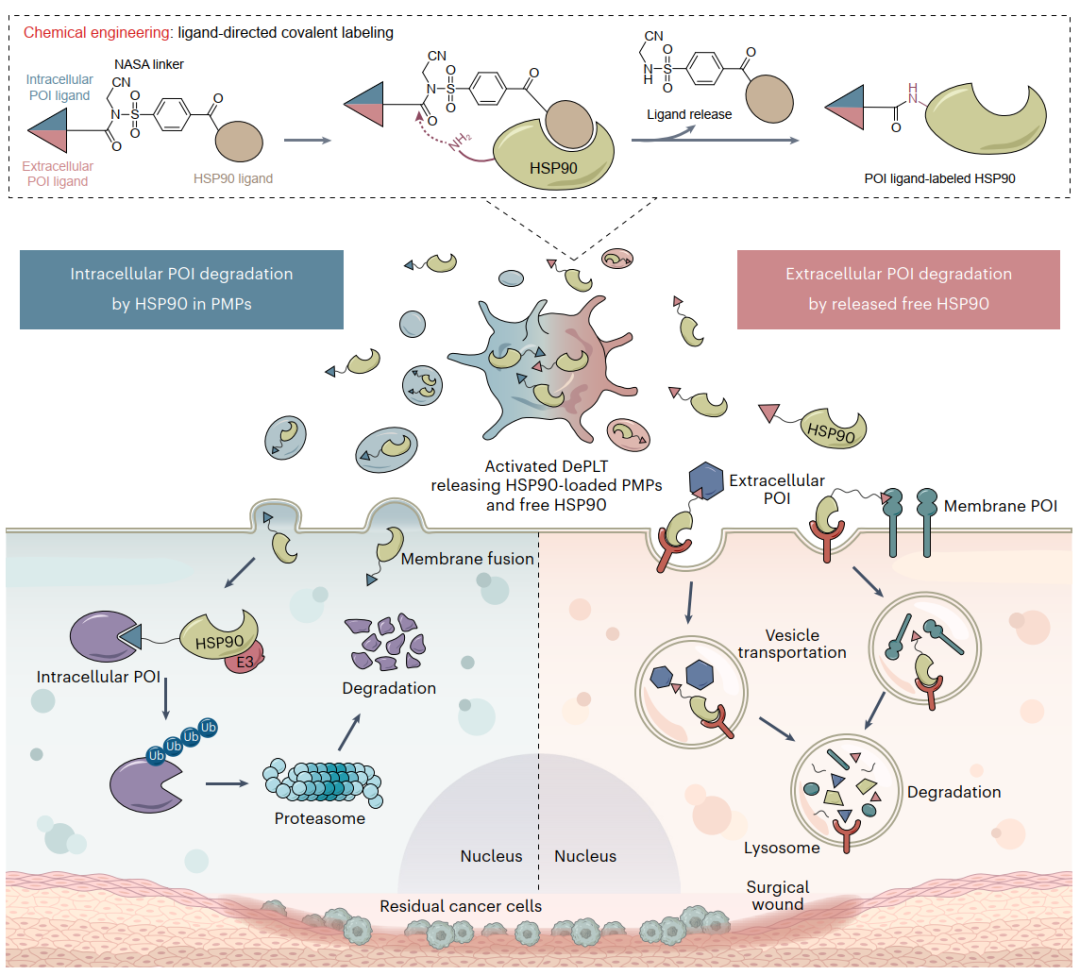
工程化血小板(DePLTs)实现靶向蛋白降解(TPD)的设计原理和功能机制(Credit: Nature Biotechnology)
DePLTs的工程化过程:图中描述了研究人员如何通过配体定向的共价标记技术(ligand-directed covalent labeling),将目标蛋白(POI)的配体与热休克蛋白90(HSP90)结合,生成带有HSP90标记的工程化血小板(DePLTs)。这一过程使血小板具备了靶向降解特定蛋白的能力。
DePLTs的靶向能力:DePLTs具有天然的“趋向性”(tropism),能够优先定位到术后出血区域。图中指出,这种定位特性源于血小板对伤口区域的高度亲和性,使得DePLTs能够选择性地聚集于病变或手术残余区域。
双重蛋白降解机制:根据图示,DePLTs可通过两种不同的途径实现目标蛋白的降解:
细胞内降解:HSP90被装载到血小板衍生微粒(PMPs)中,通过PMP与癌细胞膜的融合,HSP90进入靶细胞并启动泛素-蛋白酶体系统(UPS),降解细胞内的目标蛋白(如BRD4)。
细胞外降解:DePLTs在激活后释放自由的HSP90,这些HSP90结合细胞外的目标蛋白并引导其进入靶细胞的溶酶体,实现溶酶体介导的蛋白降解(如PD-L1)。
分子机制的高度可控性:图中强调,根据配体的不同,DePLTs可以针对细胞内或细胞外的目标蛋白,选择性地采用UPS或溶酶体途径。这种设计显著增强了技术的适用性和精确性。
内外兼修:细胞内外蛋白降解的新机制
蛋白质是细胞功能的基石,但当某些蛋白“变坏”时,它们也可能成为疾病的根源。因此,研究人员致力于研究如何高效地降解这些异常蛋白,而细胞内的泛素-蛋白酶体系统(UPS)和细胞外的溶酶体系统则是这一过程的关键“武器库”。
UPS系统:精准拆解细胞内的“废弃物”
UPS是细胞内的主要蛋白降解途径,通过为目标蛋白贴上“泛素标签”引导其进入蛋白酶体,这一“分子粉碎机”将目标蛋白分解为小分子肽段。在该研究中,工程化血小板(DePLTs)通过释放加载了目标蛋白配体的HSP90微粒(PMPs),将降解信号传递到靶细胞。PMP内的HSP90随后将目标蛋白(如BRD4)与UPS联结,从而实现细胞内的高效降解。实验显示,在不同浓度的工程化血小板处理后,乳腺癌细胞中BRD4蛋白的表达水平显著降低,降解效率呈浓度和时间依赖性,表明DePLTs通过UPS能够精确而高效地清除目标蛋白。
溶酶体:清扫细胞外的“危险因子”
溶酶体则是细胞清除外部废物的“垃圾处理站”,通过酶解作用降解进入细胞的蛋白。在细胞外,激活的DePLTs可以释放自由形式的HSP90,这些HSP90结合了目标蛋白的配体后,将外部目标蛋白(如PD-L1)重新引导至靶细胞的溶酶体。研究发现,当PD-L1被自由HSP90标记后,其在溶酶体内的积累显著增加,而溶酶体抑制剂则能够阻断这一降解过程,证实溶酶体在DePLTs介导的细胞外蛋白降解中的核心作用。
内外结合的技术优势
与传统单一机制的靶向治疗不同,DePLTs通过内外双向作用,结合UPS和溶酶体两大降解系统,显著提升了对细胞内外病变蛋白的处理能力。这种内外兼修的设计,使得DePLTs成为疾病治疗中更加灵活和高效的“清除工具”。不论目标蛋白藏身何处,它都逃不过这场降解风暴!
实战演练:从乳腺癌模型看DePLTs的威力
在乳腺癌模型中的一系列实验中,工程化血小板(DePLTs)用数据展示了其强大的“实战能力”,不仅精准降解目标蛋白,还在癌症复发和转移的抑制上发挥了令人惊叹的作用。
BRD4降解:阻断癌细胞的生存信号
BRD4是一种在癌细胞生长中起重要作用的蛋白,尤其是三阴性乳腺癌(TNBC),对现有疗法高度耐药。研究显示,当乳腺癌细胞(4T1细胞系)被DePLTs处理后,BRD4蛋白的表达水平明显下降,并呈现浓度和时间依赖性。例如,在实验中,2 × 10⁸个DePLTs处理12小时后,BRD4水平降低至原始水平的18%。这表明,DePLTs通过释放携带BRD4配体标记的HSP90微粒,将BRD4直接引导至UPS系统,精准高效地摧毁这一“癌细胞指挥官”。
PD-L1降解:唤醒免疫系统的“沉睡战士”
PD-L1是癌细胞用来逃避免疫系统攻击的“盾牌”,其过度表达是肿瘤免疫逃逸的主要原因。研究进一步验证了DePLTs在降解细胞外PD-L1的作用机制。实验显示,PD-L1标记后的自由HSP90通过溶酶体途径显著减少了PD-L1的表达。当溶酶体抑制剂加入后,这一降解过程被显著阻断,进一步确认了溶酶体的参与。这一结果不仅削弱了癌细胞的防御,还为免疫细胞的活性恢复创造了条件。
癌症复发与转移的全面抑制
在术后乳腺癌小鼠模型中,DePLTs在抑制癌症复发和转移方面展现了非凡效果。实验显示,接受DePLTs治疗的小鼠术后复发率显著降低,与对照组相比,残余肿瘤的生长几乎完全受到抑制。更令人振奋的是,DePLTs还有效防止了癌细胞向肺部的转移,在治疗组小鼠的肺部未发现任何明显的转移性病灶。
生物安全性:治疗效果与副作用的平衡
疗效固然重要,但生物安全性才是技术走向临床的关键门槛。DePLTs,这种革新性的蛋白降解“工具”,不仅在癌症治疗中表现出卓越的效果,其安全性也令人印象深刻。
精准分布:锁定目标,避开误伤
DePLTs通过血小板的天然生物学特性实现了精准的体内分布。实验表明,在术后乳腺癌小鼠模型中,工程化血小板能够迅速聚集于手术伤口附近的肿瘤组织,而对健康器官的分布相对较少。荧光成像数据显示,注射24小时后,DePLTs在肿瘤部位的累积量显著高于其他组织,仅肝脏中检测到部分分布,显示出血小板“导航系统”的高效性。这种特性使得药物精准抵达病灶,避免了传统治疗中全身分布导致的脱靶副作用。
低毒性:重要器官的“零负担”
在DePLTs治疗期间,小鼠的主要器官(如心脏、肝脏、肺和肾脏)均未表现出明显的病理损伤。血液生化分析进一步证明,这种治疗不会引起肝功能(ALT和AST)或肾功能(BUN)的显著异常。与对照组相比,接受DePLTs治疗的小鼠体重稳定,无明显毒性相关症状。这些结果表明,DePLTs在完成治疗任务的同时,对机体的重要器官几乎“零干扰”。
高安全性:持久效果与稳定性能
DePLTs不仅表现出优异的治疗效果,还展现了良好的生物相容性。在多次治疗后,小鼠的血液指标保持稳定,未见免疫反应或凝血功能异常。此外,DePLTs的工程化过程并未破坏血小板的天然功能,其激活后仍能高效聚集于病灶并释放治疗分子,确保了治疗过程的可控性和安全性。
打破僵局:DePLTs在临床应用中的潜力
癌症治疗的术后复发和转移始终是难以攻克的顽疾。而DePLTs的出现,为解决这一问题带来了全新的希望。通过精准靶向和高效降解,DePLTs有望成为术后癌症治疗的革命性武器。
改变术后癌症治疗的现状
现有术后癌症治疗手段如放疗、化疗和免疫疗法,尽管能够一定程度延缓病情,但它们往往伴随副作用,且对微小残留病灶的清除能力有限。而DePLTs则通过血小板的天然组织靶向性,将治疗分子精准递送至手术伤口和潜在转移部位。在实验中,DePLTs有效抑制了乳腺癌小鼠术后的肿瘤复发和肺部转移,这一技术显现出针对残留癌细胞的强大破坏力。更重要的是,与传统疗法相比,DePLTs的高安全性和低副作用为患者的术后恢复提供了更优选择。
拓展应用场景:更多疾病的可能性
DePLTs的应用前景绝不仅限于乳腺癌。其双重降解机制使其能够应对多种疾病,包括其他类型的实体肿瘤、转移性癌症,甚至一些与异常蛋白质相关的神经退行性疾病。特别是在对免疫治疗耐药的癌症中,DePLTs通过PD-L1降解来恢复免疫反应的能力,极具临床价值。此外,通过调整HSP90标记的配体类型,这一技术可以快速适配不同目标蛋白,打造“个性化治疗方案”。
优化方向:从实验室走向临床
虽然DePLTs已表现出非凡的潜力,但将其推向广泛的临床应用仍需解决一些技术难题。例如,如何进一步提高血小板的加载效率,如何确保它们在人体内的长效稳定性,以及如何最大限度减少可能的脱靶效应。此外,开发更高效、低成本的工程化技术将是未来的重要方向,这将决定DePLTs能否成为大规模推广的主流疗法。
DePLTs为术后癌症治疗开辟了一条全新的道路,它不仅是一项突破性技术,更是一种治疗理念的变革——从传统的“全身轰炸”到精准的“靶点摧毁”。可以预见,在未来的临床应用中,DePLTs将为患者提供更安全、更高效的治疗选择,也将成为医学界对抗癌症的新利器,为无数家庭带来希望与曙光。
参考文献
Chen, Y., Pal, S., Li, W. et al. Engineered platelets as targeted protein degraders and application to breast cancer models. Nat Biotechnol (2024). https://doi.org/10.1038/s41587-024-02494-8
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#乳腺癌# #靶向蛋白降解# #工程化血小板#
20