Cancer Res:复旦大学许杰等团队合作研究发现SEMA3G是癌症中免疫反应的关键调节因子
2025-03-21 iNature iNature 发表于陕西省
该研究确定了semaphorin 3G(SEMA3G)是癌症中免疫反应的关键调节因子。
肿瘤微环境中的T细胞通常表现出功能障碍特征,这些特征损害了它们引发先天性和治疗性诱导免疫反应的能力。免疫功能障碍的调节因子代表了激活抗肿瘤免疫的治疗靶点。
2025年3月3日,复旦大学许杰和Shouyan Deng共同通讯在Cancer Research在线发表题为“SEMA3G–NRP1 Signaling Functions as an Immune Checkpoint That Enables Tumor Immune Evasion by Impairing T-cell Cytotoxicity”的研究论文。该研究确定了semaphorin 3G(SEMA3G)是癌症中免疫反应的关键调节因子。
SEMA3G在多种人类癌症中广泛上调,并且其表达与肿瘤进展呈正相关。SEMA3G作为一种配体,抑制T细胞的激活和功能。一种全面的受体筛选方法表明,SEMA3G对神经纤毛蛋白(NRP)1的亲和力明显强于对NRP2的亲和力。此外,SEMA3G主要通过NRP1阻碍T细胞功能。使用CRISPR/Cas9技术破坏SEMA3G或用中和抗体阻断SEMA3G可有效恢复CD8+ T细胞的细胞毒性并抑制体内肿瘤的生长。本研究强调了SEMA3G在肿瘤内T细胞功能障碍中的作用,并提出了将SEMA3G作为癌症免疫治疗策略的目标。

癌症免疫治疗已经改变了癌症治疗的格局。值得注意的是,针对PD-1和PD-L1的免疫检查点抑制剂(ICI)的成功,以及抗体-药物偶联物和嵌合抗原受体T细胞疗法的进步,已经在多种癌症类型中的选定患者群体中产生了显著且持久的反应。然而,ICI的临床反应仅限于少数患者,这凸显了对预测性生物标志物的迫切需求,以及开发针对额外免疫检查点的策略以提高ICI的疗效。
Semaphorins是一个由分泌型和跨膜糖蛋白组成的大家族,最初被认为是神经回路发育过程中指导轴突生长的关键因素。最近的研究揭示了Semaphorins在多种免疫反应中的不同功能,包括免疫细胞的激活、分化、迁移和细胞间相互作用,这些功能依赖于它们在特定生物学环境中的跨膜受体和共受体。此外,越来越明显的是,如neuropilin(NRP)和plexins等Semaphorin受体对免疫系统的功能有积极贡献。NRPs是一种多功能单次跨膜糖蛋白,缺乏酪氨酸激酶活性,最初被确定为VEGF和III类Semaphorins的共受体。具体而言,NRP1和NRP2分别与VEGFRs和plexins相互作用。越来越多的研究表明,NRPs对各种T细胞亚群的发育、激活和功能具有深远影响,在维持正常免疫系统的稳态以及病理条件下起着至关重要的作用。
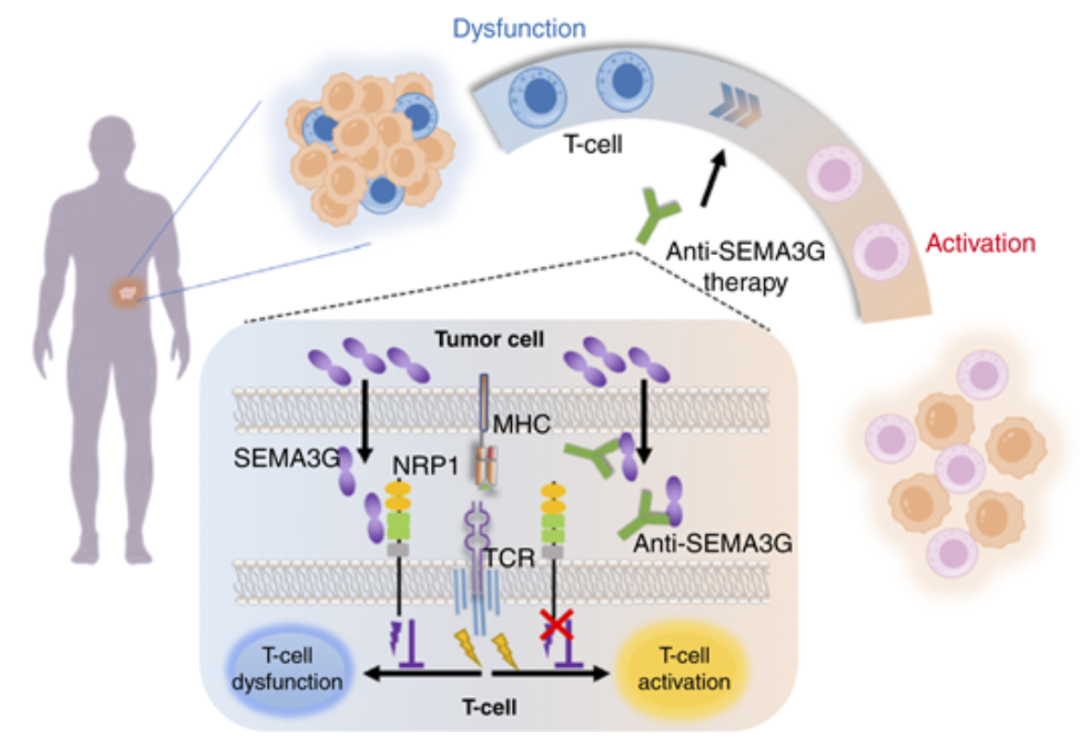
模式机理图(图片源自Cancer Research)
2005年,Semaphorin 3G(SEMA3G)被克隆并最初被鉴定为交感神经轴突的排斥因子,随后确定其参与多种生理和病理过程。值得注意的是,SEMA3G已成为成人胶质瘤的重要预后标志物。Shoda及其同事已经证明了SEMA3G在滑膜内巨噬细胞积聚和增殖中的调节作用,从而影响关节炎的进展。此外,据报道,SEMA3G通过抑制ERK和NF-κB信号通路来减弱炎症细胞因子。多项研究表明,SEMA3G与NRP2结合,从而激活相关的下游通路。多种Semaphorins之间共享的NRP和plexin成员突显了Semaphorin信号传导的复杂性。然而,全面探讨SEMA3G与肿瘤免疫监视之间的作用、机制和相互作用的研究仍然难以捉摸。
在本研究中,作者表明,在多种癌症类型中,SEMA3G的过度表达与T细胞功能障碍和肿瘤进展呈正相关。作者提出了一个假设,即肿瘤分泌的SEMA3G作为一种配体,阻碍T细胞的激活和功能。通过全面的受体增殖和功能分析,作者发现SEMA3G与NRP1的结合亲和力显著高于NRP2,随后抑制T细胞功能。这些发现为开发有效的免疫治疗策略提供了潜在的目标。
原文链接:
https://doi.org/10.1158/0008-5472.CAN-24-2223

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















肿瘤微环境中的T细胞通常表现出功能障碍特征,这些特征损害了它们引发先天性和治疗性诱导免疫反应的能力。免疫功能障碍的调节因子代表了激活抗肿瘤免疫的治疗靶点。
5
#免疫反应# #SEMA3G#
6