Lancet子刊:Maralixibat治疗进行性家族性肝内胆汁淤积症
昨天 xuyihan MedSci原创 发表于陕西省
Maralixibat显著改善了进行性家族性肝内胆汁淤积症患者的瘙痒症状,并降低了预测肝移植需求的关键指标(如血清胆汁酸水平)。
进行性家族性肝内胆汁淤积症(Progressive familial intrahepatic cholestasis, PFIC)是一组常染色体隐性遗传疾病,其中最常见的类型是由BSEP基因缺陷引起的PFIC。这些疾病会导致胆汁形成受损、胆汁淤积以及瘙痒等症状,并可能最终发展为肝硬化和肝衰竭。由于目前针对PFIC的治疗选择有限,患者通常需要依赖肝移植以延长生命。然而,肝移植具有高风险和高成本的特点,因此开发非手术治疗方法显得尤为重要。Maralixibat是一种回肠胆汁酸转运蛋白抑制剂,能够阻断胆汁酸的肠肝循环,从而减少胆汁酸的积累并缓解相关症状。在之前的一项二期研究中,Maralixibat已被证明对PFIC患者具有一定的疗效。基于这些发现,本研究旨在通过一项大型随机对照试验进一步评估Maralixibat在各类型PFIC患者中的有效性和安全性。这项研究由来自加州大学的Alexander G. Miethke教授团队,于2024年7月在线发表于《The Lancet. Gastroenterology & Hepatology》期刊(IF:30.9)。

MARCH-PFIC是一项多中心、随机、双盲、安慰剂对照的三期临床试验,在欧洲、美洲和亚洲的16个国家共29个社区和医院中心开展。纳入标准为1-17岁患有PFIC且伴有持续性瘙痒(>6个月;筛选期最后4周早晨Itch-Reported Outcome [Observer; ItchRO(Obs)]评分平均≥1.5)以及生化异常或进展性肝病病理证据的患者。研究定义了三个分析队列:BSEP队列(主要队列):仅包括两等位基因、非截短的BSEP缺陷患者,排除低胆汁酸或波动性胆汁酸水平及既往胆道手术患者。全PFIC队列:将BSEP队列与FIC1、MDR3、TJP2或MYO5B缺陷患者合并,排除既往手术患者但不论胆汁酸水平。全队列:无任何排除条件。参与者按1:1比例随机分配至口服Maralixibat组(起始剂量142.5 μg/kg,逐步增加至570 μg/kg,每日两次)或安慰剂组,疗程26周。主要终点为BSEP队列基线至第15-26周期间晨间ItchRO(Obs)严重程度评分的平均变化。次要终点为BSEP队列基线至第18、22和26周总血清胆汁酸水平的平均变化。
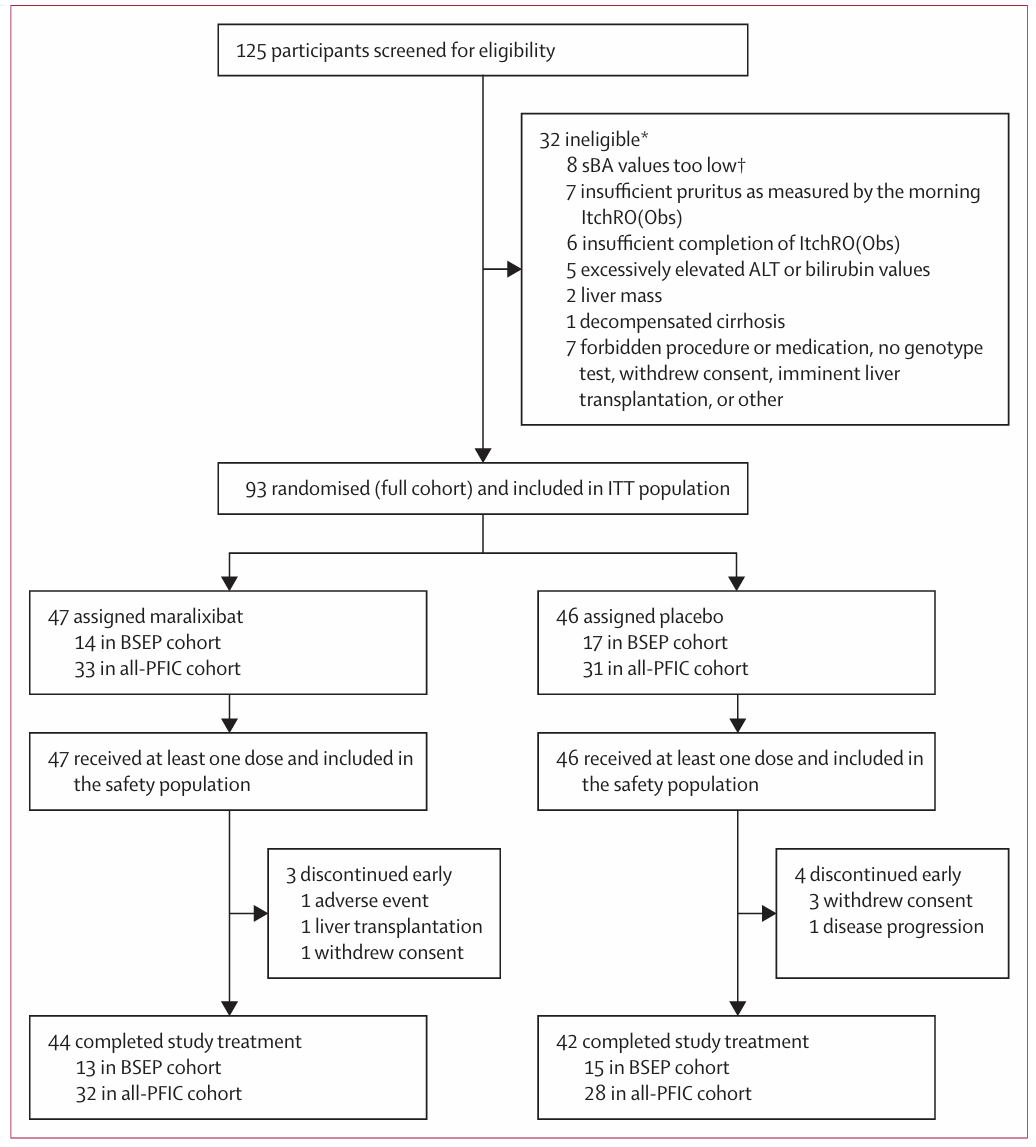
图1 该研究试验信息
共有125名患者被筛查,其中93名患者被随机分配至Maralixibat组(n=47;BSEP队列14人,全PFIC队列33人)或安慰剂组(n=46;BSEP队列17人,全PFIC队列31人),并接受了至少一剂研究药物,进入意向治疗和安全性人群分析。患者的中位年龄为3.0岁(IQR 2.0-7.0),其中女性51人(55%),男性42人(45%)。在BSEP队列中,Maralixibat组晨间ItchRO(Obs)评分的最小二乘均值变化为-1.7(95% CI -2.3至-1.2),而安慰剂组为-0.6(95% CI -1.1至-0.1),组间差异显著,为-1.1(95% CI -1.8至-0.3;p=0.0063)。同样在BSEP队列中,Maralixibat组总血清胆汁酸水平的最小二乘均值变化为-176 μmol/L(95% CI -257至-94),而安慰剂组为11 μmol/L(95% CI -58至80),组间差异显著,为-187 μmol/L(95% CI -293至-80;p=0.0013)。最常见的不良事件是腹泻,Maralixibat组发生率为57%(27/47),安慰剂组为20%(9/46),均为轻度或中度且大多为短暂性。Maralixibat组有5例(11%)患者出现严重治疗相关不良事件,安慰剂组为3例(7%)。未发生与治疗相关的死亡。
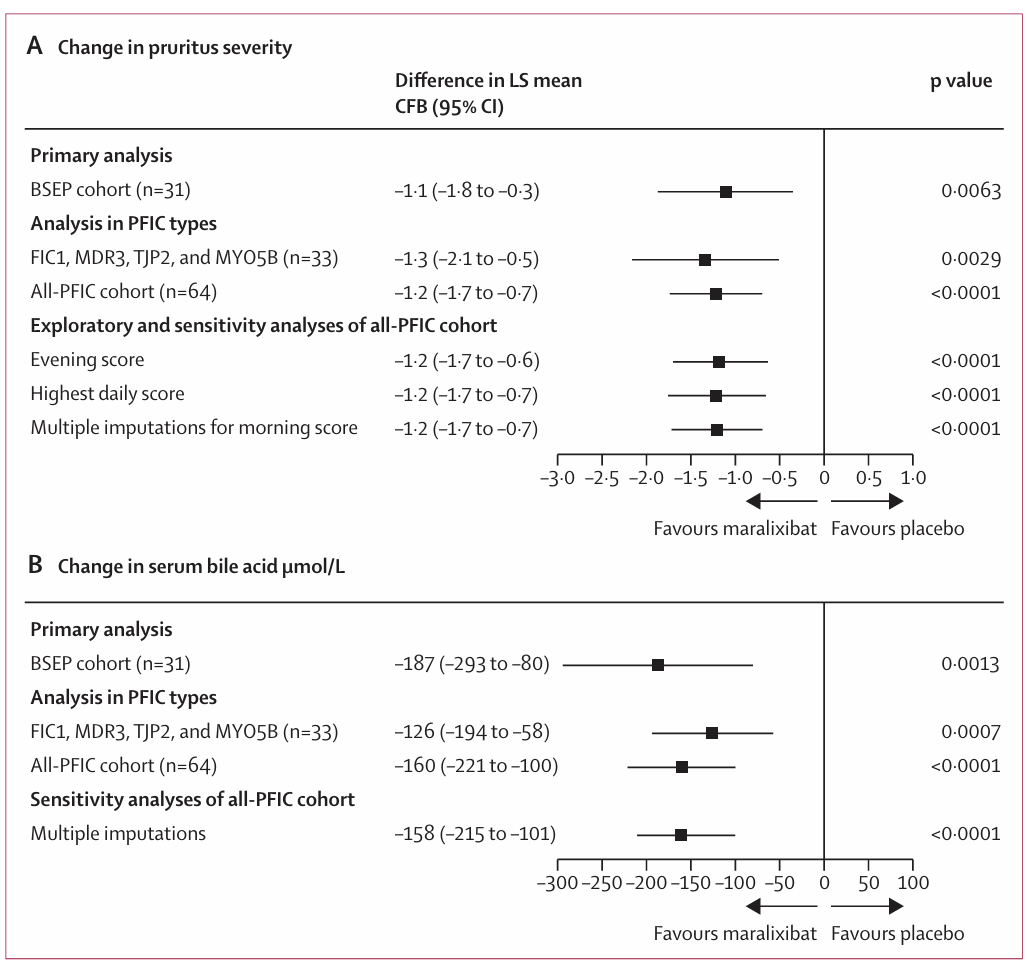
图2 意向治疗人群的疗效
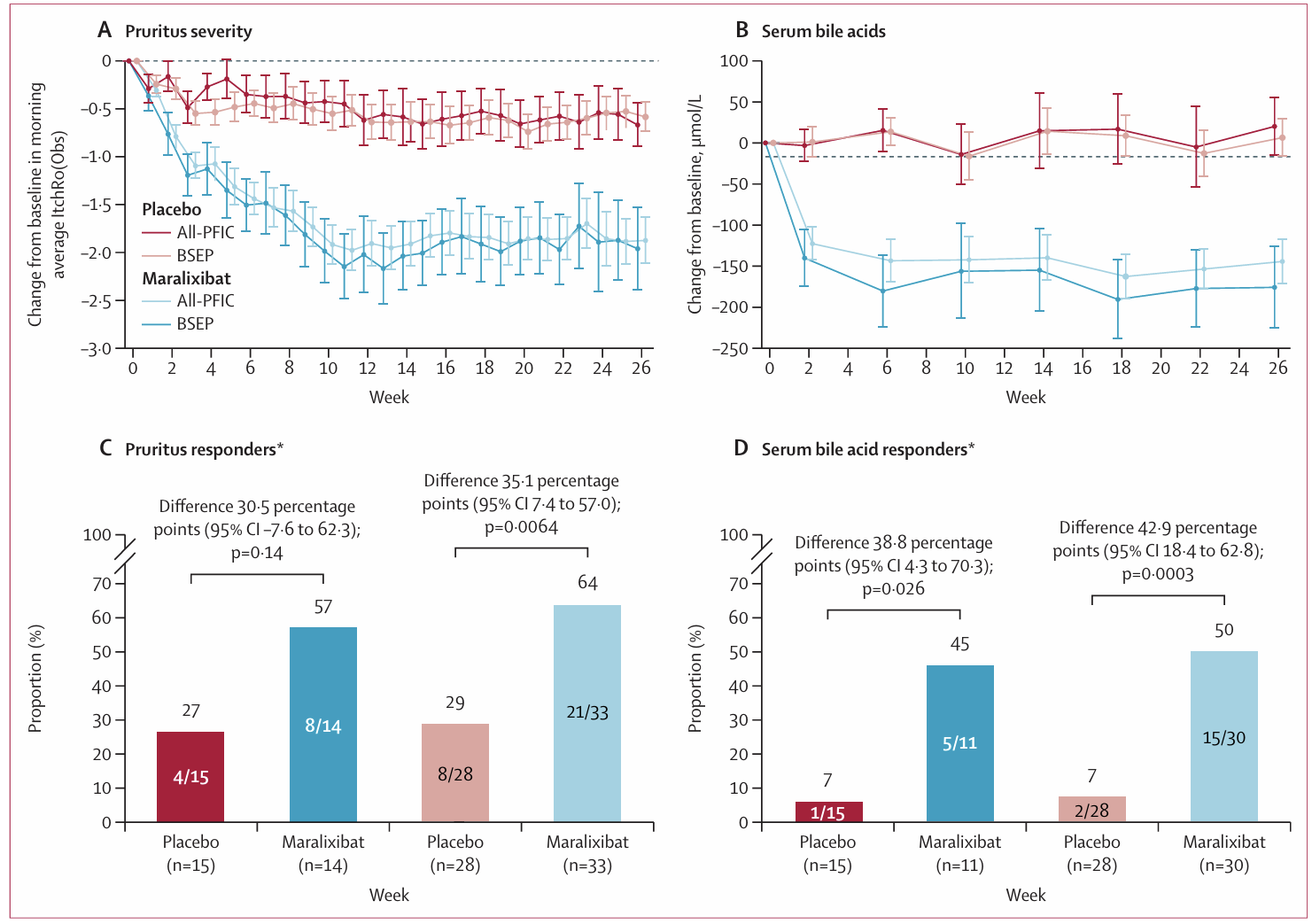
图3 瘙痒严重程度,血清胆汁酸,26周后反应
这项研究的结果表明,Maralixibat显著改善了PFIC患者的瘙痒症状,并降低了预测肝移植需求的关键指标(如血清胆汁酸水平)。Maralixibat作为一种非手术的药物治疗选择,能够有效干预胆汁酸的肠肝循环,从而改善PFIC患者的生活质量。此外,Maralixibat的不良事件主要为轻度至中度的胃肠道症状,且并未观察到严重的安全性问题,进一步证明其良好的耐受性。
原始出处:
Miethke AG, Moukarzel A, Porta G, Covarrubias Esquer J, Czubkowski P, Ordonez F, Mosca A, Aqul AA, Squires RH, Sokal E, D'Agostino D, Baumann U, D'Antiga L, Kasi N, Laborde N, Arikan C, Lin CH, Gilmour S, Mittal N, Chiou FK, Horslen SP, Huber WD, Jaecklin T, Nunes T, Lascau A, Longpre L, Mogul DB, Garner W, Vig P, Hupertz VF, Gonzalez-Peralta RP, Ekong U, Hartley J, Laverdure N, Ovchinsky N, Thompson RJ. Maralixibat in progressive familial intrahepatic cholestasis (MARCH-PFIC): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Gastroenterol Hepatol. 2024 Jul;9(7):620-631. doi: 10.1016/S2468-1253(24)00080-3. Epub 2024 May 6. Erratum in: Lancet Gastroenterol Hepatol. 2024 Jul;9(7):e10. doi: 10.1016/S2468-1253(24)00169-9. PMID: 38723644.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#进行性家族性肝内胆汁淤积症# #Maralixibat#
7