JAMA | 免疫治疗在头颈部鳞癌中的挑战:阿替利珠单抗维持治疗未能达到预期效果
2025-03-26 daikun MedSci原创 发表于陕西省
该研究旨在评估阿替利珠单抗在高危LA SCCHN患者中的维持治疗效果,IMvoke010试验未能证明阿替利珠单抗在高危LA SCCHN患者中维持治疗可以改善临床结局。
头颈部鳞状细胞癌(SCCHN)是全球第六大常见癌症,每年约有90万新发病例和50万死亡病例。该病通常涉及口腔、口咽、喉和下咽的黏膜衬里。高危局部晚期SCCHN(LA SCCHN)患者的治疗选择有限,通常包括手术、放疗和化疗的组合,随后进行常规监测以发现局部复发或远处转移。尽管如此,患者的预后仍然不佳,5年总生存率约为40%至50%,约50%的患者在完成根治性治疗后出现复发。因此,迫切需要改进的治疗方案来提高这些患者的生存率和生活质量。近年来,免疫检查点抑制剂(ICIs)在复发或转移性SCCHN的治疗中显示出一定的疗效,特别是针对程序性死亡配体1(PD-L1)和程序性死亡1(PD-1)的靶向治疗。阿替利珠单抗(atezolizumab)是一种抗PD-L1的单克隆抗体,通过阻断PD-L1与其受体(PD-1和B7.1)的结合,重新激活被抑制的T细胞以杀死癌细胞。尽管在晚期或难治性SCCHN患者中显示出一定的抗肿瘤活性,但在高危LA SCCHN患者中,阿替利珠单抗的维持治疗效果尚不明确。

方法
IMvoke010是一项全球性、双盲、安慰剂对照的III期随机临床试验,旨在评估阿替利珠单抗在高危LA SCCHN患者中的维持治疗效果。研究于2018年4月3日至2020年2月14日期间在23个国家的128个研究中心招募患者,临床截止日期为2023年9月27日。符合条件的患者在接受多模式根治性治疗后无疾病进展,包括口腔、口咽、下咽或人乳头瘤病毒(HPV)阴性或HPV阳性的口咽癌,或III期HPV阳性的口咽癌。患者被随机分配(1:1)接受每3周一次的阿替利珠单抗1200 mg或安慰剂,持续1年或直至疾病复发、疾病进展、不可接受的毒性或同意撤回。研究的主要终点是研究者评估的无事件生存期(EFS),定义为从随机化到第一次记录的疾病复发、疾病进展或任何原因导致的死亡的时间。次要终点包括总生存期(OS)和安全性的评估。
研究结果
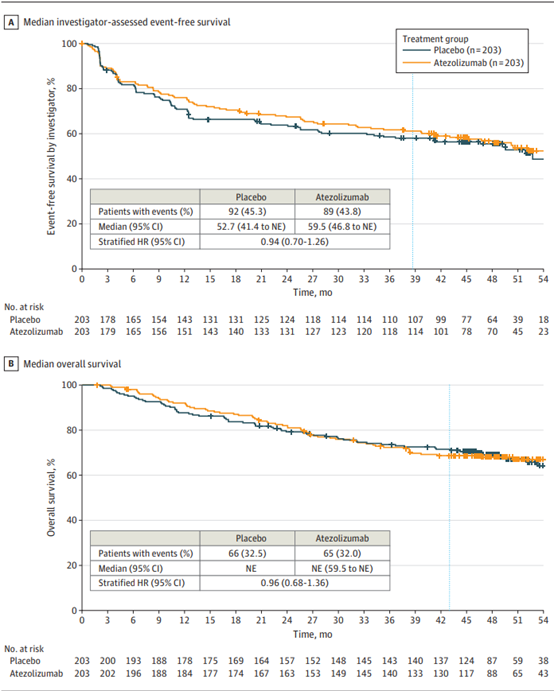
在406名随机分配的患者中,阿替利珠单抗组和安慰剂组在基线人口统计学和疾病特征上保持平衡。在中位随访46.5个月时,阿替利珠单抗组的中位无事件生存期为59.5个月,而安慰剂组为52.7个月,风险比为0.94(95% CI,0.70-1.26;P=0.68),未达到统计学显著性。两组之间的总生存期也无显著差异,24个月的总生存率分别为82.0%和79.2%。
安全性分析
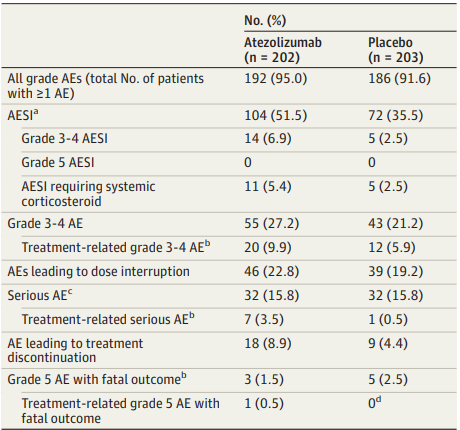
阿替利珠单抗的安全性与已知的药物安全性概况一致,未发现新的安全性信号。最常见的免疫相关不良事件包括免疫介导的甲状腺功能减退(60.7% vs 37.1%)、免疫介导的皮疹(15.8% vs 3.8%)和免疫介导的肝炎(13.4% vs 7.9%)。这些结果表明,阿替利珠单抗在维持治疗中的耐受性良好,尽管存在一些免疫相关不良事件的风险。
结论
IMvoke010试验未能证明阿替利珠单抗在高危LA SCCHN患者中维持治疗可以改善临床结局。尽管阿替利珠单抗在晚期或难治性SCCHN患者中显示出一定的疗效,但在高危LA SCCHN患者中,阿替利珠单抗的维持治疗效果并不显著。未来的研究应继续探索其他免疫治疗策略或联合治疗方案,以提高这些患者的生存率和生活质量。
原始出处
Haddad RH, Fayette J, Teixeira M, Prabhash K, Mesia R, Kawecki A, et al. Atezolizumab in High-Risk Locally Advanced Squamous Cell Carcinoma of the Head and Neck: A Randomized Clinical Trial. JAMA. 2025;323(10):955-965. doi:10.1001/jama.2025.1483.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#头颈部鳞状细胞癌# #阿替利珠单抗#
6