Nat Commun:准确性达93.7%!高度自动化临床mNGS检测可快速识别病毒性呼吸道病原体
2024-11-28 测序中国 测序中国
研究团队开发并临床验证了一种高度自动化的mNGS检测方法,从样本到结果的周转时间少于24小时,可用于识别常见和/或新型病毒性呼吸道病原体。
呼吸道感染是全球最常见的感染之一。由于潜在病原体的多样性,由病毒引起的呼吸道感染尤其难以诊断。近年来,新出现的大流行病毒是一种不可预测的健康威胁,而核酸扩增试验等传统工具并不能检测到这类病毒。当前亟需可快速识别新型和/或新发病毒的工具,以应对不明原因感染的临床诊断并为病毒大流行做准备。
新一代宏基因组测序(mNGS)是一种全面且无偏倚的诊断方法,颇具临床应用前景,可用于鉴定不明原因感染的病原体;无需特定引物和探针,只需一次检测即可鉴定所有潜在病原体。目前,mNGS已广泛用于多种样本类型的感染诊断,但由于成本高、方案复杂、缺乏自动化、周转时间过长和灵敏度较低等局限,其在临床微生物学实验室的普及中受到阻碍。
近日,美国加州大学旧金山分校的科研人员在Nature Communications发表了题为“Laboratory validation of a clinical metagenomic next-generation sequencing assay for respiratory virus detection and discovery”的文章。研究团队开发并临床验证了一种高度自动化的mNGS检测方法,从样本到结果的周转时间少于24小时,可用于识别常见和/或新型病毒性呼吸道病原体。与金标准临床多重RT-PCR检测相比,该自动化mNGS检测的病毒载量定量具有100%线性、灵敏度为93.6%、特异性为93.8%、准确性可达93.7%。此外,研究团队还在mNGS检测病原体所用的SURPI+自动化数据分析管道中纳入从头组装和翻译核苷酸算法,以发现具有大流行潜力的新型、序列差异较大的人类病毒。综上,这种高精度、快速的自动化mNGS检测方法能够增强新型病毒检测能力,有助于为病毒大流行做好强有力的准备和快速响应。

文章发表在Nature Communications
主要研究内容
1 开发、优化mNGS检测方法
新的自动化mNGS检测方法可用于检测呼吸道分泌物中的病毒病原体,包括上呼吸道拭子和支气管肺泡灌洗(BAL)液样本。基于在脑脊液中检测病原体的7年临床mNGS检测经验,研究团队通过优化样本品制备和生物信息学分析方案,提高了该方法灵敏度并缩短样本到结果的周转时间。在总核酸提取之前,单独离心可以产生最高的检测病毒reads产量;为减少周转时间,使用15分钟的人类rRNA耗尽方案,并将反转录和第二链cDNA合成步骤时间分别减少至15分钟和9分钟。最终检测使用450μL的进样量,样本到结果的周转时间为14-24小时。
此外,研究团队还将MS2噬菌体和外部RNA控制联盟(ERCC) RNA混合物分别添加到每个样本中作为内部定性和定量对照,并将定量的SARS-CoV-2、甲型流感、乙型流感、将呼吸道合胞病毒(RSV)加入到病毒阴性鼻咽拭子基质中,作为实验的外部阳性对照(PC),而来自健康未感染供者的病毒阴性鼻咽拭子作为外部阴性对照(NC)。
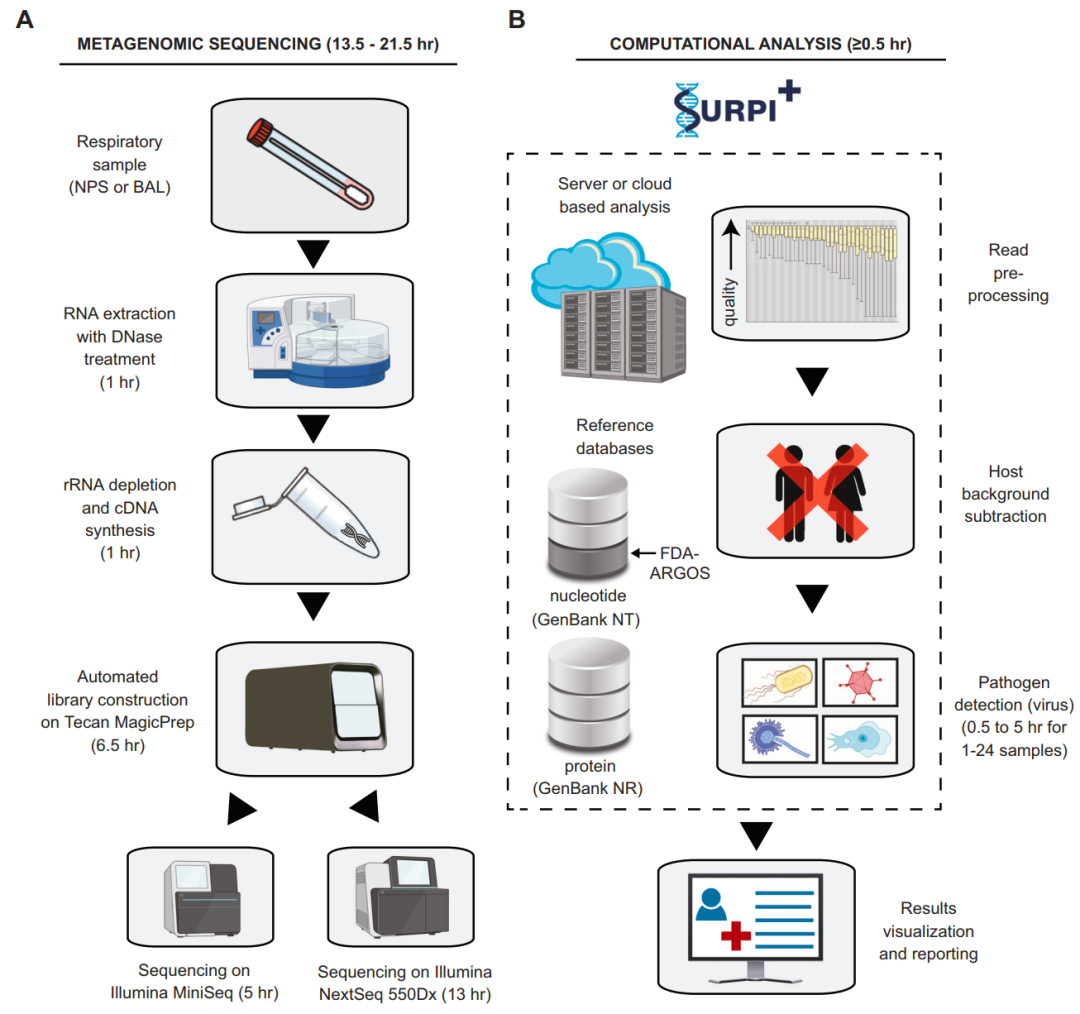
图1. mNGS检测流程示意图
SURPI+生物信息学分析管道用于从mNGS数据中识别病毒性呼吸道病原体,研究团队对其进行了三项优化以提高鉴定性能。
首先,增加了使用PC和ERCC为每个样本生成的标准曲线进行病毒载量定量的功能;使用标准化的ERCC结果为每个样本生成标准曲线,并通过比较ERCC数据和外部PC进行绝对定量。其次,在SURPI+数据库中“标记”Genbank的登记号,以便纳入病毒参考基因组,通过比对和结果报告进行病毒鉴定。最后,研究人员开发了一种定制算法,包括宏基因组reads的从头组装和翻译的核苷酸或氨基酸与病毒蛋白数据库的比对,以检测新的、序列高度分化的病毒。
研究团队还探讨了病毒载量浓度与感染严重程度之间的相关性,观察到无症状或轻度与中重度至重度感染患者之间的中位病毒载量存在显著差异,病毒载量浓度随着病症加重而增加;无症状、轻度和中重度感染之间中位病毒载量的成对差异也很显著。
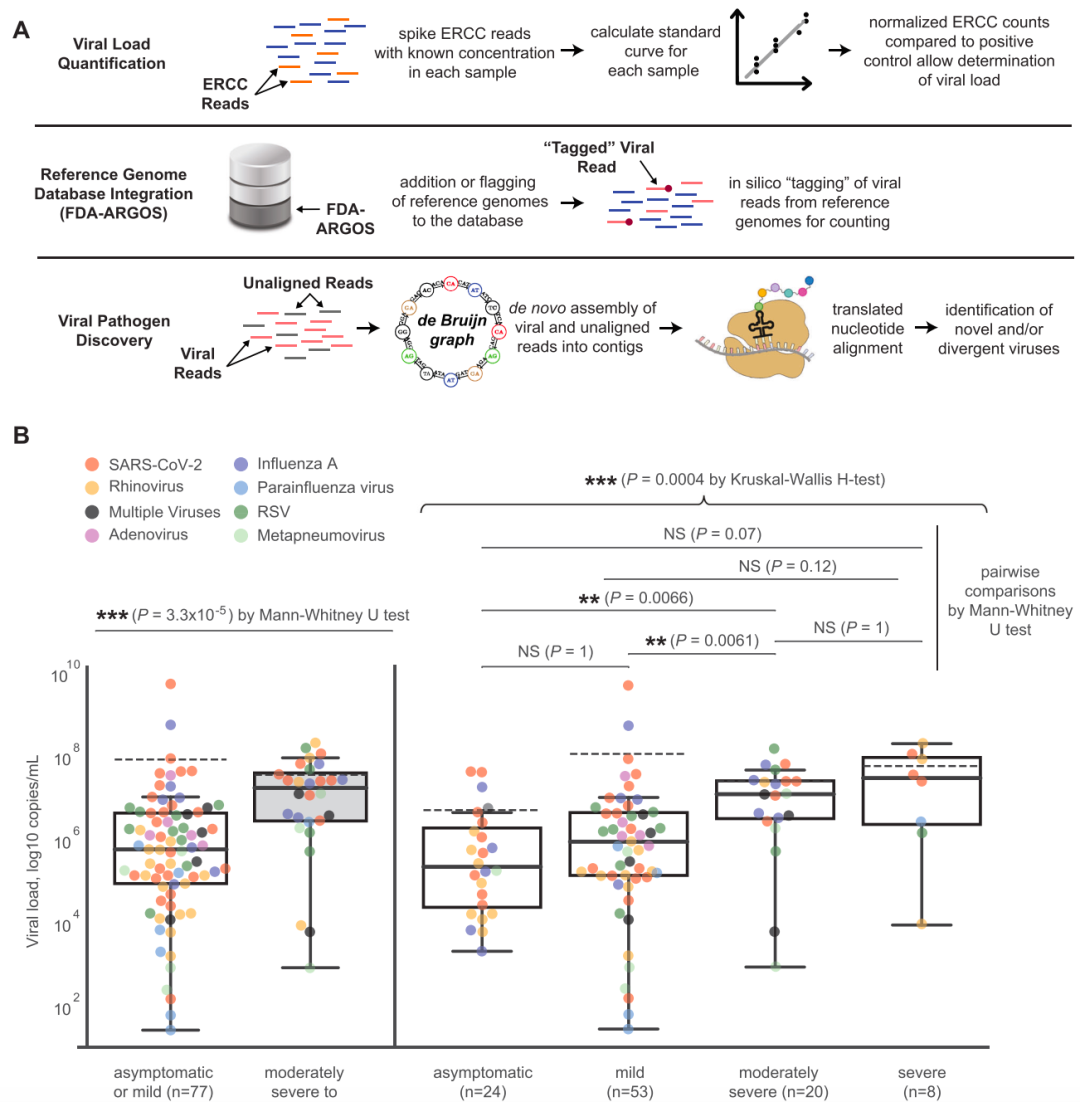
图2. 增强的SURPI+生物信息学分析管道用于病原体鉴定
2 mNGS检测方法性能评估
研究团队采用临床和实验室标准协会关于基于NGS的传染病检测(MM24)和多重核酸测定(MM24)的验证指南,对mNGS检测方法性能进行全面评估。
研究团队使用商业参考Panel以确定mNGS方法的检测限(LoD),其包含四种呼吸道病毒(SARS-CoV-2、甲型流感、乙型流感和RSV)。结果显示,四种呼吸道病毒的LoD范围为439-706拷贝/mL,平均LoD为550拷贝/mL,与特定逆转录聚合酶链反应(RT-PCR)检测病毒性呼吸道病原体的LoD相当。
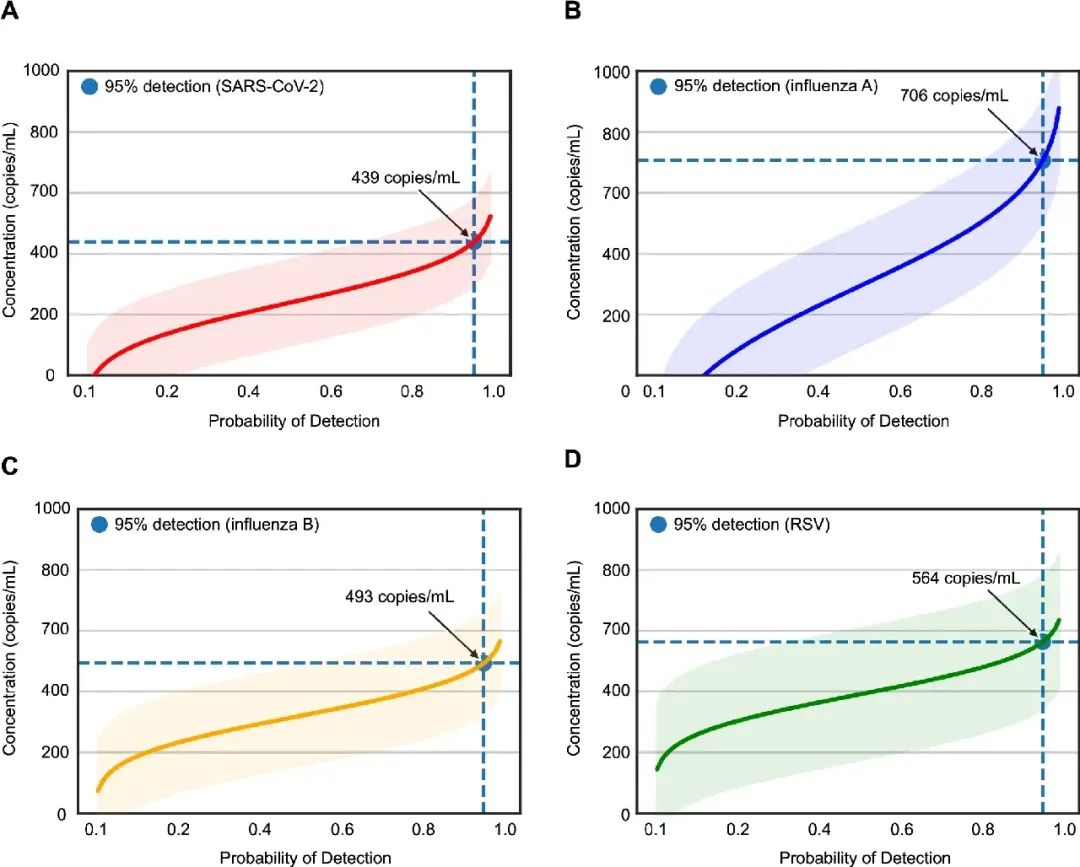
图3. mNGS检测的LoD
为评估mNGS准确定量检测病毒载量的能力,研究团队将定量高滴度SARS-CoV-2阳性鼻拭子样本进行5次对数稀释生成线性Panel,并与市售RNA线性Panel进行比较。经重复测试后,两个Panel的线性度均为100%。此外,通过在20次运行中使用不同条形码测试同一运行中的两个PC和两个NC样本测量了测定内精度,发现基本一致性(EA)为100%。
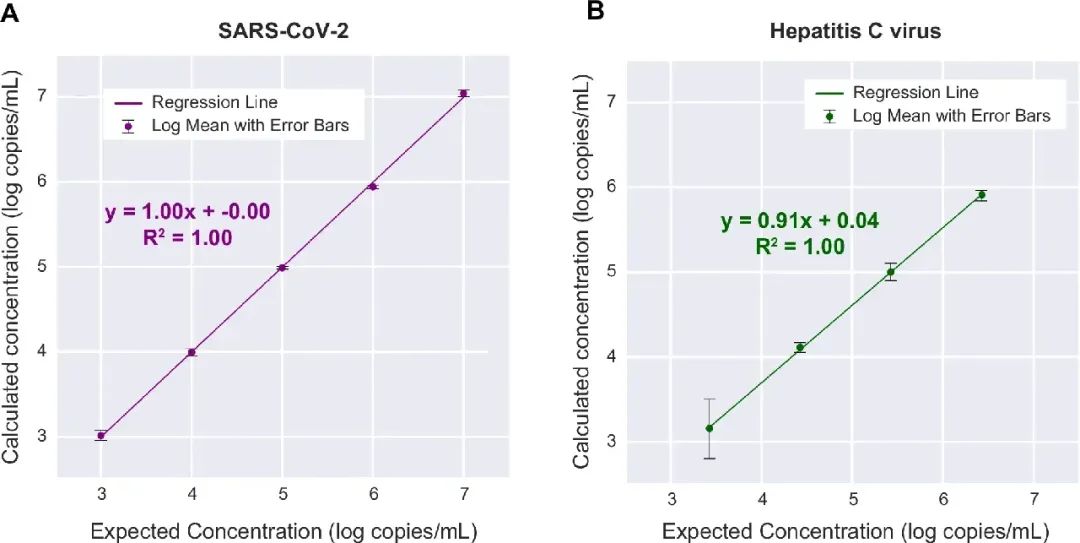
图4. mNGS检测的线性和病毒载量定量
为评估准确性,研究团队从加州大学旧金山分校临床微生物实验室获得191份常规临床检测后的残留样本,包括急性呼吸道感染患者的110份病毒阳性样本以及81个病毒阴性样本,使用mNGS对其进行深入分析。结果显示,与呼吸道病毒多重检测(RVP)金标准RT-PCR检测结果相比,自动化mNGS检测的灵敏度为93.6%,特异性为93.8%,准确性为93.7%。
随后,由两位委员会认证的传染病医生和加州公共卫生部病毒实验室对14份mNGS阳性-RVP阴性样本和7份mNGS阴性-RVP阳性样本进行审查及正交试验差异检测和临床判定(DTCA)。结果显示,mNGS方法检测性能优于RT-PCR,其总体一致性为97.9%,RT-PCR则为95.0%。
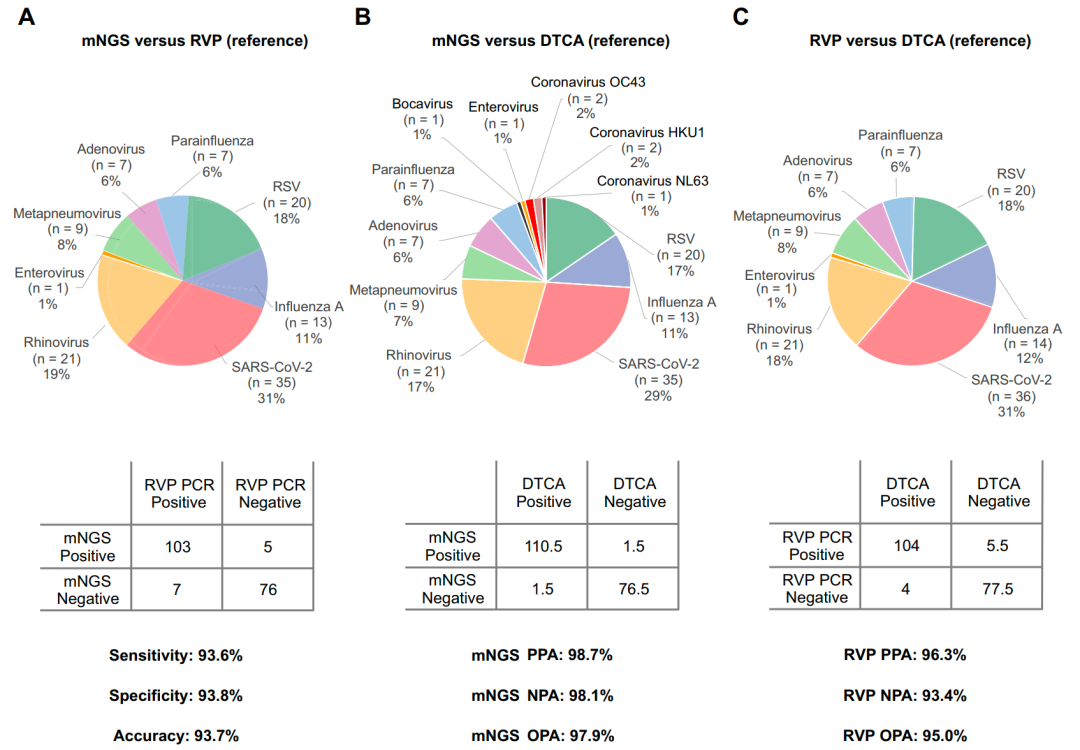
图5. mNGS检测方法的准确性
3 新型病毒检测能力评估
为测试改进的SURPI+分析管道检测新型、高度分化病毒的能力,研究团队创建了一个模拟测序输出文件,包含许多已知的人类病毒病原体以及具有大流行潜力的病毒病原体;从SURPI+参考数据库中剔除所有相同类型的病毒参考序列或对应的相同属或物种;使用SURPI+分析管道对原始和修正后的参考数据库分析模拟测序文件。
结果表明,基于与已知动植物病毒的同源性,98.6%的人类病毒在测序深度为100 reads per million(RPM)时被检测到,在1000 RPM时则可检测到100%的人类病毒。综上,与RVP等靶向检测相比,mNGS原则上能够检测呼吸道样本中所有已知的以及新型病毒病原体。

图6. 基于mNGS测定新型病毒的计算机演示
结 语
综上所述,研究团队开发、优化并在CLIA实验室验证了一种临床mNGS检测方法,这是一种实验室开发的检测方法(LDT),用于检测不可知的病毒性呼吸道病原体,旨在帮助患者诊断和公共卫生监测,能够在临床或公共卫生实验室中被常规部署和运行。与临床RVP检测相比,该mNGS检测方法具有良好的性能特征,已于2023年8月获FDA突破性设备认定。该研究证明了在临床和公共卫生实验室进行常规mNGS检测的可行性,有助于为病毒大流行做出强有力的快速反应。
论文原文:
Tan, J.K., Servellita, V., Stryke, D. et al. Laboratory validation of a clinical metagenomic next-generation sequencing assay for respiratory virus detection and discovery. Nat Commun 15, 9016 (2024).
https://doi.org/10.1038/s41467-024-51470-y
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








病毒性呼吸道病原体
19
#mNGS检测# #病毒性呼吸道病原体#
29