Mol Cancer:中南大学涂超等团队合作研究发表肿瘤微环境中焦亡和细胞因子的串扰:从机制到临床意义的综述
2024-12-03 iNature iNature 发表于陕西省
该综述深入探讨了细胞因子、焦亡和 TME 之间的复杂串扰,阐明了它们对肿瘤进展和转移的贡献。通过综合有关 TME 的新兴治疗靶点和创新技术,综述旨在提供新的见解,以改善癌症患者的治疗结果。
在癌症研究领域,肿瘤微环境 (TME) 在肿瘤的发生和发展中起着至关重要的作用,由癌细胞与周围非癌细胞之间的复杂相互作用形成。细胞因子作为必需的免疫调节剂,由 TME 内的各种细胞成分分泌,包括免疫细胞、癌症相关成纤维细胞和癌细胞本身。这些细胞因子促进了复杂的通信网络,从而显著影响肿瘤的发生、进展、转移和免疫抑制。
2024年11月30日,中南大学涂超,Xu Haodong,湖南大学王立明共同通讯在Molecular Cancer 在线发表题为“Crosstalk of pyroptosis and cytokine in the tumor microenvironment: from mechanisms to clinical implication”的研究论文。该综述深入探讨了细胞因子、焦亡和 TME 之间的复杂串扰,阐明了它们对肿瘤进展和转移的贡献。通过综合有关 TME 的新兴治疗靶点和创新技术,综述旨在提供新的见解,以改善癌症患者的治疗结果。
细胞焦亡通过促进促炎细胞因子的释放和维持慢性炎症来促进 TME 重塑,从而影响免疫逃逸和血管生成等过程。然而,由于细胞因子、细胞焦亡和 TME 之间复杂的相互作用,以及细胞焦亡对癌症进展和治疗相关并发症(如细胞因子释放综合征)的双重影响,挑战仍然存在。解开这些复杂性可以促进平衡炎症反应的策略,同时最大限度地减少治疗期间的组织损伤。

癌症是一系列以细胞增殖不受控制为特征的疾病,并受到遗传、环境和微环境因素多方面相互作用的影响。在肿瘤研究中,传统上主要关注癌细胞的内在特性,例如它们的增殖、凋亡和耐药机制。然而,越来越多的证据强调了将癌症视为一个复杂的进化和生态过程的必要性,其中包括癌细胞与肿瘤微环境 (TME) 之间的广泛相互作用。TME 构成了一个动态和支持环境,包括各种细胞和非细胞成分,包括基质细胞,如癌症相关成纤维细胞 (CAF)、免疫细胞(如巨噬细胞和中性粒细胞)、内皮细胞和细胞外基质 (ECM)。这种复杂的景观通过释放可溶性因子(如细胞因子和趋化因子)以及各种信号分子和 ECM 成分来促进癌症和非癌细胞之间的复杂通讯。
由 TME 内的不同细胞成分产生的细胞因子在调节肿瘤的发生、进展和转移中起关键作用。例如,CAF 释放各种细胞因子(例如 IL6)、趋化因子(例如 CXCL12)和生长因子(例如 LIF),这些细胞因子有助于维持促肿瘤微环境。肿瘤相关巨噬细胞 (TAM) 是细胞因子和趋化因子的重要来源,在慢性炎症的发生和持续中起关键作用,这与肿瘤发生和肿瘤进展密切相关 。TAMs分泌促炎细胞因子,如IL-1β、IL-6和IL-23,从而促进结直肠癌和其他恶性肿瘤的肿瘤生长和进展。此外,TAM 通过释放关键的促血管生成因子(包括血管内皮生长因子 (VEGF) 和 IL-8)来促进血管生成转换,这些因子可增强内皮细胞和其他支持血管网络发育的细胞的募集和激活。此外,TAM 有助于对靶向癌症治疗的适应性耐药。例如,TAM 来源的 TNF-α 作为关键的黑色素瘤生长因子,可诱导对 MAPK 通路抑制剂的耐药性。因此,了解细胞因子和其他信号分子之间错综复杂的串扰对于揭示癌症发展的免疫相关机制至关重要。这些知识可能导致针对 TME 的新型治疗策略,以破坏促进肿瘤的信号通路并增强抗肿瘤免疫力。
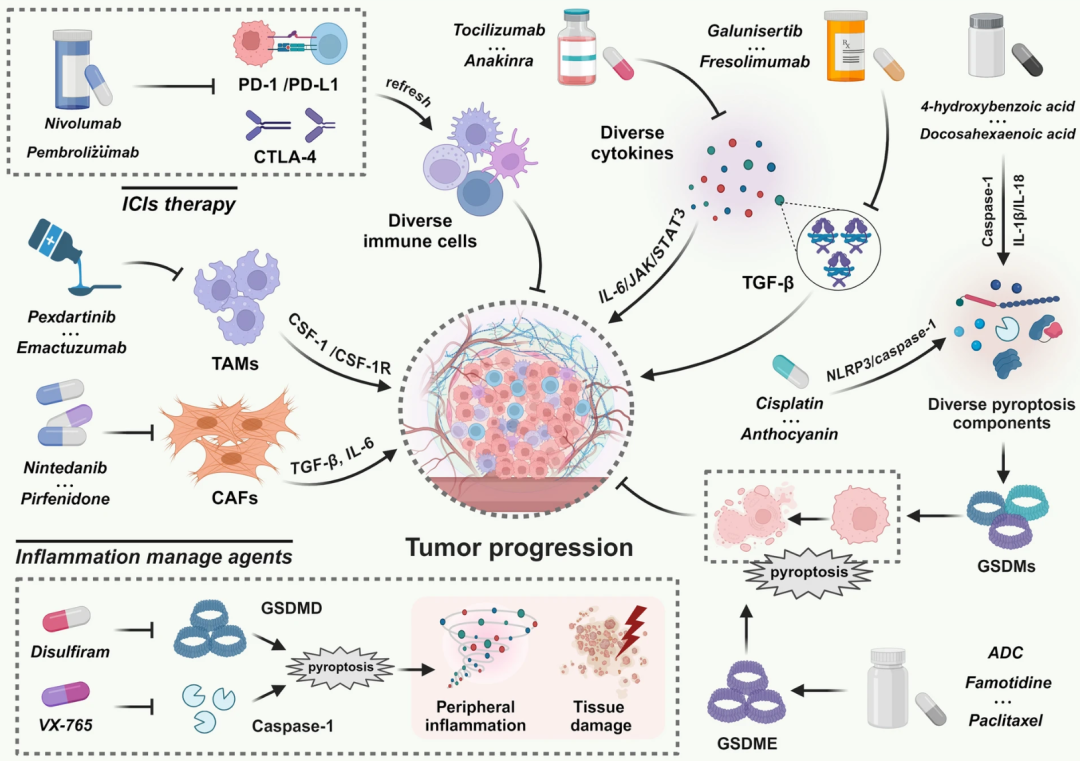
TME 的治疗靶点总结(图源自Molecular Cancer )
在多细胞生物中,保持细胞增殖和细胞死亡之间的微妙平衡至关重要。调节失衡可能导致细胞复制永生,从而随后导致肿瘤形成、进展,甚至治疗干预。在这些复杂的过程中,程序性细胞死亡 (PCD) 在维持内部平衡方面起着关键作用。细胞凋亡是研究最广泛的 PCD 方式,是对抗肿瘤的天然屏障;然而,化疗耐药性的出现限制了仅依赖于诱导细胞凋亡的传统疗法的疗效。因此,在解决细胞凋亡耐药性方面,探索针对非凋亡型 PCD 的新型治疗策略可能为癌症治疗提供有效的替代方案。细胞焦亡是一种由炎性小体激活的炎性 PCD。其特征是 gasdermin 家族蛋白的裂解,导致 IL-1β 和 IL-18 等细胞因子的释放。近年来,人们已经看到了对细胞死亡新模式的有希望的描述。然而,它们在 TME 中的作用及其潜在的临床应用需要进一步的研究和证实。
在过去的几十年里,各种形式的 PCD 得到了广泛的研究,包括坏死性凋亡、铁死亡和细胞焦亡。与坏死性凋亡和铁死亡相比,细胞焦亡是一种更普遍的免疫防御机制,与各种癌症中免疫细胞浸润到 TME 有着错综复杂的联系。此外,gasdermin 家族的多样性和炎性小体的复杂性有助于控制焦亡途径及其相关细胞因子的多方面调节网络。值得注意的是,尽管细胞焦亡在 TME 中具有积极作用,但一些研究报道了细胞因子释放综合征,这是一种由细胞焦亡介导的过度炎症反应引起的严重副作用。因此,总结肿瘤微环境中焦亡和细胞因子之间的精确机制和复杂相互作用对于开发更有效的抗癌疗法具有重要意义。
TME 内焦亡和细胞因子信号转导之间的相互作用形成了一个复杂的网络,其特征是许多通路和反馈回路。然而,潜在的分子机制仍不清楚。已知焦亡会放大炎症并改变 TME,增强细胞因子表达,从而促进癌细胞侵袭和转移。炎性细胞因子水平升高与癌症患者的不良预后有关,这凸显了它们作为有价值的预后标志物的潜力。然而,焦亡、细胞因子和肿瘤生长之间的关系是多方面的;虽然细胞焦亡可以促进促肿瘤的炎症并增强癌细胞的侵袭性,但它也可以刺激抑制肿瘤进展的抗肿瘤免疫反应。最近的研究强调了旨在诱导肿瘤细胞焦亡的治疗策略的潜力。通过触发这种形式的细胞死亡,可以激活免疫系统并增强抗肿瘤反应,从而为癌症治疗提供一条有希望的途径。细胞焦亡和细胞因子动力学的交集为创新疗法提供了机会,这些疗法可以调节 TME 中的炎症和免疫反应,从而可能克服与当前专注于细胞凋亡的疗法相关的限制。
综述简要概述了细胞因子和焦亡的基本原理和特征,并强调了它们各自的功能和 TME 的最新进展。此外,广泛讨论和阐明了 TME 中细胞因子和细胞焦亡之间错综复杂的串扰和联系,深入研究了调节对肿瘤发生、转移、免疫逃避和血管生成至关重要的网络的复杂分子机制。通过综合和总结抗肿瘤治疗中新兴的治疗靶点和新技术(例如单细胞测序和空间转录组学),希望提出新的见解,以推动未来的研究和临床应用,旨在改善肿瘤炎症和免疫生物学背景下的癌症治疗结果。
参考消息:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-024-02183-9
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#肿瘤微环境# #细胞因子#
7