IF:40.8!杭州市肿瘤医院,第一单位发STTT!
2024-11-11 BioMed科技 BioMed科技 发表于上海
本文综述 NK 细胞在多种生理病理过程中的作用、信号传导、分子机制及临床应用,强调癌症免疫治疗潜力,包括与肿瘤微环境相互作用及工程化 NK 细胞。
NK细胞的多重奏:免疫战场上的自然杀手和调节者
自然杀伤细胞(Natural Killer Cells, NK细胞)是免疫系统中的关键成员,它们在癌症、病毒感染、自身免疫性疾病、妊娠、伤口愈合等多种生理和病理过程中发挥着重要作用。NK细胞以其快速识别和清除病毒感染细胞和肿瘤细胞的能力而著称,它们通过分泌细胞因子如干扰素γ(IFNγ)和转化生长因子β(TGFβ)来调节免疫反应。
NK细胞最初被发现是因为它们能够无需预先致敏就能杀死某些肿瘤细胞和病毒感染细胞。随着研究的深入,科学家们逐渐揭示了NK细胞在免疫监视和免疫调节中的复杂作用。NK细胞起源于共同的淋巴样祖细胞,它们缺乏CD3、B细胞或T细胞受体,但通过穿孔素和颗粒酶等分子展现出强大的细胞毒性。
当前,NK细胞的研究正迅速发展,特别是在癌症免疫治疗领域。工程化的NK细胞,如嵌合抗原受体(CAR)-NK细胞,正在被开发用于针对性地杀死癌细胞。这些细胞在体外扩增和基因改造后,能够被重新输回患者体内,以增强对肿瘤的免疫攻击。此外,NK细胞在自身免疫性疾病和COVID-19治疗中的潜在作用也在研究之中。临床试验正在评估这些经过改造的NK细胞的安全性和有效性,以及它们在不同疾病中的实际应用。随着对NK细胞功能、信号传导和分子机制的深入了解,这些细胞有望成为未来治疗多种疾病的有力工具。
哈佛大学医学院附属麻省总医院Youssef Jounaidi、杭州市肿瘤医院Sumei Chen提供了关于NK细胞在多种生理和病理过程中的作用、信号传导、分子机制和临床应用的全面概述,特别关注了NK细胞在癌症免疫治疗中的潜力,包括它们与肿瘤微环境的相互作用、激活与抑制的复杂平衡,以及如何通过工程化NK细胞来增强其抗肿瘤活性。相关内容以“Comprehensive snapshots of natural killer cells functions, signaling, molecular mechanisms and clinical utilization”为题发表在《Signal Transduction and Targeted Therapy》上。

【主要内容】
NK细胞的研究历程
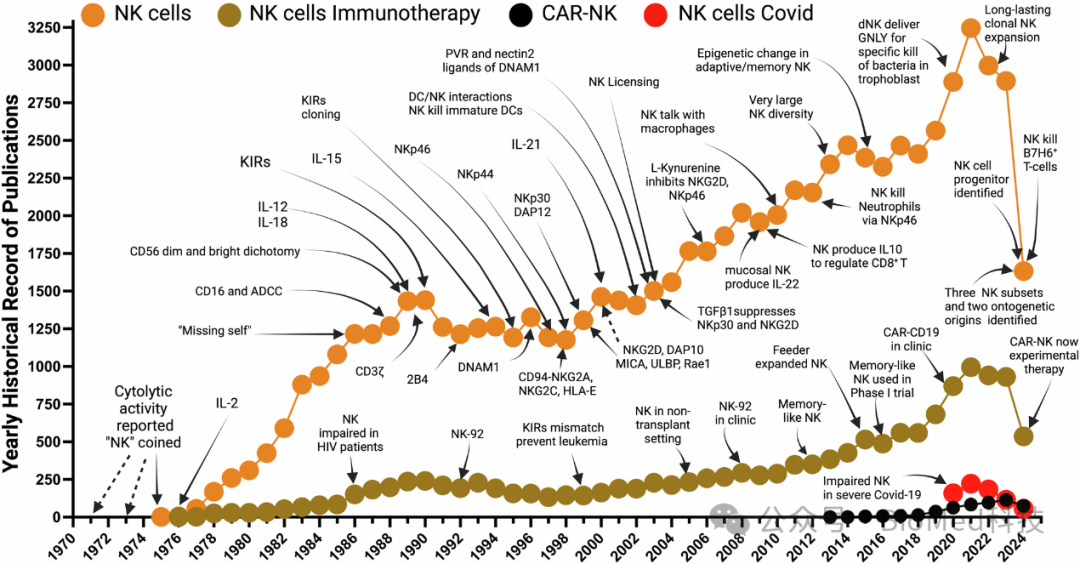
图1 NK细胞研究历程
该图通过关键词搜索,作者汇总了PubMed上关于NK细胞、NK细胞与免疫疗法、NK细胞与CAR-NK技术、以及NK细胞与新冠病毒的相关文献,呈现了从早期发现到CAR-NK细胞作为MD Anderson癌症中心治疗癌症的实验性治疗方案的演变过程。值得注意的是,与T细胞相关的研究文献数量远多于NK细胞,而CAR-NK领域的研究文献更是相对较少。
NK细胞识别致病细胞
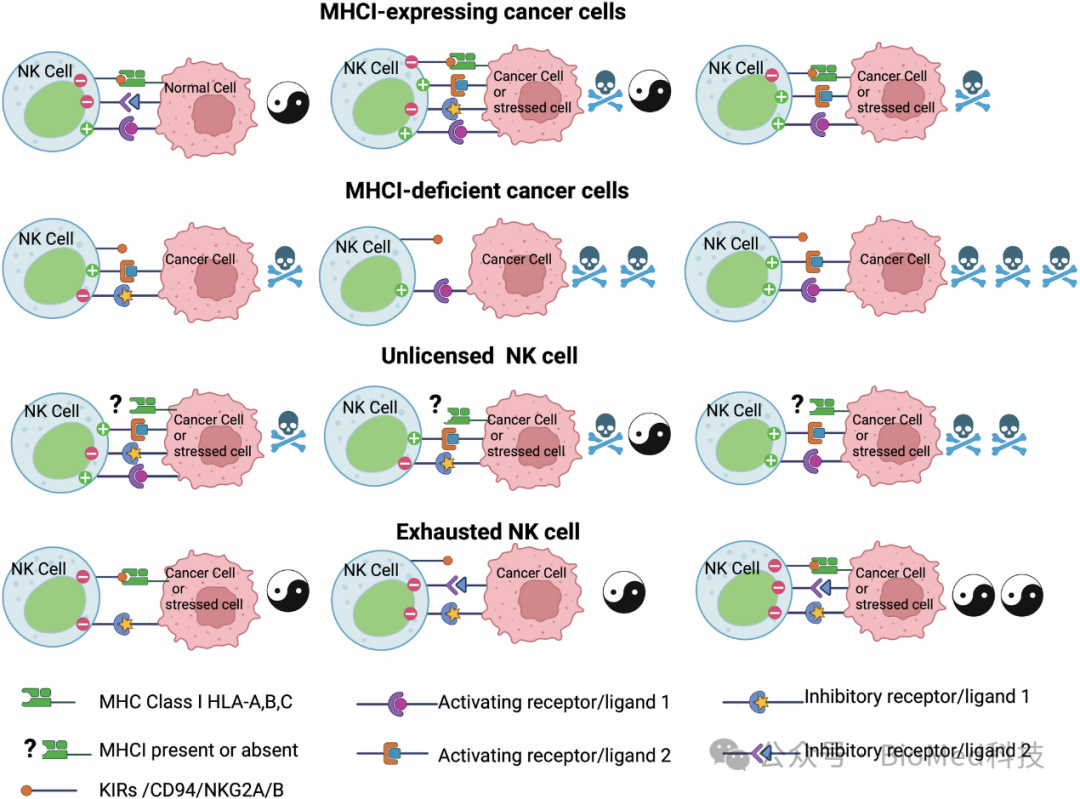
图2 MHC I分子与NK细胞上的抑制性和激活性受体相互作用
在正常情况下,NK细胞通过其抑制性受体如KIRs和CD94/NKG2A与MHC I分子结合,产生抑制信号,防止对正常细胞的杀伤。当目标细胞表达MHC I分子时,这些抑制信号占主导地位,NK细胞通常不会发动攻击。然而,癌细胞常常通过降低MHC I分子的表达来逃避T细胞的监视,但这种策略并不能有效地逃避NK细胞,因为NK细胞不依赖MHC I分子来识别目标。因此,缺乏MHC I分子的癌细胞更有可能被NK细胞通过“缺失自我”机制识别并杀伤。如果NK细胞因为弱激活或疲劳而对MHC I缺乏的癌细胞产生耐受,那么IL-18和IL-12等细胞因子可以逆转这种状态,恢复NK细胞的活性。未表达KIRs/CD94/NKG2A/B的NK细胞在杀伤MHC I表达正常的癌细胞时可能更为有效,因为它们不受MHC I抑制信号的影响。
NK细胞从出生到成熟
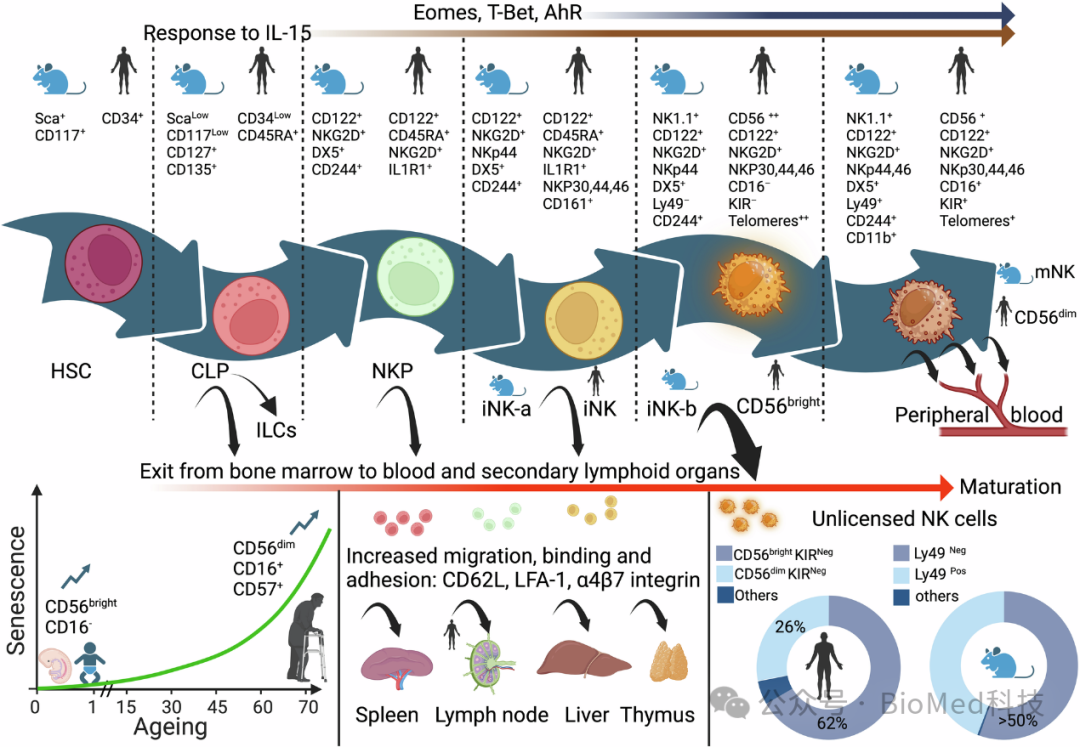
图3 NK细胞的发育和成熟过程
该图从CD34+的造血干细胞开始,追踪了NK细胞在骨髓中的成熟路径,直至发展成为具有完全功能的成熟NK细胞,表现为CD56阳性和CD16阳性。NK细胞的成熟过程伴随着对多种细胞因子受体的获得,包括对IL-15的响应、转录因子EOMES、T-bet和AhR的表达,以及抑制性受体KIRs和抗体介导的细胞毒性受体CD16的获取。NK细胞从共同淋巴样祖细胞(CLP)起源,通过早期NK祖细胞(ENKP)和先天淋巴细胞祖细胞(ILCP)的分化,形成不同的NK细胞亚群,包括CD56bright和CD56dim表型。
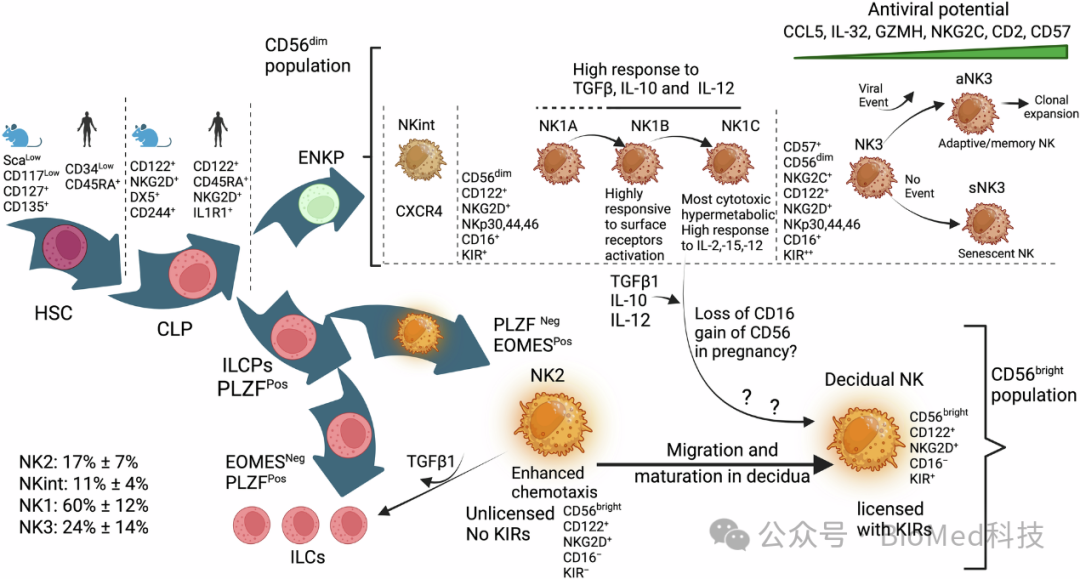
图4 NK细胞起源和成熟过程的示意图
该图展示了NK细胞从CLP起源,通过ENKP和ILCP两条不同的路径发展成熟。ENKP路径主要产生CD56dim表型的NK细胞,而ILCP路径则产生CD56bright表型的NK细胞以及其它先天淋巴细胞(ILCs)。图中还详细描绘了NK细胞在骨髓中的成熟过程,包括NK细胞前体(NKP)向不成熟的iNK细胞(分为iNK-a和iNK-b阶段)的转变,以及最终发展成为成熟NK细胞的不同阶段,如CD56bright和CD56dim表型。
NK细胞的信号调节通路
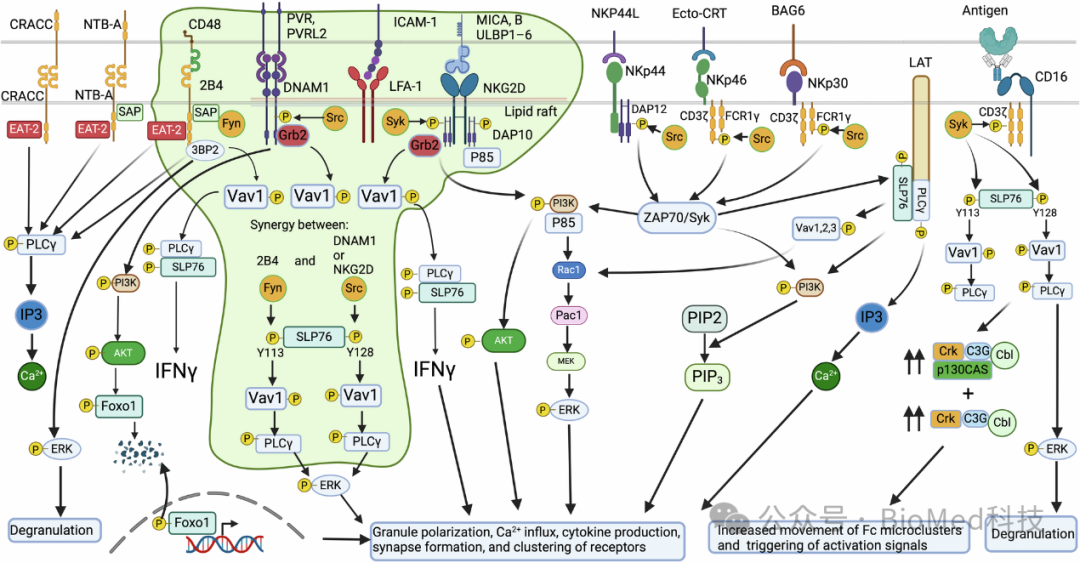
图5 NK细胞与癌细胞和应激细胞接触时的激活信号动态
图中展示了多种激活受体如何通过特定的信号传导途径促进NK细胞的激活。这些受体包括SLAM家族受体(如2B4、NTB-A和CRACC),它们在与配体结合后通过免疫受体酪氨酸基开关(ITSM)依赖的信号传导来激活NK细胞。此外,上图还展示了NKG2D受体如何与DAP10结合,以及DNAM-1受体如何通过与PVR或Nectin-2结合来激活NK细胞。这些激活信号涉及Src家族激酶、Syk激酶、PI3K、PLCγ、VAV和ERK等关键分子,最终导致颗粒极化、钙内流、细胞因子产生、突触形成和受体聚集,从而引发NK细胞的杀伤功能。
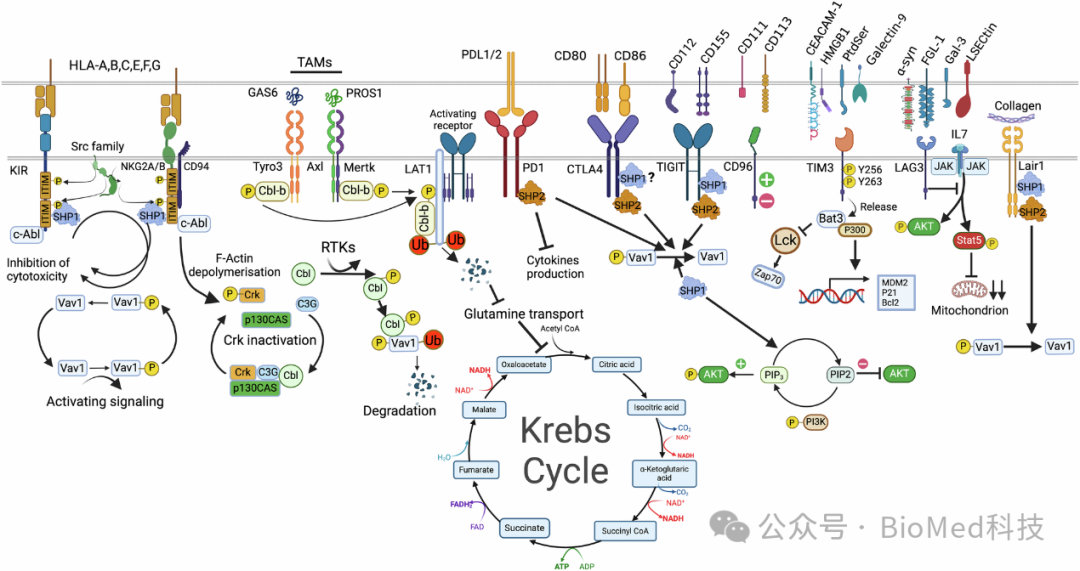
图6 NK细胞的抑制性信号传导路径
图中详细描述了抑制性受体如何通过不同的机制来抑制NK细胞的功能,包括MHC I特异性抑制受体通过SHP-1去磷酸化VAV1,以及Crk蛋白通过c-Abl介导的磷酸化而从c-Cbl/Crk/C3G和p130CAS/Crk/C3G复合体中解离。此外,上图还描绘了PD-1通过其内质网域信号招募SHP-2来抑制DNAM-1的磷酸化,以及TIGIT如何通过与PVR和DNAM-1竞争来增强抑制信号。这些抑制性信号的相互作用对于维持免疫系统的平衡至关重要,它们防止NK细胞过度激活,从而避免对正常组织的损伤。
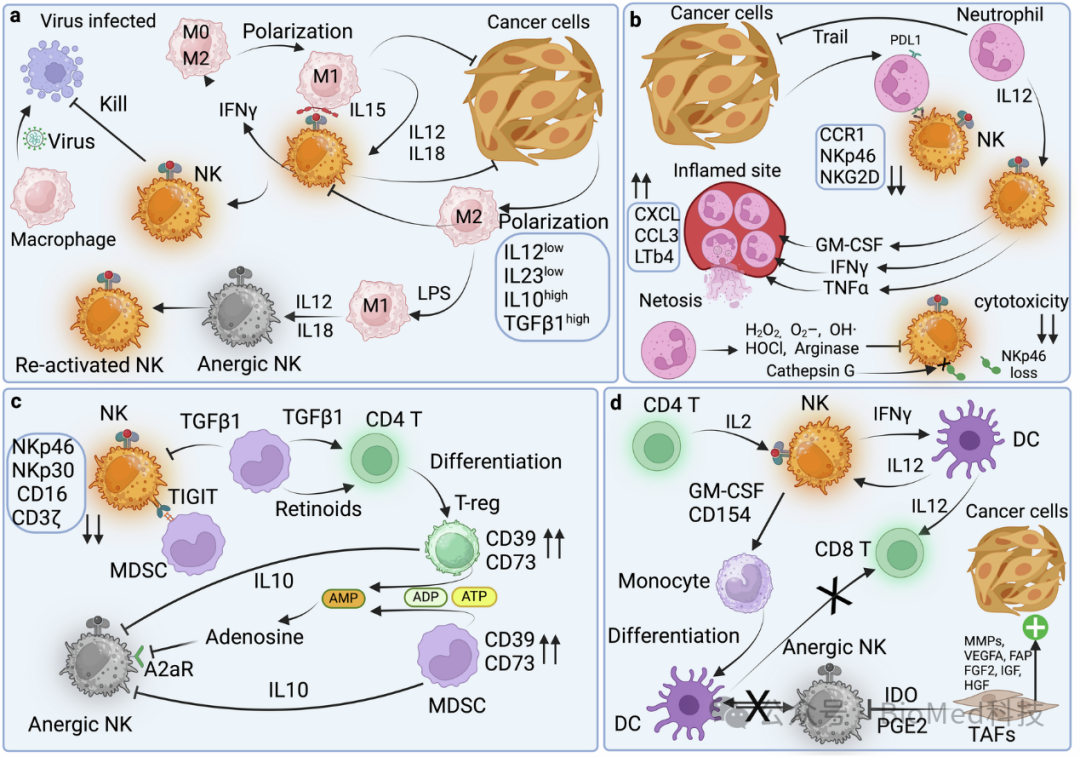
图7 NK细胞与其他免疫细胞之间的相互作用
图中详细描绘了NK细胞与巨噬细胞、中性粒细胞、髓系来源的抑制细胞(MDSCs)以及调节性T细胞(Tregs)之间的复杂关系。NK细胞通过分泌IFNγ等细胞因子激活巨噬细胞,促使它们向抗肿瘤的M1表型极化,同时,巨噬细胞通过分泌IL-12和IL-15增强NK细胞的活性。中性粒细胞通过TRAIL途径增强NK细胞的抗肿瘤作用,但也存在通过PD-L1途径抑制NK细胞的情况。MDSCs和Tregs在肿瘤微环境中通过多种机制抑制NK细胞的功能,包括直接接触、分泌TGFβ1和IL-10等免疫抑制因子。此外,上图还展示了T细胞与NK细胞之间的协作关系,其中IL-2激活的NK细胞能够通过IFNγ激活树突状细胞(DCs),进而促进CD8+ T细胞的抗肿瘤活性。
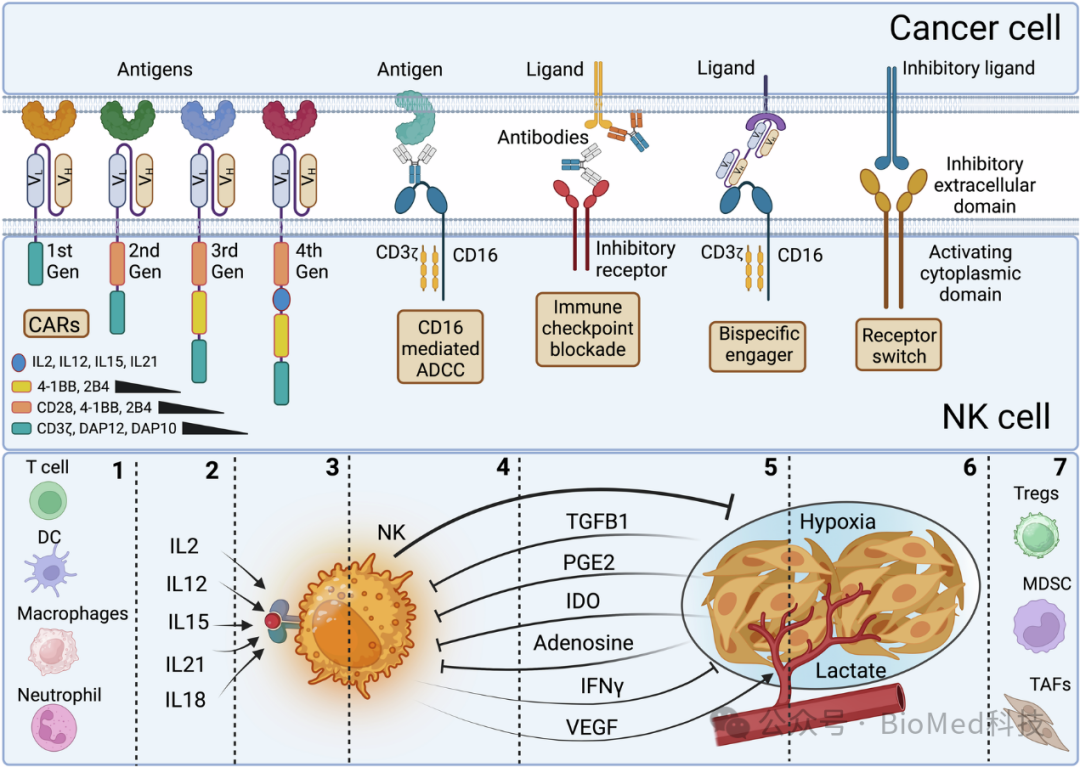
图8 通过多种策略武装和部署NK细胞以增强其抗肿瘤活性
图中概述了七个层次的干预措施,包括改善NK细胞与其他效应细胞如T细胞、树突状细胞(DCs)、巨噬细胞和中性粒细胞的协作;通过细胞因子信号武装NK细胞;工程化NK细胞以提高其持久性、代谢能力和抵抗疲劳的能力;预防TGFβ1、IDO、PGE2和腺苷等引起的免疫抑制;改善NK细胞进入肿瘤的能力;预防肿瘤血管生成和免疫抑制;减少MDSCs、Tregs和肿瘤相关成纤维细胞(TAFs)引起的免疫抑制。此外,上图还强调了通过嵌合抗原受体(CAR)技术、治疗性抗体、免疫检查点阻断、双特异性/三特异性引导剂以及将抑制信号转换为激活信号的策略来增强NK细胞的抗肿瘤反应。
环境影响NK细胞功能
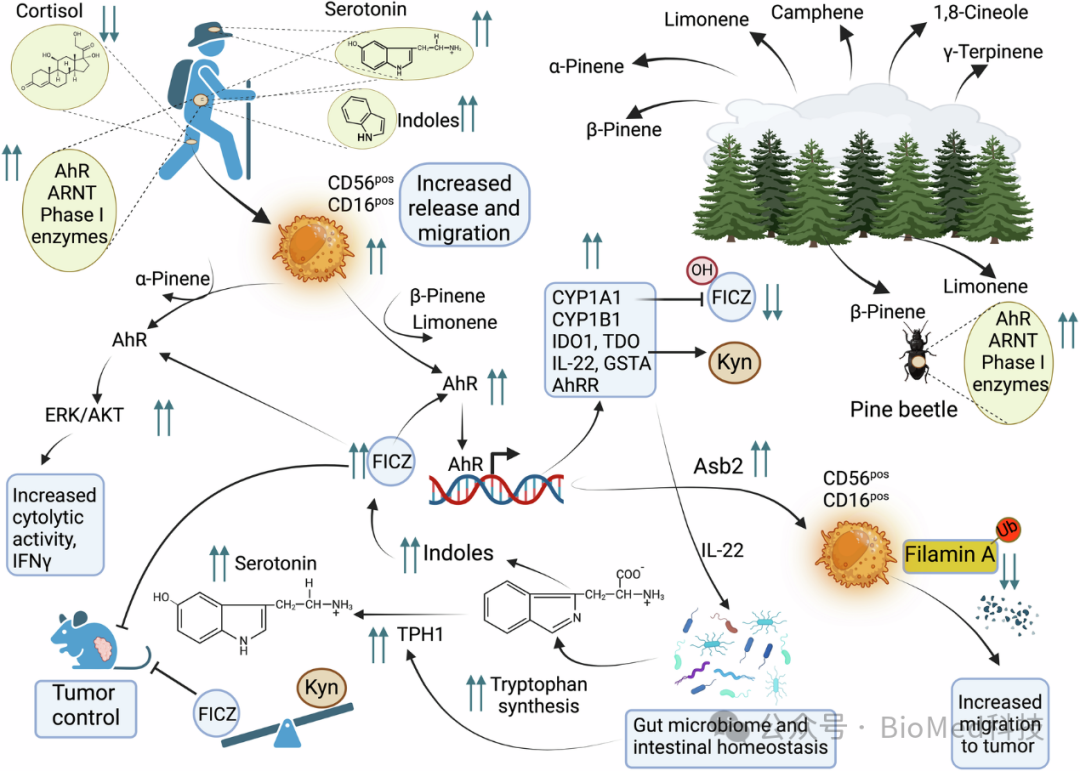
图9 环境因素对人类NK细胞功能的影响
图中阐释了森林环境中的植物挥发性化合物(如α-蒎烯)如何通过激活NK细胞内的ERK/AKT信号通路来增强其细胞毒性。此外,上图还揭示了芳香烃受体(AhR)和芳香烃受体核转运蛋白(ARNT)在感应环境化学物质并激活CYP1A1、IDO1、IL-22等基因表达中的作用。这些基因的激活有助于增强NK细胞的IFNγ产生和细胞毒性,从而更好地控制肿瘤。上图还提出了一个假设,即通过森林浴增加的IL-22可以促进肠道微生物群产生更多的色氨酸衍生物FICZ,这是一种强效的AhR配体,能够进一步增强NK细胞的功能。
【全文总结】
本文综述了自然杀伤(NK)细胞的多功能性、信号传导机制、分子调控途径以及在临床治疗中的应用,特别强调了NK细胞在癌症、病毒感染和自身免疫性疾病中的作用,以及如何通过工程化NK细胞来增强其抗肿瘤活性,同时探讨了NK细胞与其他免疫细胞的相互作用和在肿瘤微环境中的调节作用,为开发新的免疫治疗策略提供了科学依据。
原文链接:
https://doi.org/10.1038/s41392-024-02005-w
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#免疫治疗# #肿瘤微环境# #NK细胞#
5