雪上加霜 | 糖尿病与帕金森病:是巧合还是必然?
2025-01-05 神经科学论坛 神经科学论坛 发表于陕西省
2 型糖尿病与帕金森病密切相关,糖尿病患者帕金森病风险增高,二者在致病机制等方面有相似之处,调节糖代谢等或成治疗途径,但缺乏脑胰岛素抵抗临床评估标记物。
论坛导读:大约10%的成年人患有2型糖尿病(T2DM),1%的60岁以上的人口患有帕金森病(PD)。2型糖尿病和帕金森病是与影响老年人并造成重大社会经济负担相关的慢性疾病。支持这两种衰老相关疾病之间密切关系的流行病学数据导致了对共同病理生理学分子机制的研究。在过去的十年中,大脑中受损的胰岛素信号传递受到了越来越多的关注,并被认为通过几种病理过程的失调而促进了帕金森病的发展。
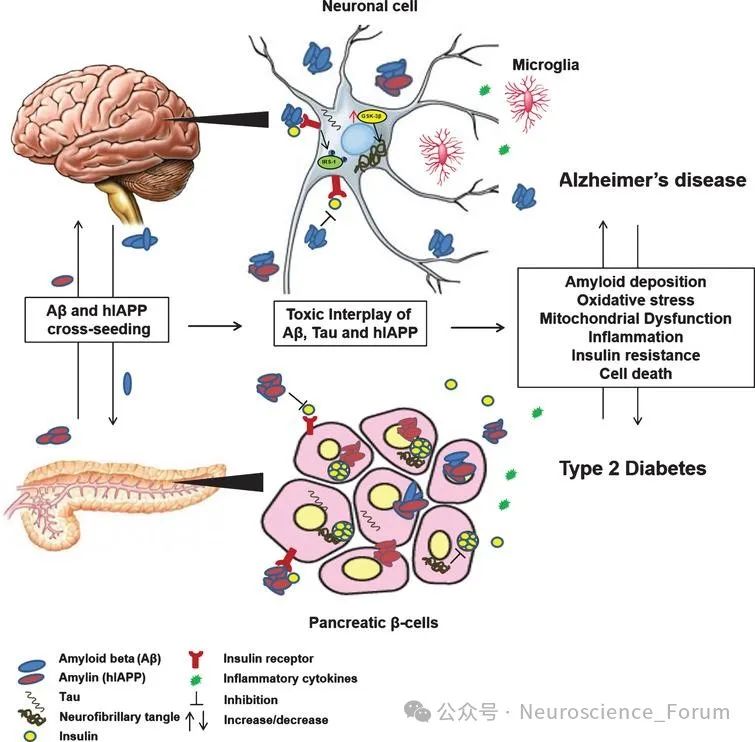
doi: 10.3233/JAD-161192.
帕金森病是一种常见的中老年人神经系统变性疾病,在60岁以上人群中患病率为1000/10万,并随年龄增长而增高。帕金森病会造成肢体活动紊乱,产生常见的肢体“僵、慢、颤”等症状,严重影响患者生活质量。帕金森病病因迄今未明,发病机制十分复杂。一项荟萃分析共入选了7个队列研究,包含1,761,632名受试者,研究结果发现,糖尿病患者的帕金森病风险明显增高,相对风险比为1.38。研究证实某些降糖药物可以带来神经保护作用。糖尿病已经被视为神经退行性变和帕金森病的促进因素,糖尿病患者中帕金森病的筛查应更加准确,并且帕金森病前驱症状中应包括糖尿病。
帕金森病和糖尿病都是与年龄相关的慢性疾病,会严重影响老年人的生活质量。从致病机制来看,糖尿病和帕金森病具有明显相似的细胞功能失调途径包括线粒体功能障碍、内质网应激、维生素D缺乏、炎症、脂质代谢功能障碍在两者中可能发挥作用,且这些因素可能导致代谢综合症和胰岛素抵抗,使患帕金森病的风险增加。
一项研究通过观察性研究的荟萃分析和遗传数据的孟德尔随机化分析两种不同的分析评估2型糖尿病和帕金森病之间的联系发现2型糖尿病与帕金森病风险增加有关,2型糖尿病或是帕金森病风险的驱动因素。研究者发现2型糖尿病与帕金森病发病风险增加21%有关,也和更快的症状进展相关。虽然该观察性研究并未证明糖尿病和帕金森病的因果关系,但是该结果让研究人员注意到这两种疾病的相关性。研究者进一步使用遗传数据来检查糖尿病和帕金森病的因果关系,结果发现2型糖尿病本身可直接增加患帕金森病的风险为8%。
循环中的胰岛素可能具有神经保护作用,而系统性和局部的胰岛素抵抗可以影响已知的帕金森病发病机制中重要的途径,包括与线粒体功能障碍、神经炎症、突触可塑性相关的途径。一项研究发现近2/3的PD患者(58.4%)具有未确诊的胰岛素抵抗,尽管空腹血糖正常,并且很多时候糖化血红蛋白(HbA1c)水平也正常。研究结果也证实了之前的发现,肥胖者的胰岛素抵抗是体型偏瘦人的两倍以上。除此之外,研究者还发现体型偏瘦PD患者胰岛素抵抗的比例更高(41%)。但是胰岛素抵抗与认知能力下降无关。脑胰岛素信号调节全身代谢以及外周器官特异性代谢,大多数时候是以辅助方式进行的。
胰岛素通过大脑与胰岛素受体结合,并且独立于血浆胰岛素水平,参与多种全身代谢过程,包括食欲调节、产热、抑制脂肪组织中的脂解以及葡萄糖产生、甘油三酯分泌和肝脏中支链氨基酸的分解代谢。这些过程主要通过迷走神经和/或交感传出纤维的调节来调节。因此,脑胰岛素信号传导受损可导致代谢控制失调,并增加全身性胰岛素抵抗和T2DM的风险。有趣的是,使用脑功能磁共振成像和鼻内胰岛素给药对肥胖个体和正常体重个体进行的研究表明,鼻内胰岛素可以抑制正常体重个体的下丘脑、纹状体和尾状核中内源性葡萄糖的产生,但对肥胖个体无效。同时,正常体重的人与肥胖的人相比,他们的前额叶皮层似乎具有更好的胰岛素敏感性,这表明这些奖励系统关键大脑区域的胰岛素抵抗促进了对食物的渴望,并通过这种方式促进了肥胖。这得到数据的支持,数据显示就食物适口性而言,肥胖个体对鼻内胰岛素具有更差的效果。
在已经被证实的科学研究中,帕金森病与糖尿病在炎症、氧化应激等方面存在共同的发病机制,血糖水平的升高会引起黑质多巴胺能细胞功能的丧失,从而增加糖尿病患者发展帕金森病的风险。此外,糖尿病影响帕金森病非运动症状,可以使非运动症状的数目增加。有文献报道合并糖尿病的帕金森病患者嗜睡、抑郁、性功能障碍、认知障碍及幻觉、胃肠道症状比无糖尿病的帕金森病患者发生率明显增高。引起此现象的病理生理机制可能与糖尿病患者血液中长期胰岛素浓度过高,导致血脑屏障上胰岛素受体的表达减少,进入脑内的胰岛素量下降有关。 最近一项与对照组相比,诊断为帕金森病的参与者表现出早晨血糖水平降低的趋势。有自主神经症状的PD患者有更大的血糖变异性,并且更倾向于在早晨降低血糖水平。自主神经功能障碍的存在,尤其是直立性低血压和排尿障碍,以及自主神经症状的严重程度与血糖变异性较大相关。帕金森病病程中自主神经紊乱的发生使患者更易发生严重的血糖失调。
研究显示由于GLP-1分子质量较小,可直接透过血脑屏障,经胰高血糖素样肽(GLP-1)类似物联合复方左旋多巴治疗6个月后,合并有糖尿病的帕金森病患者的认知功能、日常生活活动能力与运动能力的改善率均明显优于门冬胰岛素、甘精胰岛素等常规胰岛素联合复方左旋多巴的治疗效果;而DPP-4抑制剂,即二肽基肽酶Ⅳ抑制剂,包括西格列汀、维格列汀、沙格列汀、阿格列汀等,能够抑制胰高血糖素样肽-1( GLP-1)和糖依赖性胰岛素释放肽(GIP)的灭活,提高内源性GLP-1和GIP的活性。因此,作为目前治疗2型糖尿病的新靶点,DPP-4抑制剂在合并有糖尿病的帕金森病患者的治疗中已成为首要选择药物。因此,通过调节糖代谢和胰岛素通路可能成为未来治疗帕金森病,尤其是治疗帕金森病合并糖尿病的重要途径之一,这也为合并有糖尿病的帕金森病患者的治疗开启了新篇章。
越来越多的证据支持大脑中胰岛素信号受损的发生,并且可能与帕金森病的神经变性有关。基于此,使用包括GLP1-RAs在内的抗糖尿病药物作为帕金森病患者的疾病缓解剂具有潜在的前景。然而,还没有建立用于临床评估脑胰岛素抵抗的标记物,该标记物将是在PD中测试抗糖尿病药物的未来临床试验的设计和患者选择中有价值的工具。总之,对于2型糖尿病的患者如何管理才能降低患PD的风险目前尚不明确,但无论如何,高血糖毫无疑问是帕金森病的危险因素。控制好血糖、血压和血脂等代谢指标可以延缓脑血管的硬化,同时改善一般健康状态,避免增加心脏病、卒中和肾衰竭等疾病的风险。
参考文献
Ntetsika T, et al. Understanding the link between type 2 diabetes mellitus and Parkinson's disease: role of brain insulin resistance. Neural Regen Res. 2025 Nov 1;20(11):3113-3123. doi: 10.4103/NRR.NRR-D-23-01910.
Komici, K, et al. Diabetes Mellitus and Parkinson’s Disease: A Systematic Review and Meta-Analyses. Journal of Parkinson's Disease, 2021. 11(4): p. 1585-1596.
Chmiela T, et al. Glucose Metabolism Disorders and Parkinson's Disease: Coincidence or Indicator of Dysautonomia? Healthcare (Basel). 2024 Dec 6;12(23):2462. doi: 10.3390/healthcare12232462.
Wahlqvist, M.L, et al. Metformin-inclusive sulfonylurea therapy reduces the risk of Parkinson's disease occurring with Type 2 diabetes in a Taiwanese population cohort. Parkinsonism & Related Disorders, 2012. 18(6): p. 753-758.
Faizan M, et al. Type 2 diabetes mellitus augments Parkinson's disease risk or the other way around: Facts, challenges and future possibilities. Ageing Res Rev. 2022 Nov;81:101727. doi: 10.1016/j.arr.2022.101727.
Pagano G, et al. Diabetes mellitus and Parkinson disease. Neurology. 2018 May 8;90(19):e1654-e1662. doi: 10.1212/WNL.0000000000005475.
Brauer R, et al. Diabetes medications and risk of Parkinson's disease: a cohort study of patients with diabetes. Brain. 2020 Oct 1;143(10):3067-3076. doi: 10.1093/brain/awaa262.
Bayram E, Litvan I. Lowering the risk of Parkinson's disease with GLP-1 agonists and DPP4 inhibitors in type 2 diabetes. Brain. 2020 Oct 1;143(10):2868-2871. doi: 10.1093/brain/awaa287.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#糖尿病# #帕金森病#
9