【Ann Oncol】欧洲骨髓瘤协作组关于原发性浆细胞白血病的诊疗共识
2025-02-27 聊聊血液 聊聊血液 发表于陕西省
欧洲骨髓瘤网络(EMN)专家组回顾了最近的文献,选择PPCL管理中主要关注的领域,采用德尔菲问卷法形成共识,更新了PPCL患者管理指南,基于当前关于该疾病的生物学和临床知识背景提供了实用诊疗建议。
PPCL
原发性浆细胞白血病(PPCL)是浆细胞恶性肿瘤中最具侵袭性的疾病,IMWG最近制定了新的诊断标准:目前PPCL定义为在伴有症状性多发性骨髓瘤(MM)的患者(但既往没有MM)外周血涂片存在>0.5 %的克隆性循环浆细胞(CPC)。研究表明,不适合移植的PPCL患者接受新药联合治疗的中位生存期可达2年,接受移植的患者可延长至3年或更长,但预后仍不佳,特别是与多发性骨髓瘤相比。
欧洲骨髓瘤网络(EMN)专家组回顾了最近的文献,选择PPCL管理中主要关注的领域,采用德尔菲问卷法形成共识,更新了PPCL患者管理指南,基于当前关于该疾病的生物学和临床知识背景提供了实用诊疗建议,近日Pre-proof于《Annals of Oncology》。现整理相关建议供参考。

如何诊断PPCL?
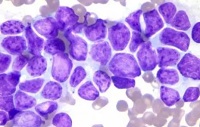
专家组建议通过常规显微镜对所有新诊断 MM 患者的外周血涂片进行仔细的形态学评价。根据 2021 IMWG 标准,如果检测到≥5%的CPC,则可诊断为PPCL。每张涂片应由经验丰富的血液科医生系统分析至少200个循环有核细胞。由于形态学检测并不总是直接易懂(即富含t(11;14)易位的PPCL通常具有淋巴浆细胞样外观),专家组也支持在诊断时常规使用流式细胞术(FC),特别是在确认外周血CPC约为5%的可疑病例时。还应确定CPC的克隆性质,尤其是在存在其他可能解释非克隆性CPC或其他循环肿瘤细胞的情况时。
哪些是 PPCL 的正确初始检查和预后评估?
与 MM 相同,PPCL的充分实验室检查还应包括完整血象和生化及肾/肝功能和钙水平、血清和尿 M 成分的定量和定性(免疫固定电泳)评估、总血清免疫球蛋白、血清受累/未受累游离轻链 (FLC) 比值及其绝对值、一级凝血试验、LDH和β2微球蛋白。建议对骨髓穿刺和骨环钻活检中的克隆浆细胞进行形态学和表型定量。应通过骨髓和外周血中肿瘤浆细胞的多参数 FC 评价表型panel,包括至少CD38、CD138、CD19、CD20、CD27、CD45、CD56、CD81和 CD117 以及细胞质κ和λ链。
染色体畸变分析包括染色体13、t(11;14)、t(4;14)、t(14;16)、del(17p)、gain/amp(1q) 和 del(1p) 的倍性、单体和缺失,应在纯化的骨髓肿瘤细胞上通过 FISH 或经验证的等效分子方法进行,如有必要,在外周血中进行。在无 del(17p) 的患者中也应考虑 p53 突变状态。
外周血中 FC 检测到的 CPCs数量较少,特异性 PPCL 样转录组谱或其他基因组风险标签为未来浆细胞肿瘤的分类及其预后评估开辟了前景。专家小组鼓励将这些技术应用于研究性目的,但尚未建议将其用于 PPCL 患者的当前临床实践。
基线诊断成像应包括低剂量全身计算机断层扫描 (LDWBCT) 联合正电子发射断层扫描 (PET),以识别骨骼溶骨性病变和髓外病变。全身磁共振成像 (WB-MRI),尤其是弥散加权 (DW)MRI,也是一种新兴的(尽管弥散程度较低)关键技术,可能很快成为新的标准。WB-MRI至少与 PET/CT 具有相同的灵敏度和特异性,允许基于人工智能 (AI) 的扫描报告和较高的患者接受度。因此,专家组的一些专家建议,如果可用,WB-MRI应作为首选的初始影像学手段。
根据最近发表的数据,PPCL累及 CNS 的风险增加;因此,如果存在神经系统症状,应进行诊断性腰椎穿刺,但也可以考虑在特定患者中进行(即CPC数量高的患者),最好在初始治疗后等待症状消失,以防止肿瘤溢出至CNS。
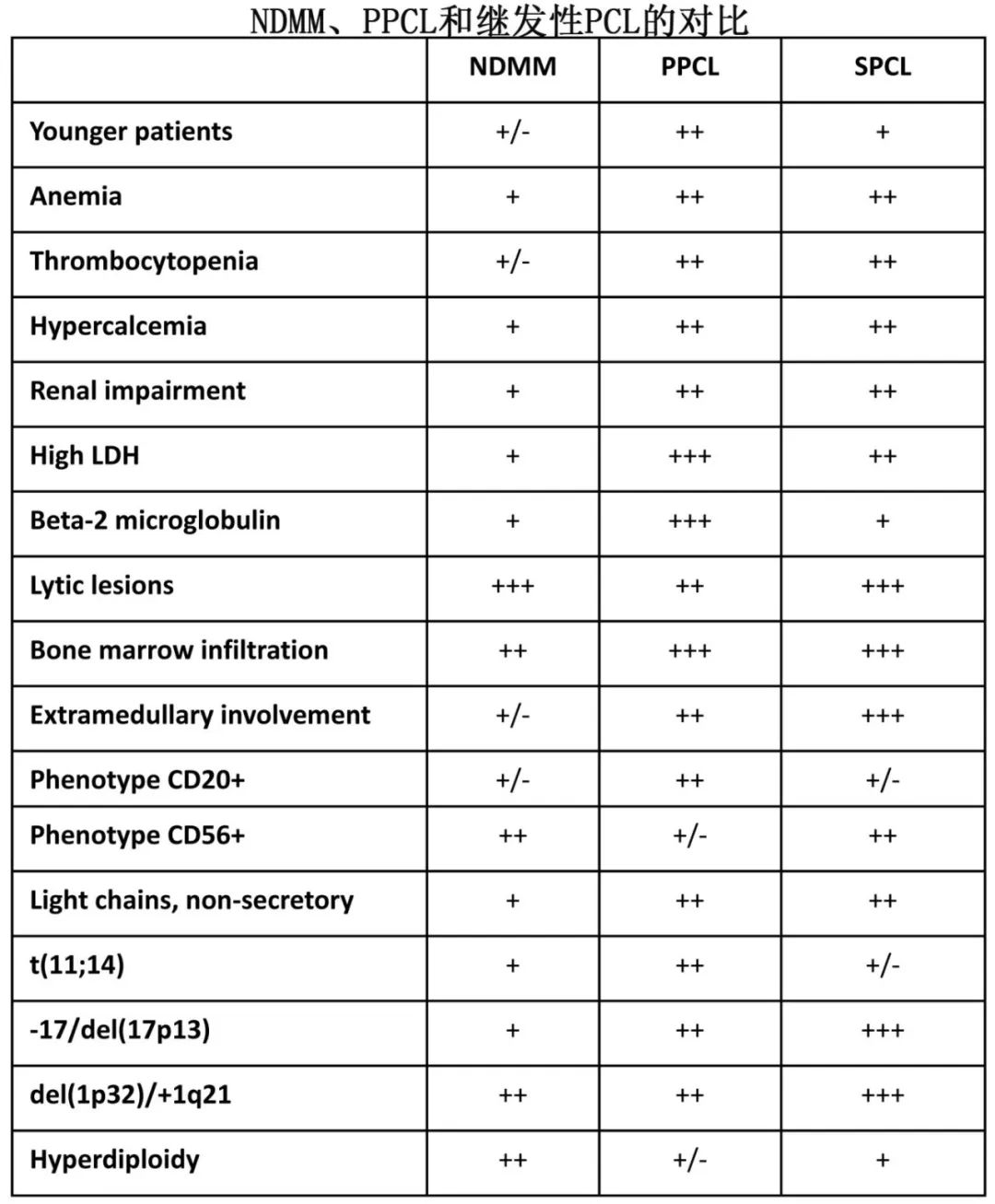
新诊断 PPCL 患者的预后评估应考虑年龄、CPC绝对值、血小板计数、伴随浆细胞瘤、β2微球蛋白和 LDH 水平以及高危细胞遗传学;t(11;14) 的存在可能是有利标志物。
目前PPCL的治疗方法?
a)一般方面
很少有 PPCL 的前瞻性研究,且研究中预后仍不佳,但这些研究形成了推荐的基础,直到出现进一步的证据。专家组认为入组专门的临床试验(如可用)应视为所有 PPCL 患者的有价值选择。
总体而言,应立即开始 PPCL 治疗,个体患者(根据年龄和虽然)应尽可能强化治疗,且无治疗间隔较短。这对于获得快速疾病控制、减少因初始并发症导致的早期死亡、预防/延迟克隆演变诱导的耐药以及对残留疾病具有可能的活性从而降低复发风险是必要的。
所有 PPCL 患者还建议预防 MM 患者常发生的肿瘤溶解综合征,以及进行双膦酸盐类和抗感染预防(包括疫苗接种)。同样,接受 IMID 的无重度血小板减少症患者应按照 MM 的现行指南进行血栓预防。
对于 PPCL 患者,可以考虑使用抗肿瘤药物进行鞘内预防,但尚无关于其有效性的数据,也不推荐使用特定药物,因此专家小组同意鞘内预防仍不推荐作为 PPCL 的标准程序。
b)适合移植(TE)患者的一线治疗
所有 PPCL 患者的初始治疗正在发生变化,取决于最近引入的分子的批准/报销。在此前提下,专家组建议将抗 CD38 抗体、IMID、PI和地塞米松四联治疗作为 TE PPCL 患者的首选一线治疗方案,持续4个周期,之后在70岁以下的健康患者中进行大剂量美法仑 (200 mg sqm)预处理双次自体移植。但专家小组也承认,鉴于 PPCL 中的证据仍然薄弱且仅为回顾性证据,建议使用四药方案以及使用双次而非单次自体移植仅为专家共识意见(目前基于过时的治疗,可能存在选择偏倚)。
由于巩固/维持治疗是改善超高危MM 患者预后的最重要组分之一,因此采用同样的诱导治疗,进一步“灵活”巩固,然后维持治疗直到进展或不耐受(理想情况下采用双药方法,即来那度胺+卡非佐米,或最好添加抗cd38单克隆抗体),可以是合理的移植后治疗。
既往经常采用侵袭性的“淋巴瘤样”化疗方案联合 PI 和/或IMID,如 hyper-CVAD-VD 或VTD/VRD-PACE,尤其是在髓外疾病年轻患者中。但是没有证据表明其优于基于四联诱导方案,专家组建议首选四联诱导作为初始治疗(如可用)。
与自体移植相比,异基因移植在 PPCL 中未显示明显的生存优势,异基因移植与较低的复发率相关,但也与较高的 NMR 风险相关。因此大多数专家组不建议在一线中使用异基因移植。然而根据最近的 EBMT 数据,对于诱导后未达到 CR 的特定 TE 患者,可以考虑在自体移植后进行减低强度预处理异基因移植(如果有合适供者)。

c)不适合移植(TNE)患者的一线治疗
TNE PPCL 患者的预后较差。专家组证实,在当前更新的 EMN 建议中,应计划对年龄较大但fit的患者进行适应年龄、合并症和耐受性的连续治疗,其中KRD方案后 KR 维持在前瞻性研究中提供最佳OS。最近的结果支持在新诊断TNE MM 中使用含 CD38 抗体、PI、IMiD和地塞米松的四联治疗,但尚未在 PPCL 中正式检验。然而专家组认为,尽管仍未进行广泛研究,但抗 CD38 抗体、PI和/或IMID+地塞米松三联治疗或四联治疗(适用时)目前可能是这些 PPCL 患者的适当一线治疗选择,理想情况下,直至缓解得以维持或出现显著毒性。
在高龄和/或frail患者中,除支持性治疗外,还应考虑个体化治疗(即,来那度胺或硼替佐米+地塞米松的剂量和时间调整的联合治疗,以及通常耐受良好的抗 CD38 单克隆抗体辅助治疗),目的是尽可能维持这些患者的治疗时间。

d)复发性/难治性患者的治疗
难治性/复发性 PPCL 的预后极差,目前的挽救治疗很少有效。一般来说,应考虑改用诊断时未使用的药物,倾向于与新一代IMIDs和PI联合使用地塞米松和单克隆抗体。根据年龄和衰弱,“淋巴瘤样”化疗可作为复发时疾病敏感的年轻适合移植患者的异基因移植桥接,但 T 细胞重定向疗法(CAR-T或双特异性抗体)的其他治疗(如可用)可能是更好的替代方案。维奈克拉作为单药或与其他药物联合,可能是携带t(11;14) 患者的选择。

e)缓解评价
应根据 IMWG 标准评估 PPCL 患者的缓解评价。特别是,完全缓解(CR)的定义应包括:除了采用MM的传统标准外,还应包括所有CPC的形态学消失以及通过CT-PET评估的代谢反应。考虑到在PCL中,一线治疗后达到CR的预后重要性,专家组还鼓励对髓系和外周血微小残留病(MRD)进行纵向评估,方法包括使用二代流式细胞术(NGS)或二代测序(NGS)。此外,对于存在髓外病变的患者,还应进行基于MRD的影像学评估。事实上,尽管目前还不建议将MRD数据用于临床目的,但收集这些数据可能会提供进一步的相关见解,这些见解可能会对未来研究的规划有所帮助。
未来展望
PPCL的临床表现和行为可能与超高危多发性骨髓瘤存在重叠,因此,PPCL是否代表一个独特的疾病实体,还是仅仅是MM的一个极为侵袭性的变体,仍然是一个有争议的问题。EMN专家组认为,这两种观点可能都是正确的,但大多数专家的意见是,至少在目前,应维持IMWG对PPCL的现行定义,并据此对患者进行治疗,最好是在专门的临床试验环境中进行。希望这些研究能够包括对现代治疗策略的适当序贯组合,这些策略结合了具有不同作用机制的新药、单克隆抗体、移植(对于适合移植的患者)以及T细胞重定向免疫疗法。专家组承认,尽管关于这些最新治疗方法的数据仍然有限,但在真实世界中接受治疗的某些PPCL患者中,CAR-T细胞疗法已显示出疗效,这突显了前瞻性临床试验在验证这些疗法对这一人群影响方面的重要性。此外,双特异性抗体已在多发性骨髓瘤中显示出显著的单药和联合抗肿瘤活性,但尚未在PPCL中广泛评估,应在适当的时候积极探索,可能结合双靶策略。最后,携带t(11;14)易位的PPCL患者也应纳入第二代和第三代BCL-2抑制剂的临床试验中进行研究。
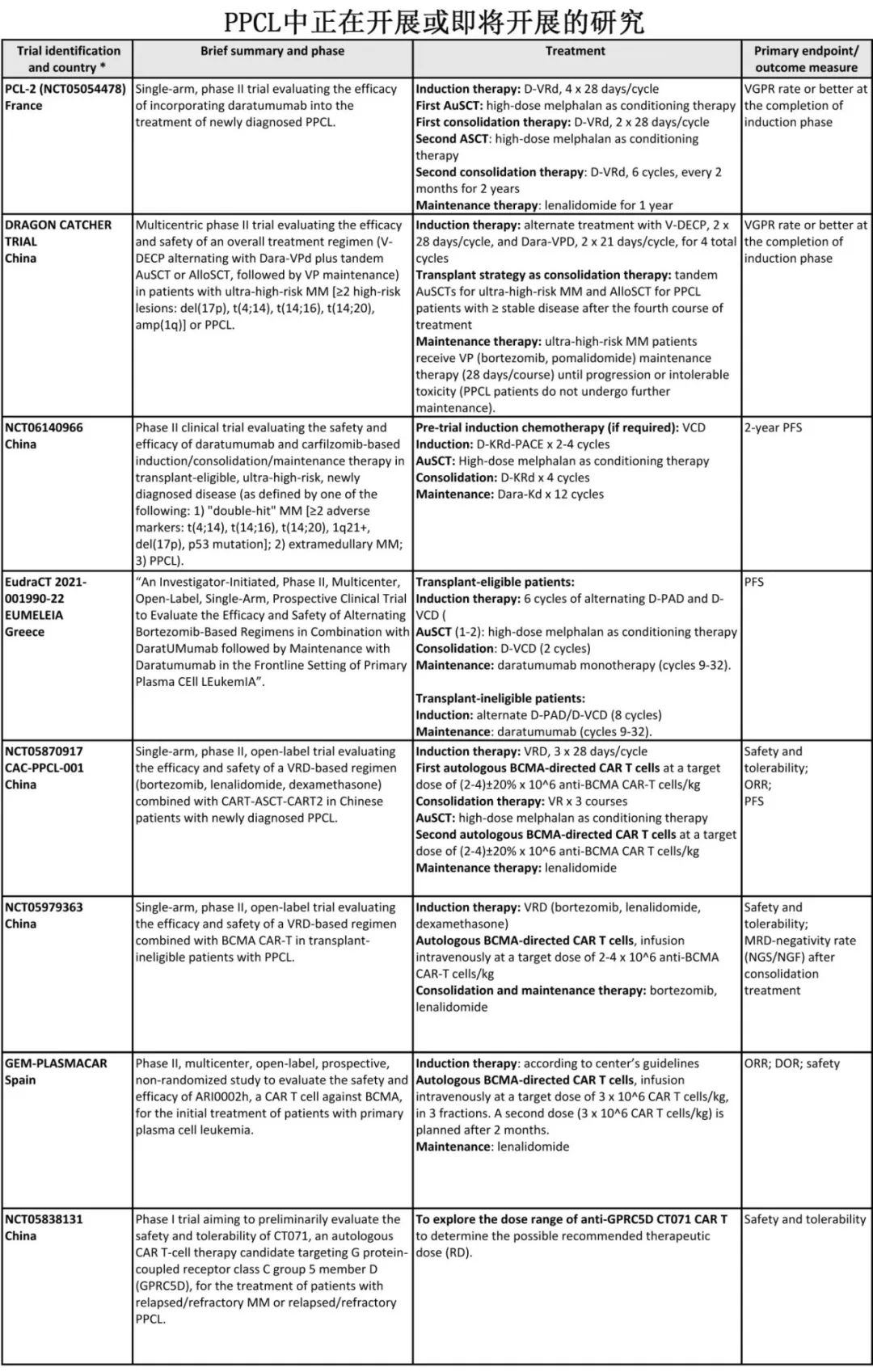
下表总结了正在进行的、包含PPCL患者的临床试验,但其他计划中的研究也即将启动,特别是针对BCMA、GPRC5D及其他靶点的CAR-T细胞疗法或双特异性抗体的研究。然而,尽管新的IMWG诊断标准可能会增加PPCL患者在研究中的入组人数,但该疾病的罕见性仍然存在,并限制了仅在PPCL中开展研究的实际可行性。为了避免这些患者在创新和进步中被忽视,一个可能的解决方案是将他们纳入MM的试验中(而不是像目前这样将他们排除在外)。例如,超高危多发性骨髓瘤和PPCL可以一起纳入研究(因为它们之间可能存在重叠),但需对不同人群分别进行分析。
展望未来,使用基于 AI 的系统和生物计算方法的创新工具可能在未来有助于进行更高效和标准化的 CPC 筛查,并在 PPCL 患者中识别潜在的“可靶向(druggable)”遗传标志物。
PPCL 仍然是未满足的临床需求。尽管如此,还是取得了一些不可忽视的进展。EMN小组强烈支持正在进行和计划中的临床试验,以及基于新技术、战略和治疗方案的生物学研究,这些研究可能代表着未来的突破。
参考文献
Musto P, Engelhardt M, van de Donk NWCJ, Gay F, Terpos E, Einsele H, Fernández de Larrea C, Sgherza N, Bolli N, Katodritou E, Gentile M, Royer B, Derudas D, Jelinek T, Zamagni E, Rosiñol L, Paiva B, Caers J, Kaiser M, Beksac M, Hájek R, Spencer A, Ludwig H, Cavo M, Bladé J, Moreau P, Mateos MV, San-Miguel JF, Dimopoulos MA, Boccadoro M, Sonneveld.P, European Myeloma Network Group Review and Consensus Statement on Primary Plasma Cell Leukemia Annals of Oncology (2025), doi: https://doi.org/10.1016/j.annonc.2025.01.022.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#原发性浆细胞白血病# #PPCL#
10