阿尔茨海默病(AD)最早的病理变化通常始于内侧颞叶,随着病情发展,逐渐扩散至额叶、顶叶、颞叶新皮质及皮质下区域。更惊人的是,患者出现临床症状的20年前,大脑中就可能已存在β-淀粉样蛋白的异常沉积。这一发现揭示了AD的漫长潜伏期——神经退行性病变可能早在数十年前就已悄然启动。然而,这些变化究竟何时开始影响大脑结构?是先天神经发育不足导致“脑储备”不足,还是后天神经退行性加速了萎缩?一项跨越5大队列、近4万人的研究给出了关键答案。

为了破解AD与大脑结构的关联,研究者采用了双向双样本孟德尔随机化分析,整合了5个独立队列(包括英国生物银行、ENIGMA联盟等)的数据,参与者年龄覆盖8至81岁。通过分析AD风险基因对全脑及区域皮层厚度、颅内总体积、皮质下结构体积等指标的影响,团队发现了一个关键时间点:中年。在非临床人群中,AD风险等位基因对大脑皮层和皮质下结构的负面影响从中年开始显现,而在儿童和青年时期,这种关联非常微弱。这意味着,AD的病理进程可能并非“从小潜伏”,而是在中老年阶段突然加速。
传统观点认为,AD主要侵袭记忆相关脑区(如海马体),但新研究却发现了“非典型嫌疑犯”——纹状体结构(如丘脑)。从童年到老年,这些区域始终与AD风险基因存在稳定关联。这一结果挑战了既往认知,提示AD的病理机制可能比想象中更复杂。不过,研究也明确了一点:大脑形态的差异(如先天脑容量大小)并不会直接改变AD风险。换言之,决定患病与否的关键并非“起点”(脑储备),而是后天神经退行性进程的速度。
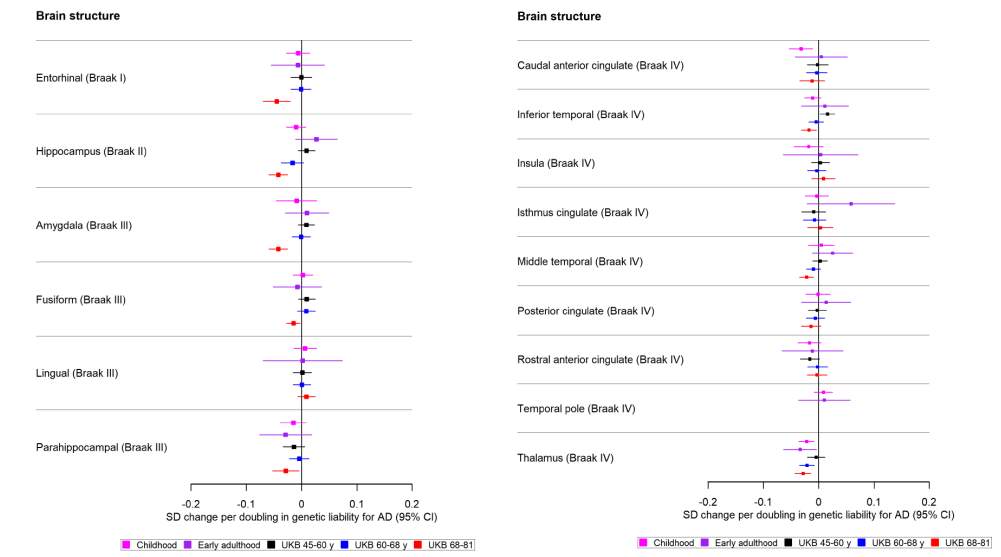
此前有理论认为,大脑先天发育不良(如颅内体积较小)可能增加AD风险,但本研究的数据并不支持这一假说。相反,AD遗传风险主要通过中老年阶段的脑萎缩机制发挥作用。例如,携带高风险基因的人群可能在50岁后出现更显著的皮层变薄或海马萎缩。这解释了为何某些人终身认知正常,却在老年突然发病——衰老与基因的“双重打击”,才是压垮大脑的最后一根稻草。
尽管研究填补了AD时间线上的关键空白,但作者强调,纵向追踪(即对同一人群多次脑扫描)仍是未来的金标准。只有通过动态观察,才能区分“先天不足”与“后天退化”的各自贡献。此外,针对纹状体等非典型脑区的深入研究,或许能为AD早期干预开辟新路径。
参考文献:
Korologou-Linden R, et al. Genetics impact risk of Alzheimer's disease through mechanisms modulating structural brain morphology in late life. J Neurol Neurosurg Psychiatry. 2025 Mar 24;96(4):350-360.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#老年痴呆症# #大脑萎缩#
9