Cell Stem Cell | 功能性神经与血管系统的成功构建:人类肠道类器官研究的重大突破
19小时前 MedSci原创 MedSci原创 发表于陕西省
研究团队通过应用肠道干细胞生态位因子EPIREGULIN(EREG),成功诱导了包含功能性神经和血管系统的复杂HIOs,为人类肠道疾病研究和再生医学提供了新的工具。
人类肠道类器官(HIOs)是从多能干细胞(hPSCs)衍生的三维结构,能够模拟人类肠道的发育和功能。然而,传统的HIOs在体外培养时缺乏神经元、内皮细胞和有组织的平滑肌,这限制了其在模拟复杂肠道功能和疾病中的应用。为解决这一问题,研究团队探索了利用EREG替代传统表皮生长因子(EGF)来增强HIOs的分化能力。
近日,一项发表于《Cell Stem Cell》的研究在人类肠道类器官(HIOs)领域取得了重大突破。题目为“Coordinated differentiation of human intestinal organoids with functional enteric neurons and vasculature”。研究团队通过应用肠道干细胞生态位因子EPIREGULIN(EREG),成功诱导了包含功能性神经和血管系统的复杂HIOs,为人类肠道疾病研究和再生医学提供了新的工具。

研究团队发现,EREG是人类肠道发育中的重要干细胞生态位因子。通过将EREG应用于HIOs的培养,成功诱导了上皮细胞、间充质细胞、神经胶质细胞、内皮细胞和有组织的平滑肌的协调分化。实验中,研究者测试了不同浓度的EREG(1 ng/mL、10 ng/mL、100 ng/mL),最终发现10 ng/mL的EREG条件在HIOs形成效率和细胞类型多样性方面表现最佳。
通过单细胞RNA测序(scRNA-seq)和单核RNA测序(snRNA-seq),研究团队发现EREG培养的HIOs中出现了丰富的神经细胞、内皮细胞和平滑肌细胞,而这些细胞在EGF培养的HIOs中很少见。EREG-HIOs中的细胞不仅在形态上存在,其基因表达谱也与人类肠道细胞高度相似,表明这些细胞在功能上具有相似性。
为了进一步验证EREG-HIOs的功能,研究团队将这些类器官移植到免疫缺陷小鼠的肾包膜下。经过10-12周的体内培养,HIOs进一步成熟并形成了更复杂的组织结构。移植后的HIOs(tHIOs)表现出与人类肠道相似的组织结构,包括有组织的平滑肌、丰富的神经细胞和内皮细胞。
通过器官浴实验,研究团队发现EREG-tHIOs能够自发地进行有节奏的收缩,类似于人类肠道的蠕动功能。这一现象表明,EREG-tHIOs中存在功能性神经肌肉单位。此外,通过药物干预实验,研究团队进一步证实了这些神经肌肉单位的功能性。例如,使用乙酰胆碱受体激动剂(如Bethanechol)能够增强tHIOs的收缩力,而使用乙酰胆碱受体拮抗剂(如Scopolamine)则能够抑制收缩力。
EREG-HIOs中的内皮细胞不仅在体外形成了血管网络,还能够在体内与宿主血管系统连接并形成功能性血管。通过荧光标记的VE-CAD抗体和荧光微珠的实验,研究团队观察到EREG-HIOs中的内皮细胞能够与宿主血管系统连接,并允许血液流动。这一发现表明,EREG-HIOs中的血管网络不仅在结构上与人类肠道相似,而且在功能上也具有相似性。
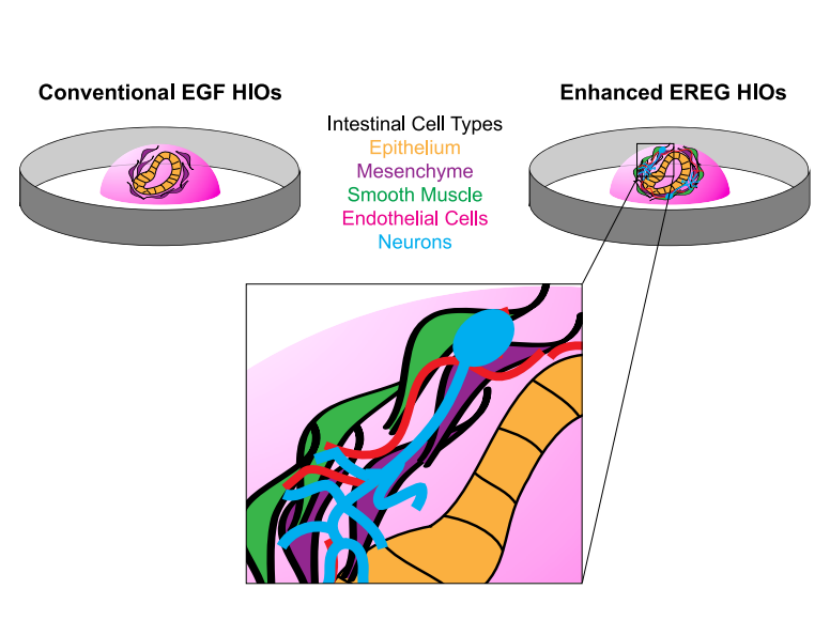
图 本研究模式图
综上所述,这项研究通过创新性地应用EREG,显著提高了HIOs的复杂性和功能性,为人类肠道疾病研究和再生医学提供了新的工具。这种复杂的HIOs模型不仅能够更准确地模拟人类肠道疾病,还能用于高保真度的药物筛选和个性化医学研究,为未来的临床应用提供了新的可能性。
尽管这项研究取得了显著进展,但仍存在一些局限性。例如,HIOs中仍然缺乏某些重要的细胞类型,如免疫细胞和淋巴细胞,这些细胞在人类肠道功能和疾病中发挥着重要作用。此外,尽管EREG在HIOs分化中发挥了关键作用,但其具体的分子机制尚不清楚。未来的研究需要进一步探索EREG在肠道发育中的作用机制,并尝试添加其他细胞类型以完善HIOs模型。
原始出处:
Coordinated differentiation of human intestinal organoids with functional enteric neurons and vasculature. Cell Stem Cell. 2025 Feb 27:S1934-5909(25)00046-3. doi: 10.1016/j.stem.2025.02.007. Epub ahead of print. PMID: 40043706.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#再生医学# #肠道类器官# #干细胞生态位因子# #EREG#
5
神经细胞
0