【麻案精析】时间就是出血风险:接受紧急抗栓治疗患者的硬膜外导管管理
2025-03-24 古麻今醉网 古麻今醉网 发表于陕西省
2025年3月,A A Pract杂志刊发来自美国密苏里大学医学院麻醉和重症医学科的2个病例,描述了接受紧急抗栓治疗患者的硬膜外导管管理。
硬膜外导管在手术和疼痛管理中经常使用,在胸腹部手术中发挥重要作用。硬膜外导管有诸多显著益处,包括改善术后镇痛效果、减少阿片类药物的使用。然而,在导管置入和拔除过程中存在硬膜外血肿的风险。硬膜外血肿会导致严重病残,包括截瘫、生活质量下降,甚至在高达9%的病例中会导致死亡。虽然硬膜外血肿并不常见,但其中19%的病例是由医疗操作(医源性)引起的,这凸显了在导管置入、拔除以及危险因素管理方面保持警惕的必要性。
众所周知,由于基础疾病或更常见的是抗凝药物使用,会导致凝血功能障碍。随着人口老龄化,抗血小板和抗血栓药物的使用也在不断增加。美国区域麻醉与疼痛医学学会(ASRA)的共识指南建议,在进行椎管内麻醉前停用大多数抗血小板药物,氯吡格雷和替格瑞洛的建议停药时间为5-7天。然而,在某些临床情况下,需要对已留置硬膜外导管的患者紧急启动双联抗血小板治疗(DAPT)。在这种复杂的情况下,目前还缺乏关于导管拔除时机的指南,迄今为止的证据仅由个别病例报告组成,处理方法和结果各不相同。
2025年3月,A A Pract杂志刊发来自美国密苏里大学医学院麻醉和重症医学科的2个病例,描述了接受紧急抗栓治疗患者的硬膜外导管管理。
病例1
患者,男性,73岁,ASA分级3级,因休闲车翻车后出现右侧胸痛入院。患者被诊断为多发肋骨骨折,并伴有右侧气胸。入院第2天,患者疼痛剧烈且呼吸状况恶化,遂在T12-L1间隙采用18GTuohy针,通过生理盐水阻力消失法置入胸段硬膜外导管,过程顺利。尽管置入了导管,患者肋骨疼痛仍然明显,且对氧气需求较高,因此在入院第4天安排进行肋骨接骨手术。
全身麻醉诱导后,患者顺利插管。术中,患者血氧饱和度降低,并迅速发展为无脉电活动(PEA)心脏骤停。随即开始胸外按压,并置入右侧胸腔闭式引流管,气胸得以缓解。患者恢复脉搏,氧合改善。手术中止,患者被送回ICU,处于插管和镇静状态。在ICU中,患者肌钙蛋白升高且心电图出现变化,遂请心内科会诊。根据心内科建议,患者负荷剂量服用325mg阿司匹林和300mg氯吡格雷,并随后开始静脉滴注肝素,为心脏支架植入做准备。经与心内科和重症监护团队讨论,确定患者需要立即开始长期双联抗血小板治疗。
因此,决定在抗血小板药物达到最大抑制作用之前立即尝试拔除导管。重要的是,镇静药物能够适当减量,以便进行基础神经系统检查。在服用阿司匹林和氯吡格雷负荷剂量3h后拔除导管,并在ICU中对患者进行频繁的神经系统检查。患者神经系统检查结果保持稳定,当天晚上开始静脉滴注肝素,导管拔除21h后的次日早晨开始维持性双联抗血小板治疗。入院第6天停用肝素滴注。之后,患者顺利进行气管造口术和内镜下胃造瘘管置入术。入院第15天,患者在维持性双联抗血小板治疗下转至长期急性护理机构。
病例2
患者,男性,45岁,ASA分级3级,计划进行经腹会阴联合切除术、结肠造口复杂修复术以及盆底重建术。采用上述方法在T12-L1置入硬膜外导管用于术后疼痛控制,过程顺利。患者被送入手术室并顺利插管。手术开始前,患者接受2g头孢唑林、500mg甲硝唑以及5000单位皮下肝素注射。切开皮肤进入皮下组织时,麻醉团队通知手术团队患者出现严重低血压,血压降至29/22mmHg。
患者因疑似过敏反应注射肾上腺素,但随后被发现处于无脉电活动状态。迅速开始胸外按压,注射3轮肾上腺素,进行11min胸外按压后恢复自主循环。心电图II导联出现ST段抬高,诊断为ST段抬高型心肌梗死(STEMI),给予患者5000单位静脉肝素,并紧急送往心导管室。患者接受了血栓切除术和血管成形术,置入2枚药物洗脱支架,手术结束时负荷剂量服用180mg替格瑞洛和325mg阿司匹林。心内科团队选择替格瑞洛是因为与氯吡格雷相比,其心血管后遗症风险较低。
术后,患者插管并镇静,转至ICU。疼痛管理团队得知情况,经过多学科讨论,心内科团队建议开始长期双联抗血小板治疗。鉴于抗血小板治疗预计不会是短期的,决定在抗血小板药物达到最大抑制作用之前拔除导管,在负荷剂量给药30min后完成导管拔除。根据心内科建议,术后第1天早晨开始使用75mg替格瑞洛和81mg阿司匹林进行维持性双联抗血小板治疗。此后2天患者情况持续改善,术后第4天在维持性双联抗血小板治疗下出院回家。
麻案精析的评述
这两例病例聚焦于接受硬膜外导管镇痛的患者在突发急性心肌梗死后需紧急抗血小板治疗时,出现硬膜外导管的管理难题,为临床麻醉医生提供了极具价值的参考。
从病例处理过程来看,存在诸多值得肯定之处。多学科协作在其中发挥了关键作用。在面对复杂病情时,麻醉科、心内科以及重症监护团队等共同商讨治疗方案,这种跨学科的合作模式有助于综合考虑患者的整体状况,权衡不同治疗措施的利弊。例如,在决定是否拔除导管以及何时拔除时,多学科团队能够从各自专业角度出发,为决策提供全面依据。这也提醒临床麻醉医生,在遇到复杂病情时,不应孤立地处理,而要积极寻求其他科室的支持与协作,充分发挥多学科团队的优势。
在第一例病例中,接受肋骨接骨手术的患者,在留置硬膜外导管的情况下突发急性心肌梗死。为进行心脏支架植入,立即启动双联抗血小板治疗。经过多学科讨论后,决定迅速拔除导管,3h后完成拔除。事后看来,理想情况下应更早拔除导管,使抗血小板药物达到最大血小板抑制作用的时间更短。然而,由于缺乏相关指南,且疼痛管理团队接到变更通知存在延迟,更快采取行动不太可能实现。
在第二例病例中,同样在留置硬膜外导管期间突发急性心肌梗死。疼痛管理团队反应迅速,在负荷剂量给药后30min内拔除导管,将血小板抑制发生的时间减到最短。需要注意的是,如果疼痛管理团队更早介入,考虑到替格瑞洛出血风险较高,相比之下使用氯吡格雷可能更为合适。由于两例患者都将继续接受双联抗血小板治疗,实验室检查值不太可能改变导管拔除的必要性,因此在拔除导管前,并没有为了评估实验室检查值而延迟拔除。
ASRA与欧洲区域麻醉学会(ESRA)在2018年联合发布的总结指南建议,在尝试进行椎管内麻醉前停用抗血小板治疗。然而,对于已留置的硬膜外导管,在拔除时机方面提供的指导有限。指南对药代动力学进行了深入讨论。阿司匹林在服用1h后可显著抑制血小板。然而,阿司匹林导致硬膜外血肿的风险极小。对于接受负荷剂量药物的患者,替格瑞洛在30min时达到血小板抑制峰值,氯吡格雷在4-6h达到峰值(见表)。
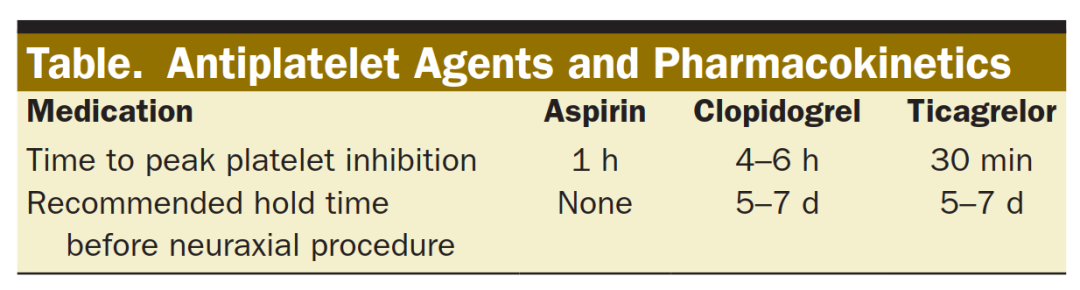
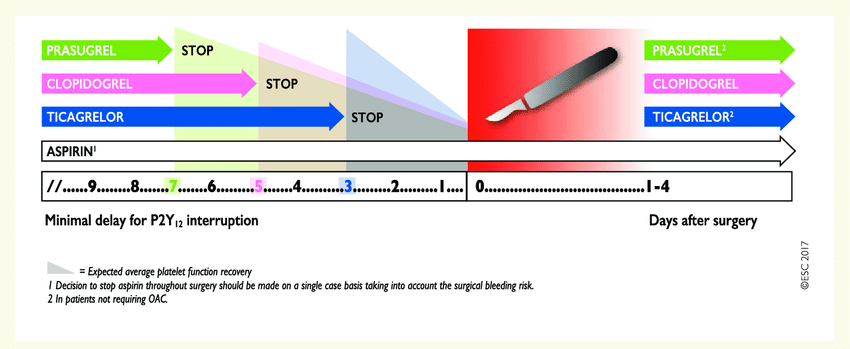
这表明在启动双联抗血小板治疗和达到血小板抑制峰值之间存在一个短暂的“机会窗口”。在此期间拔除导管风险较低。欧洲区域麻醉学会建议“对于负荷剂量服用阿司匹林和氯吡格雷的患者,可以在氯吡格雷完全起效前立即拔除神经轴导管”。然而,该指南的推荐级别较低(2C),因为它基于药代动力学数据,而非临床证据。
然而,病例也暴露出当前临床实践中的一些问题。目前,对于已留置硬膜外导管的患者在紧急启动双联抗血小板治疗时,缺乏明确统一的导管拔除时机指南。这导致在实际操作中,医生只能依据有限的病例报告和经验来做出决策,存在较大的不确定性。这提示临床麻醉医生,在面对此类情况时,要保持谨慎态度,密切观察患者病情变化,同时积极参与相关研究,为完善指南提供临床数据支持。
另外,不同医院和医生在处理此类病例时方法和结果差异较大。部分案例中,因沟通不畅或评估不全面,导致导管拔除时机不当,进而引发严重并发症。这警示临床麻醉医生,在处理复杂病例时,要严格规范操作流程,加强团队内部以及与其他科室之间的沟通交流,确保信息传递准确及时,避免因人为因素造成不良后果。
对于临床麻醉医生而言,这两例病例带来的启发是多方面的。在日常工作中,要不断加强专业知识学习,不仅要精通麻醉技术,还要深入了解心血管疾病、抗凝药物等相关知识,提升应对复杂病情的能力。同时,要积极参与多学科会诊和病例讨论,积累经验,提高自身在复杂情况下的决策能力。在面对指南未覆盖的情况时,要依据现有的医学理论和临床经验,制定合理的治疗方案,并密切关注患者的治疗效果和不良反应。
这两例病例为临床麻醉医生在处理紧急抗栓治疗下硬膜外导管管理问题提供了重要的借鉴。通过对病例的深入分析和总结,有助于提升临床麻醉医生的专业水平,优化临床实践,最终为患者提供更安全、有效的医疗服务。
参考文献:
Murin P, Verma M, Sadeghipour H. Time Is Bleeding Risk: A Case Report of Epidural Catheter Management in Two Patients Receiving Emergent Antithrombotic Therapy. A A Pract. 2025;19(3):e01945. doi: 10.1213/XAA.0000000000001945
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















前沿开阔眼界
2
#抗栓治疗# #硬膜外导管#
6