锌治疗痤疮临床应用研究进展
2024-10-24 海龙话皮 海龙话皮 发表于上海
本文介绍锌治疗痤疮的机制及研究进展,包括锌稳态、作用机制、临床应用、有效性安全性及不良反应,锌可辅助治疗痤疮,未来需进一步研究其作用及临床应用。
痤疮是一种主要累及毛囊和皮脂腺的慢性炎症性皮肤病,主要好发于年轻人。大多数患者通过规范治疗,皮损能得到一定程度的改善,但仍有一部分患者效果欠佳或者停药不久后又复发。痤疮丙酸杆菌(cutibacterium acnes,C acnes)等毛囊微生物定植是痤疮重要的致病因素,在痤疮的治疗中,抗生素的应用起着不可或缺的作用,但滥用抗生素或长期使用,会导致细菌对传统药物产生耐药性。有研究发现痤疮患者的皮损部分出现痤疮丙酸杆菌生物膜样结构,形成生物膜后会进一步导致抗菌治疗失败。由于疾病控制不佳或反复发作,痤疮患者往往伴有不同程度的焦虑情绪,故寻找有效治疗痤疮的辅助药物至关重要。
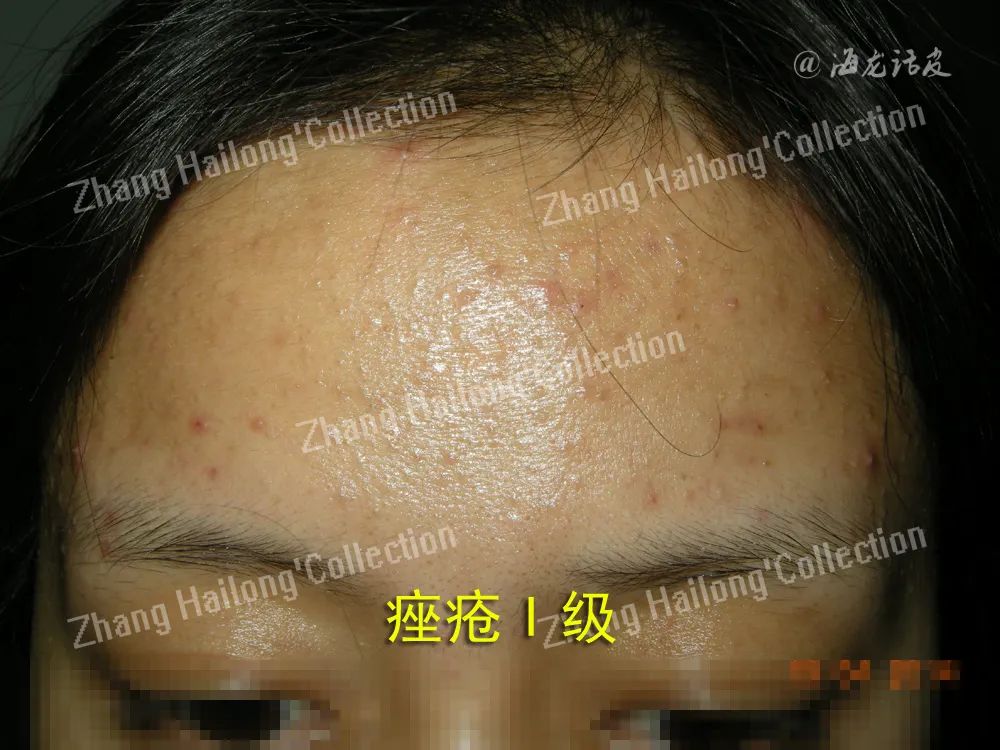
锌是细胞内最丰富的元素之一,也是1000多种酶促反应和2000多种转录因子的辅助因子,是各种生理过程的必需元素,在机体生长发育、代谢、维护免疫功能中发挥 重要作用。在表皮角质形成细胞中,锌主要参与其分化、抗炎和伤口愈合过程。
锌稳态
锌是人体所必需的微量元素,它在体内以锌离子(Zn2+)的形式存在,并通过与各种结构结合发挥其作用,最常见的是与蛋白质结合,如在血清中与白蛋白或α2巨球蛋白结合,在细胞质中与金属硫蛋白或钙卫蛋白结合。金属硫蛋白是最重要的锌结合蛋白,它能充当细胞内锌储库并且在需要时释放细胞内游离的锌。
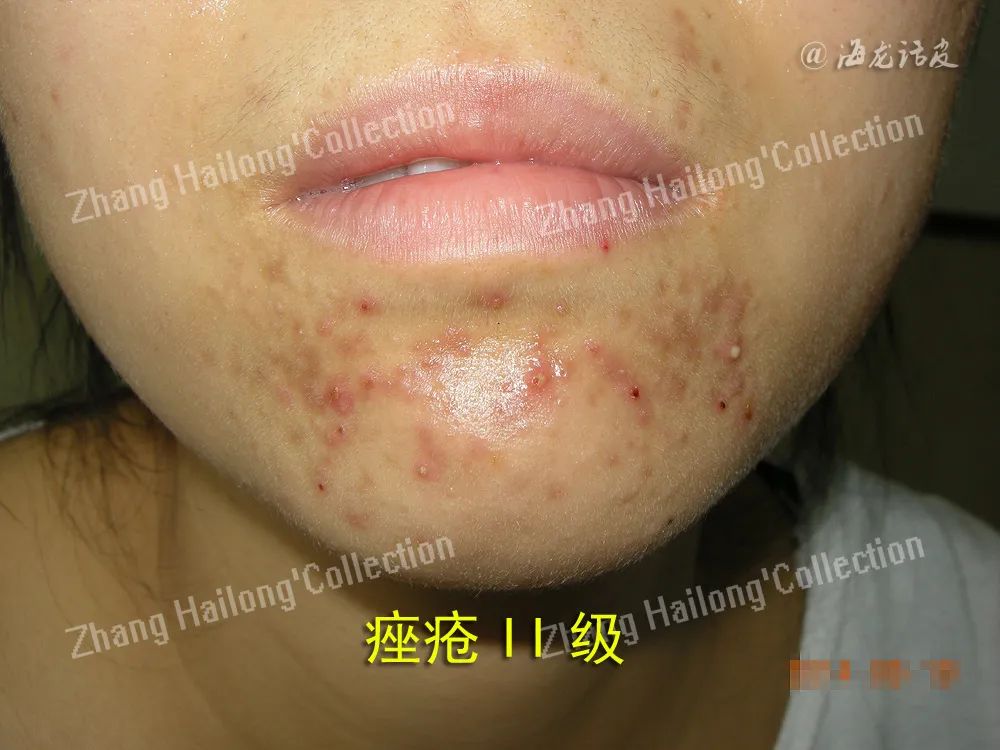
锌稳态对于维持免疫系统正常功能以及维持肠道菌群和皮肤稳态至关重要,锌稳态主要通过14个增加细胞质锌的锌转入蛋白(zinc importers,ZIP)和10个降低细胞质锌的锌转出蛋白(zinc exporters,ZnP)的表达和作用来调节,锌缺乏会导致免疫细胞数量和活动的严重紊乱,从而导致感染和炎症性疾病的易感性增加,如炎性肠病、寻常痤疮、化脓性汗腺炎等。
锌治疗痤疮的作用机制
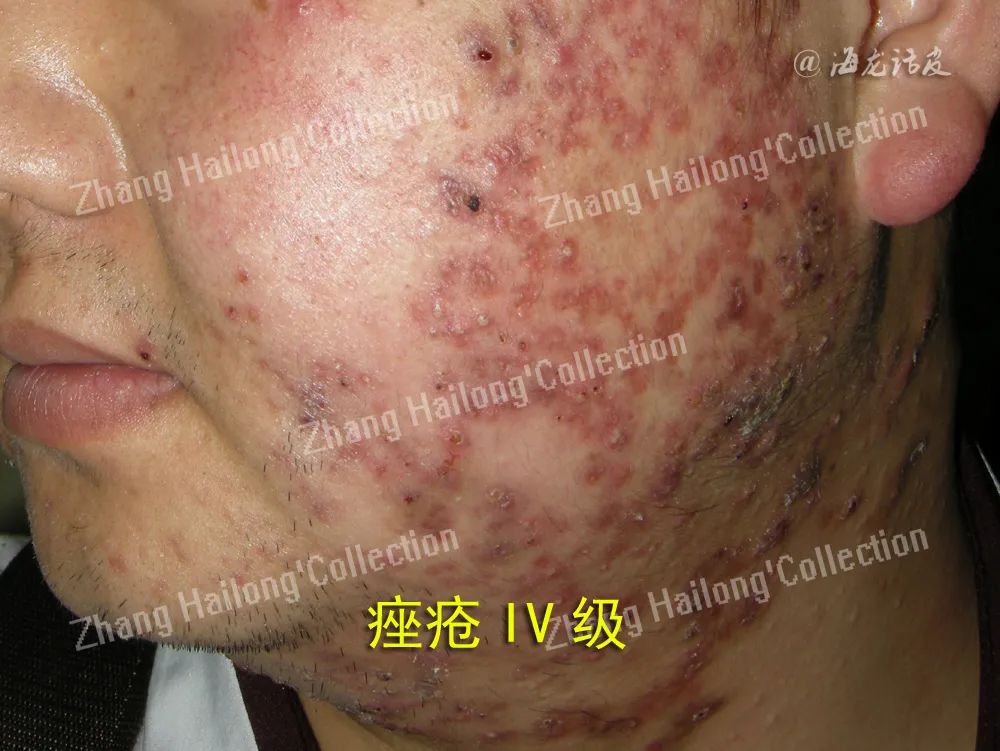
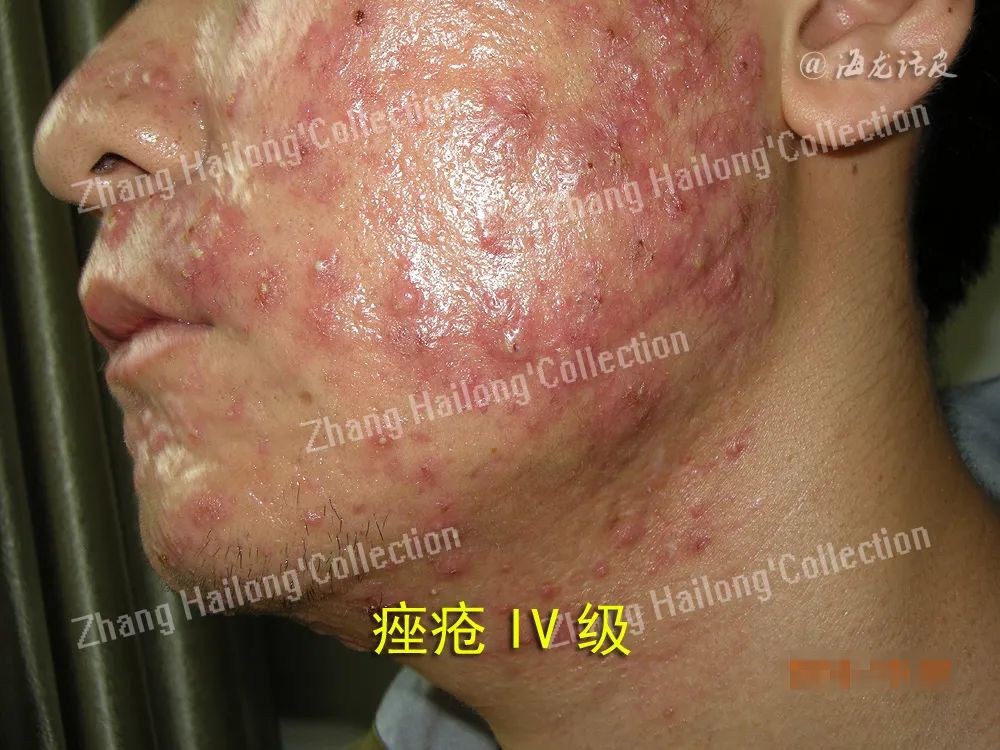
痤疮是一种多因素的毛囊皮脂腺疾病,其促成因素包括雄激素引导皮脂腺过度分泌皮脂、毛囊皮脂腺导管角化异常、C.acnes等毛囊微生物定植、炎症及免疫反应。C.acnes是一种革兰氏阳性厌氧菌,喜欢定植于无氧的皮脂腺单位,有研究发现,C.acnes的分离株能在体外诱导人表皮角质形成细胞生长,而C.aacnes介导角质形成细胞增殖并加剧其所在区域的炎症可能是引起炎症性痤疮病变和痤疮初始阶段微粉刺形成的关键因素,此外,C.acnes还能够介导免疫反应、促进炎症因子释放来引发炎症。
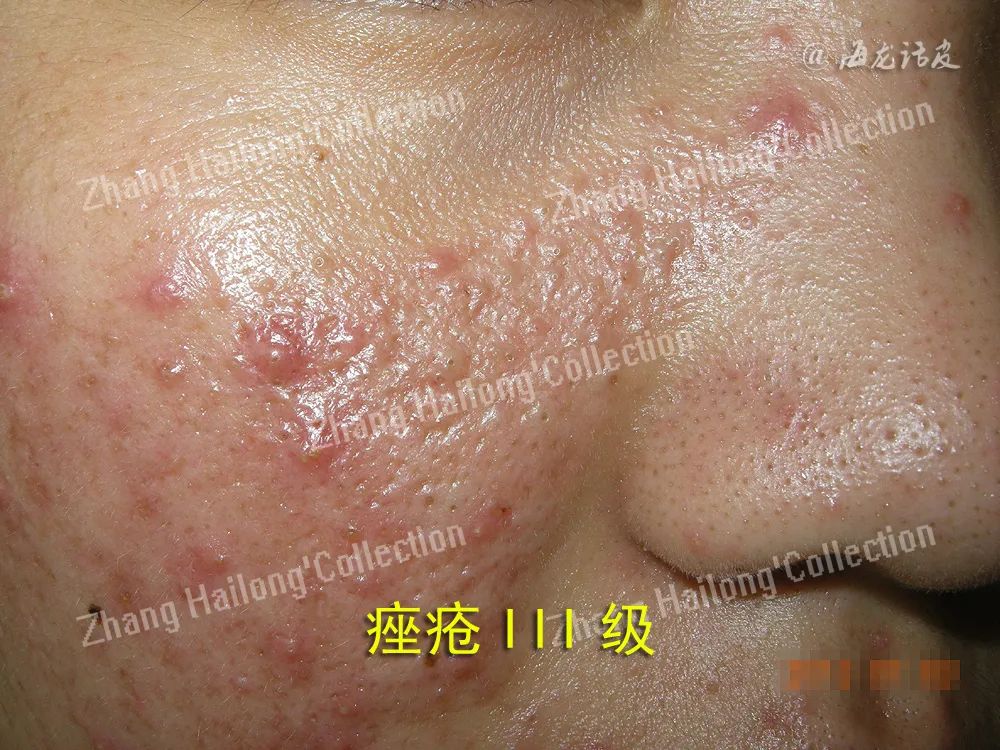
锌是人体必需的微量元素,是免疫系统的关键调节剂,研究表明痤疮患者存在不同程度的锌缺乏,锌的摄入可通过不同机制降低炎症反应,锌能够抑制白细胞趋化、抑制雄激素的活性来减少皮脂分泌,还能抑制人角质形成细胞上的TOLL样受体2(toll like receptors-2,TLR-2)的表达以减少促炎因子的合成和释放,通过干扰细菌脂肪酶的活性来达到抑菌的作用等。
1、锌、C.acnes与炎症因子和免疫反应:
研究表明C.acnes通过产生脂肪酶、透明质酸酶和蛋白酶等物质来激发免疫反应,引起多种促炎因子释放,从而引起炎症,在一项观察性研究中有学者表明在不同严重程度的痤疮皮损周围均能观察到极化的Th1/Th1细胞、巨噬细胞和肥大细胞的异常浸润。Yang等在GSE108110数据库中选取了18例痤疮患者的丘疹活检样本通过CIBERSORT分析发现,痤疮病变周围的中性粒细胞、单核细胞和活化的肥大细胞浸润明显较正常皮肤增加。
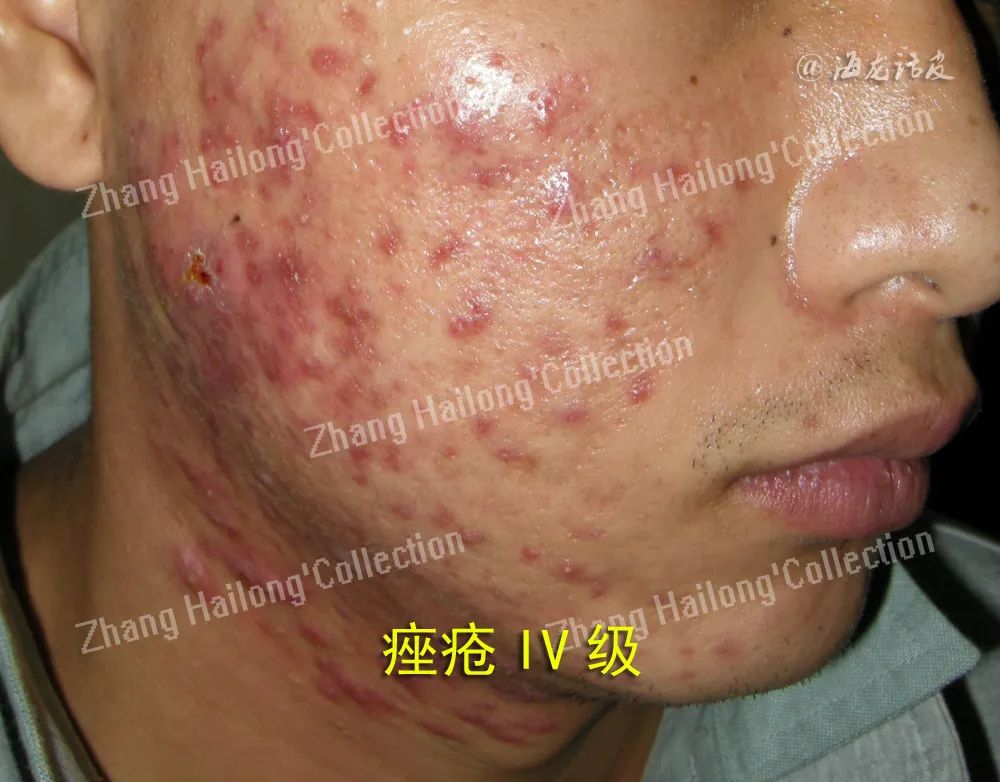
另有研究表明,IL-6是痤疮发病中重要的促炎因子之一,它诱导表达的急性期蛋白(APP)会与TLR相互作用再诱导产生NLRP3炎性小体,随后激活Janus激酶/信号转 导子和转录激活子(janus activated kinase signal transducer and activator of transcription,JAK-STAT)3和丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)信号通路,锌缺乏会刺激JAK-STAT3信号通路的激活;在原髓细胞系中的体外研究表明,补充锌(100或20μM锌,10μM吡啶硫酮)会降低粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colony stimulating factor,GM-CSF)诱导的MAPK信号传导和G-CSF诱导的信号转导和转录激活因子(STAT3)的激活。
关于锌影响细胞分化中STAT活性以及细胞间的信号传导通路的详细机制,值得进一步深究。在痤疮发展过程中,C.acnes能激活TLR2产生,从而刺激离体人皮脂腺导管过度角质化和粉刺形成。Jugeau等发现锌盐能够降低TLR2的表达,从而表现出抗炎作用,故推测锌盐能够改善毛囊口的角化和减少粉刺的形成。未来仍需要大样本的数据以及实践应用来证实这样的推测。
近年来,越来越多关于通过调节肠道微生物群来维持皮肤稳态的研究出现,肠道微生物群失调也可造成皮肤炎性疾病。Volkova等在对114例痤疮患者肠道微生物群差异性的观察性研究中发现54%的患者出现了肠道菌群失调。Deng等发现痤疮患者的厚壁菌门减少,拟杆菌门增加,梭菌科(如毛螺菌科和瘤胃球菌科)显著减少。而锌可通过调节肠道免疫细胞的功能和免疫活性物质的表达来帮助维持功能性黏膜免疫屏障,还可通过免疫机制维持肠道微生物的稳定。
2、锌、C.acnes与氧化应激:
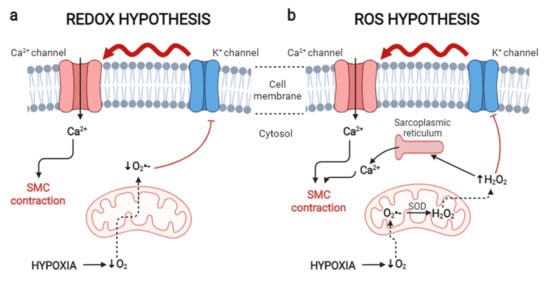
痤疮的发生与氧化应激反应密切相关,在C.acnes定植过程中,C.acnes能产生多种化学因子来诱导嗜中性粒细胞的趋化,而嗜中性粒细胞分泌活性氧分子(reactive oxygen species,ROS)攻击C.acnes,以此循环来引发炎症;此时体内许多酶和化合物,如过氧化氢酶(catalase,CAT)、超氧化物歧化酶(super oxide dismutase,SOD)、髓过氧化物酶(myeloperoxidase,MPO)、谷胱甘肽(glutathione,GSH)和黄嘌呤氧化酶(xanthine oxidase,XO)等参与氧化应激反应来清除或减少ROS的产生。
锌可激活抗氧化分子和蛋白质,例如GSH和SOD,并降低促氧化酶的活性;抑制产生超氧化物的酶-烟酰胺腺嘌呤二核苷酸磷酸(nicotinamide adenine dibucleotide phosphate,NAD-PH)氧化酶,而锌缺乏会导致SOD功能障碍,从而ROS不能被及时清除,ROS诱导的细胞凋亡又进一步导致细胞缺氧和氧化应激,加剧痤疮的发生。
Akamatsu等报道痤疮炎症患者中性粒细胞产生的ROS水平较健康人显著增加,Iinuma等发现抗坏血酸锌具有显著的SOD样活性,并对痤疮丙酸杆菌、金黄色葡萄球菌、大肠杆菌均有显著抑制作用。Bae等在研究中比较了氧化锌(ZnO)、柠檬酸(citric axid,CA)及其混合物对C.acnes的抗菌活性,表明在CA浓度不变的情况下,ZnO-1的浓度能直接影响ROS的产生,1:1的ZnO和CA的比例产生了最高的抗菌活性,得出的结论是ZnO与CA抗菌有协同作用,ZnO能减少ROS的产生,故ZnO可以作为预防和改善痤疮的有效抗菌成分。
3、锌、痤疮与脂质代谢:
皮脂过多是痤疮发生、发展的重要因素,也是重度痤疮的危险因素。痤疮大多始于青春期,这是由于肾上腺和性腺来源的雄激素增加,使得皮脂分泌更加旺盛,在痤疮病变的皮肤区域,雄激素受体和5α-还原酶表达较多,5α-还原酶可将睾酮(testosterone,T)转化为最有效的雄激素二氢睾酮(dihydrotesterone,DHT),而锌可以抑制1型5a-还原酶的活性来抑制雄激素之间的转化从而减少皮脂分泌。
Szanto等发现C.acnes会刺激皮肤中胰岛素样生长因子1(Insulin like growth factors-1,IGF-1)的分泌,IGF-1可增强皮脂生成并促进角质形成细胞和皮脂细胞的增殖,还是性腺睾酮和肾上腺脱氢表雄酮产生的强效诱导剂,并促进T转化为DHT,而锌具有下调IGF-1和IGF-1R水平的作用,葡萄糖酸锌可抑制角化细胞中C.acnes对IGF-1和IGF-1R表达的诱导。
锌治疗痤疮的研究进展
1、锌在治疗痤疮中的临床应用:
随着越来越多关于锌制剂治疗炎性疾病的报道,我国也陆续展开了锌制剂对痤疮的研究,多篇文献表明联合甘草锌颗粒治疗轻中度痤疮患者效果显著。甘草锌颗粒的作用与糖皮质激素相似,可促进皮损消退,联合其他药物或物理治疗可缩短病程。在一项回顾性分析中发现阿达帕林凝胶联合甘草锌颗粒能显著提高治疗痤疮患者的疗效。
严芳等发现果酸联合甘草酸颗粒治疗寻常性痤疮患者疗效优于单用甘草酸颗粒,在显著减轻炎症的同时还淡化了瘢痕及色素沉着。还有研究表明甘草锌颗粒联合红蓝光治疗,或者联合口服异维A酸也能加快痤疮皮损症状的消退。未来可以探索更多锌的联合疗法来治疗严重程度不同的痤疮。
2、锌治疗痤疮的有效性及安全性评估:
自从锌制剂应用于临床后,来自不同国家的多项观察性研究均证 实了锌制剂治疗痤疮的有效性和安全性。Abendrot等通过实验证明化合物甘氨酸锌和组氨酸锌对角质形成细胞和成纤维细胞的体外细胞毒性低,但对 C.acnes的抑制活性高,故将0.66%甘氨酸锌和1.27%组氨酸锌制成凝胶,通过测量pH、密度和黏度评估了这两种制剂,发现其物理化学性质稳定、微生物纯度高, 且有防腐的功效;并通过斑贴试验对一组25例有过敏史健康志愿者进行皮肤耐受性测试,结论为甘氨酸锌凝胶、组氨酸锌凝胶对受试者没有刺激作用,可局部用于治疗痤疮。
Saedana等在一项观察性研究中让48例轻中度痤疮患者接受连续3个月的口服甲硫氨酸结合锌胶囊治疗,3次/d,一次1粒,结果显示第8周有79%患者皮损达到80%~100%改善,脓疱、丘疹和闭合性粉刺均明显减少,且只有2例患者出现了不良反应,1例患者出现腹痛腹泻,另1例患者出现急性荨麻疹。
Tolino等通过招募100例轻中度痤疮患者,并对他们进行随机分组来比较硫酸锌与赖甲环素的疗效,治疗期为12周,分别在治疗第4周和12周后,使用全球痤疮分级系统(global acne grading system,GAGS)和痤疮特异性生活质量(acne quality of life,AQOL)问卷来评估痤疮的严重程度。研究发现两组患者在治疗4周和12周GAGS评分均下降,组间差异不明显,但硫酸锌治疗的患者AQOL评分的改善明显高于赖甲环素组。由此可知,硫酸锌的优势在于治疗期间安全性更高,受众人群更广,可以用于儿童患者以及孕妇,并且不会引起任何光毒性或光敏反应,且不受日光照射的影响。
国外一项研究表明单独使用锌治疗或联合治疗时,可显著改善炎性丘疹平均计数。虽然单剂锌产品和组合锌产品的研究均表明锌可有效治疗寻常性痤疮,但通过比较研究表明组合剂可能比单剂更有效,并且更易耐受。锌制剂在大部分痤疮患者中是安全、有效的,相关不良反应均可自行缓解,但锌制剂在重度痤疮患者中的应用研究还很缺乏,以及对于痤疮患者的长期维稳和预后相关研究相对很少,故其长期疗效和治疗重度痤疮患者的疗效还有待进一步研究。
3、锌治疗痤疮的不良反应:
既往多项研究均证实了锌在痤疮中应用的有效性及安全性,不良反应事件的发生概率很低。Cervantes等分析了32篇关于口服锌治疗痤疮的研究,有11篇报告锌治疗引起的不良反应,大多数报告不良反应的研究(10/11)均为使用锌作为单药治疗,主要为胃肠道不良反应,如恶心、呕吐、腹泻等。总体锌合剂具有良好的耐受性,且不良反应持续时间短暂且轻微。
局部用锌可能会引起皮肤刺激,红斑,灼热和瘙痒,这可能是由于锌在亚油酸向前列腺素的转化中的潜在作用。随着锌复合制剂的形式越来越多,我们应根据患者的具体情况(有无合并其他疾病)来选择合适的复合制剂,虽然目前还未发现不可逆转的不良反应,仍需长期观察和随访。
总结与展望
目前世界上许多国家把锌制剂作为痤疮的代替或辅助治疗,欧洲皮肤病学论坛痤疮治疗指南推荐口服锌治疗轻中度丘疹性痤疮。锌制剂可适度改善痤疮患者的临床效果,包括减轻炎症、改善毛囊口角化、减少皮脂分泌、减轻痤疮患者的焦虑程度、减少其他抗生素类药物的使用等等,锌制剂的长期安全性也在临床使用中得到了肯定的验证。在未来,对锌作用机制的进一步了解将为锌制剂在痤疮治疗中的应用提供理论依据。未来的研究需要评估在不同程度炎症表型中的有效性,或联合哪种药物能发挥最佳作用。
在临床工作中广泛引入锌作为代替或辅助治疗之前,需要解决部分研究的局限性。目前临床观察研究中大都采用几种痤疮严重程度分级量表进行评估痤疮患者的严重程度及疗效对比,但这些量表缺乏对患者用药后的具体评估,尚无研究明确提及治疗后的随访时间或治疗结束后痤疮有无复发。在未来研究中,可以增加一些更具体的标准量化指标,例如治疗后皮脂分泌情况、毛囊口角化改善情况、治疗平均起效时间、复发时间等等,以便更好地量化治疗结果。目前,我国应用联合锌制剂治疗痤疮的有效性及安全性均较好,但仍处于探索研究阶段,需要更大规模的临床研究、长期随访及相关数据证实其长期的有效性及安全性。
参考文献:
1.王一帆,缪雨晴,张敏红等.锌治疗痤疮的作用机制及临床应用研究进展[J].四川医学,2023,44(3):311-314.
2.张冬霞.甘草锌颗粒联合红蓝光治疗仪治疗痤疮的临床疗效及安全性观察[J].黑龙江医药,2022,35(2):406-408.
3.顾月婷.载低氧预处理间充质干细胞条件培养基的可溶微针构建及其用于雄激素源性脱发的治疗研究[D].杭州:浙江大学,2023:89.
3. 夏丹英.异维 A 酸联合甘草锌治疗痤疮的临床疗效[J].中国医疗美容,2015,5(3):72-73.
4.其他文献略。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#锌# #痤疮#
21