Br J Pharmacol 南方科技大学王莹团队合作揭示核定位cAMP信号微域调控肾脏纤维化新机制
2024-10-26 论道心血管 论道心血管 发表于上海
本研究揭示糖尿病肾病中核定位 β1-AR/cAMP 信号微域激活 YAP 促肾系膜细胞纤维化,建立新方法可视化 cAMP 调控,抑制磷酸二酯酶 4 可减轻肾脏纤维化,提供精准治疗策略。
慢性肾病大约影响全球10%的人口,其中糖尿病肾病(Diabetic nephropathy,DN)是导致慢性肾病的主要原因之一。DN会导致纤维化基质过度沉积,进而介导肾脏结构和功能的损害。研究表明,肾系膜细胞在DN进展过程中发生实质性改变,产生大量基质。剖析肾系膜细胞纤维化机制可能为治疗DN提供新的治疗策略。最新研究表明,cAMP信号以纳米尺度排列在胞内的不同区域,cAMP信号异常可以导致多种组织纤维化。与传统的cAMP信号调控相比,亚细胞定位的cAMP信号微域(microdomain)能更精确调控胞内过程。然而,在肾脏肾系膜细胞中是否存在cAMP信号微域及cAMP信号调控肾脏纤维化分子机制还需要进一步研究。
2024年10月2日,南方科技大学医学院药理学王莹课题组与美国UC Davis药理系合作在药理学经典期刊British Journal of Pharmacology上发表了题为“Diminished nuclear-localized β-adrenoceptor signalling activates YAP to promote kidney fibrosis in diabetic nephropathy”的研究性文章。本研究利用区域化荧光共振能量转移(Fluorescence Resonance Energy Transfer,FRET)生物传感器揭示了DN肾脏肾系膜细胞中核定位的β1-AR/cAMP信号微域的时空调节,发现了β-AR信号在DN中一种新的作用:细胞核定位的β1-AR/cAMP信号微域,进而通过PKA依赖的去磷酸化激活YAP,促进肾系膜细胞纤维化。

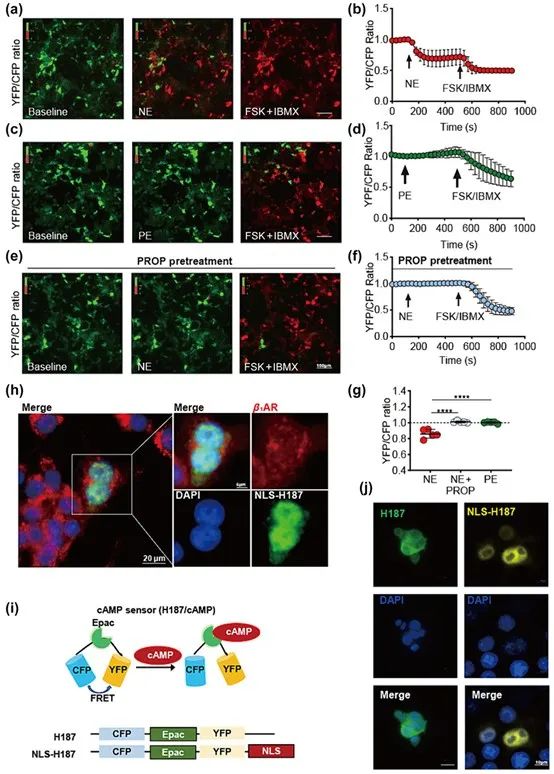
研究表明,PKA依赖的磷酸化活性能被区域化的cAMP微域精准调控。与现有的治疗策略相比,区域化cAMP精准调控以高疗效、低不良反应已经成为了一种有潜力的靶向治疗策略。为了评估肾系膜细胞中微域特异性PKA介导的YAP磷酸化机制,本研究建立了基于基因编码的FRET生物传感器的区域化cAMP研究新方法去可视化肾系膜细胞中cAMP对肾上腺素受体调控的实时动态,开展核定位cAMP调控DN的研究。
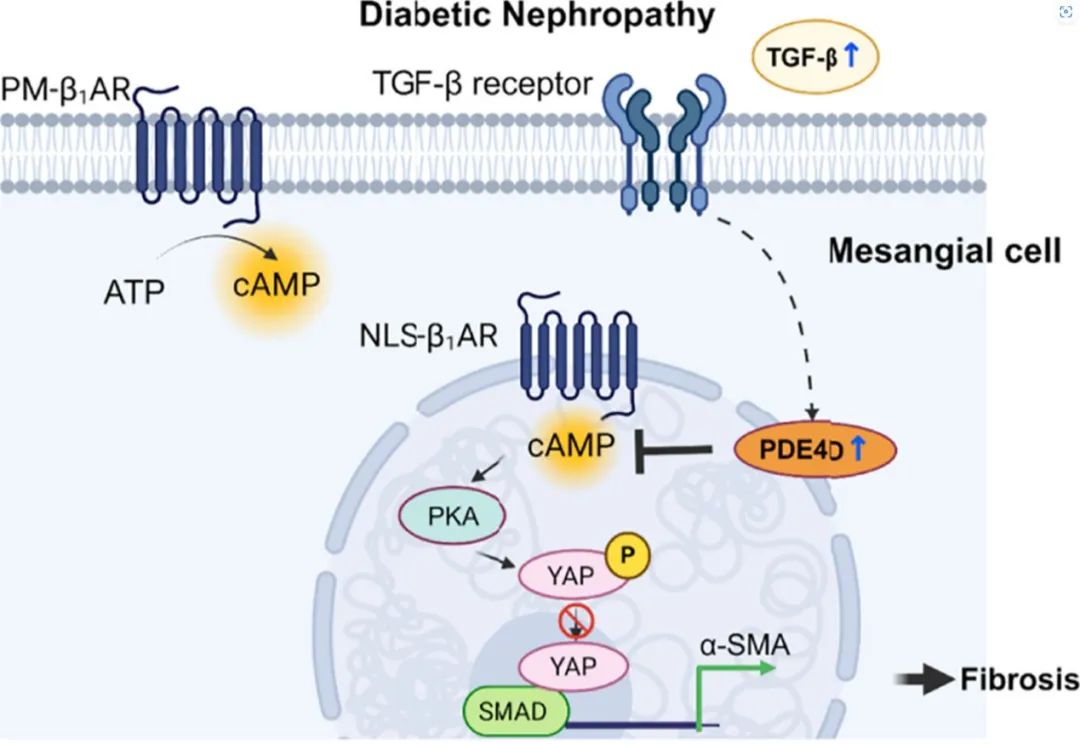
本研究发现,DN导致肾上腺素受体信号紊乱和肾系膜基质沉积。其中,肾系膜细胞纤维化在DN中扮演重要角色,且与YAP激活有关。在此过程中,YAP在细胞核内的积累促进肾系膜细胞纤维化基因Acta2、Ctgf的转录表达。借助FRET成像研究发现,肾系膜细胞中β1-AR产生的cAMP在细胞核内形成微域,进而介导YAP (Ser397)磷酸化。在纤维化刺激条件下,磷酸二酯酶4 (PDE4D)的上调选择性地破坏了细胞核定位的cAMP微域,进而导致PKA介导的YAP (Ser397)磷酸化水平下降,YAP介导的基因转录活性增加。PDE4的选择性抑制剂Rolipram可以恢复TGF-β刺激下肾系膜细胞中的NLS-cAMP信号,减轻糖尿病(db/db)小鼠肾脏纤维化。
综上所述,本研究利用基因编码的FRET生物传感器探究DN肾脏肾系膜细胞中的区域化cAMP信号传导,揭示了肾系膜细胞中核β1-AR/cAMP微域通过激活YAP促进肾脏纤维化进展。通过抑制磷酸二酯酶4可以减轻DN肾脏功能紊乱及系膜基质沉积。总之,本研究定义了DN肾脏肾系膜细胞中一个核定位cAMP信号调节的时空范式,揭示了在肾系膜细胞中通过β1-AR/cAMP/YAP信号轴调控肾脏纤维化,提供了一种新的精准治疗DN的治疗策略。
南方科技大学王莹课题组2024级博士生向文静为该论文的第一作者。同时,该研究得到了国家自然科学基金(82470293, 32300948和82070406)资助。
原文链接:
https://bpspubs.onlinelibrary.wiley.com/doi/10.1111/bph.17347
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#糖尿病肾病# #肾脏纤维化#
18