Radiology:来自多参数MRI的AI衍生肿瘤体积和局限性前列腺癌的预后评估
5小时前 shaosai MedSci原创 发表于上海
近年来,深度学习算法在检测具有临床意义的前列腺癌方面的表现已经接近经验丰富的放射科医生。最近有报道称,深度学习算法有潜力在MRI上描绘前列腺内肿瘤,用于局灶外束放射治疗(RT)增强。
现阶段,多参数MRI彻底改变了局部前列腺癌的治疗。MRI引导下的活检可以提高临床显著性疾病的检出率,同时降低临床不显著性疾病的检出率。此外,前列腺内肿瘤的MRI特征,包括前列腺成像报告和数据系统(PI-RADS)评分、放射学T分期和病变大小。
然而,这些特征受制于观察者之间的可变性。例如,多读者研究报告了PI- RADS 2.0版本评分报告中观察者之间的差至中等差异。最近在26个中心进行的一项研究表明,PI-RADS评分对至少为3+4的前列腺癌Gleason评分的阳性预测值很低(35%)且可变。此外,存在多种分级系统用于分配前列腺外扩展,每种分级系统在确定组织学前列腺外扩展程度时具有不同的敏感性。MRI表现变化的原因可能是多因素的,部分归因于技术和解释因素,以及类似恶性肿瘤的良性条件。
MRI的临床应用可以通过人工智能(AI)分割算法得到改善,该算法具有以一致的方式评估图像的潜力。近年来,深度学习算法在检测具有临床意义的前列腺癌方面的表现已经接近经验丰富的放射科医生。最近有报道称,深度学习算法有潜力在MRI上描绘前列腺内肿瘤,用于局灶外束放射治疗(RT)增强。

最近,发表在Radiology 上的一篇文章评估了人工智能生成的前列腺内肿瘤的总体积(VAI)为接受放射治疗(RT)或根治性前列腺切除术(RP)的局限性前列腺癌患者提供的附加预后价值。
本项回顾性单中心研究(2021年1月至2023年8月)评估了进行MRI并接受RT或RP治疗的cT1-3N0M0前列腺癌患者。接受RT治疗的患者随机分为交叉验证组和测试RT组。在为测试RT组和RP组提供分割之前,训练AI分割算法来描绘交叉验证RT组中的前列腺成像报告和数据系统(PI-RADS) 3-5个病变。使用Cox回归模型评估VAI与转移时间之间的关系,并对联合RT(即交叉验证RT和测试RT)和RP组的临床和放射学因素进行调整。计算患者工作特征曲线下面积(AUC),用于VAI和国家综合癌症网络(NCCN)风险分类,并预测5年转移(RP组)和7年转移(联合RT组)。
研究共纳入732例患者(联合放疗组,438例;RP组294例)。联合放疗组和联合放疗组的中位年龄分别为68岁(IQR, 62-73岁)和61岁(IQR, 56-66岁)。在联合放疗组中,VAI与转移相关(中位随访时间为6.9年;校正风险比[AHR],AHR 1.09;95% ci: 1.04, 1.15;P = .001)和RP组(中位随访时间,5.5年;AHR, 1.22;95% ci: 1.08, 1.39;P = .001)。VAI和NCCN风险类别联合RT组7年转移AUC分别为0.84 (95% CI: 0.74, 0.94)和0.74 (95% CI: 0.80, 0.98) (P = 0.02)。RP组VAI和NCCN风险类别的5年AUC分别为0.89 (95% CI: 0.80, 0.98)和0.79 (95% CI: 0.64, 0.94) (P = 0.25)。
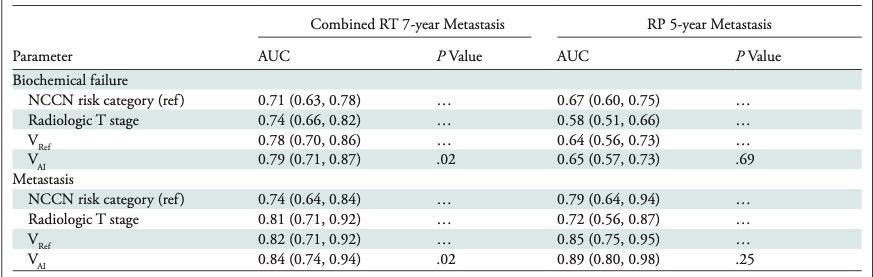
表 生化治疗失败和转移的AUC
本项研究表明,人工智能提供的病灶体积是局部前列腺癌的独立预后因素。
原始出处:
David D Yang,Leslie K Lee,James M G Tsui,et al.AI-derived Tumor Volume from Multiparametric MRI and Outcomes in Localized Prostate Cancer.DOI:10.1148/radiol.240041
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#前列腺癌# #多参数MRI#
2