Nature子刊:少吃蛋白质,尤其这种,高蛋白饮食或促进心血管疾病
2024-02-22 医诺维 医诺维 发表于上海
该研究显示,高蛋白饮食可能会增加动脉粥样硬化的风险,促进心血管疾病。
饮食是多种慢性疾病、过早死亡,以及健康衰老的重要因素。尤其是,蛋白质的摄入对于维持健康起着重要作用。高蛋白摄入在西方社会很常见,并且经常被提倡为健康生活方式的一部分,维持氮平衡的推荐蛋白质摄入量为0.8克每千克每天,约占总能量需求的11%。然而,观察性研究显示,高蛋白摄入量与心血管疾病死亡率增加有关。
2024年2月19日,美国匹兹堡大学医学院的研究人员在" Nature Metabolism "期刊上发表了一篇题为" Identification of a leucine-mediated threshold effect governing macrophage mTOR signalling and cardiovascular risk "的研究论文。
该研究显示,高蛋白饮食可能会增加动脉粥样硬化的风险,促进心血管疾病。人体试验、小鼠实验、细胞实验发现,从蛋白质中摄入的能量超过总能量的22%时,会导致免疫细胞的激活增加,这些细胞在血管壁内堆积,从而导致疾病的发生。
此外,研究还发现,亮氨酸是巨噬细胞中mTOR信号传导的关键激活剂,在驱动与动脉粥样硬化方面发挥着不成比例的作用。研究证明了高蛋白质饮食对心血管疾病风险产生不利影响的机制。

在这项研究中,研究人员进行了两项临床实验,以研究膳食蛋白质消耗与人类单核细胞或巨噬细胞中氨基酸-mTOR-自噬途径的氨基酸特异性之间的剂量反应关系。
在第一项研究中,研究人员通过比较含有10%或50%蛋白质能量对单核细胞中mTORC1通路激活的影响来检查蛋白质消耗极限。在第二项研究中,使用一个更“真实世界”的场景,评估了接受标准蛋白质膳食或含有更多蛋白质的混合膳食(15%千卡与22%千卡)的参与者的这些结果。
该研究集中分析了CD14+、CD16-单核细胞,因为它们在循环单核细胞中占最大比例,并且最有可能发展成动脉粥样硬化巨噬细胞。
此外,还分析了14名超重参与者,在12小时过夜禁食后进行了两次调查,一次食用低蛋白饮食,10%的能量来自蛋白质,另一次食用高蛋白饮食,50%的能量来自蛋白质。在进食前、进食后1小时和3小时收集血样,以确定血浆氨基酸浓度并分离单核细胞。
研究发现,急性高蛋白摄入会诱导单核细胞mTORC1激活和自噬的相互抑制。
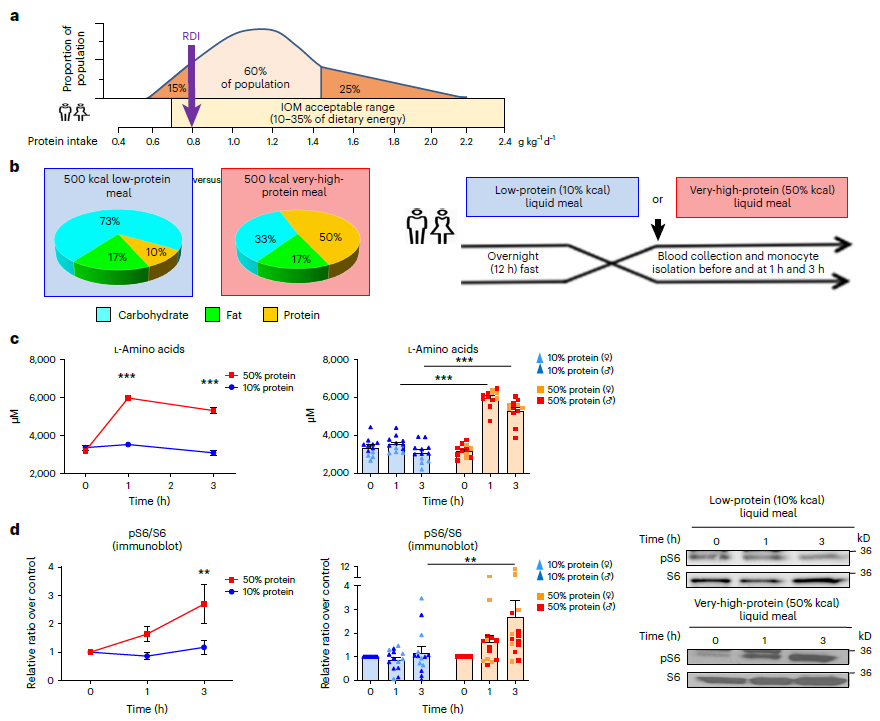
而第二项实验发现,只有每餐摄入25克以上的蛋白质才能激活mTOR并产生功能性影响,从蛋白质中摄入的能量超过总能量的22%时,会触发人类单核细胞和巨噬细胞中有害的氨基酸-mTORC1-自噬信号通路,从而导致雄性小鼠动脉粥样硬化。
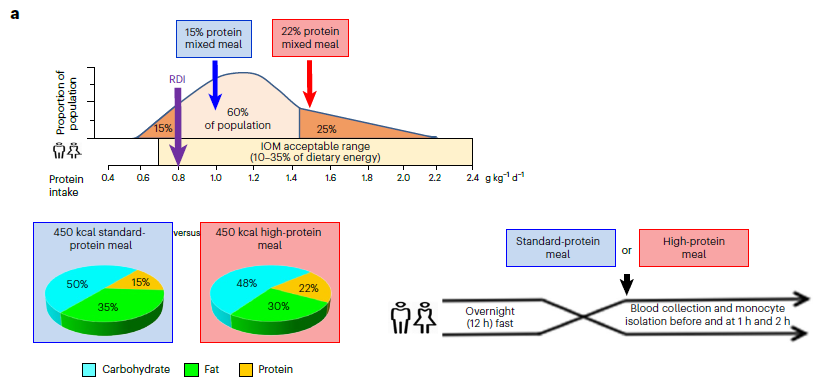
最后,研究还发现,亮氨酸是巨噬细胞中mTOR信号传导的主要激活剂,与0.8克每千克每天蛋白质相比,1.6克每千克每天蛋白质可导致更高的mTORC1激活。
研究发现,高蛋白摄入与动脉粥样硬化性心血管疾病风险之间存在密切联系,这表明饮食建议和治疗措施的可能性。研究表明,增加饮食中的亮氨酸对于在体内产生高蛋白饮食的促动脉粥样硬化作用是必需的,也是足够的。
研究人员表示,我们希望这项研究能够引发一场关于如何以精确的方式改变饮食的讨论,从而在分子水平上影响身体功能并降低疾病风险。
总而言之,结果表明,高蛋白质饮食,特别是通过升高血浆亮氨酸,可能会抑制单核细胞和巨噬细胞中mTORC1介导的自噬和动脉粥样硬化形成。
从蛋白质中摄入的能量超过总能量的22%时,会对负责清除细胞碎片的巨噬细胞产生负面影响,导致这些细胞在血管壁内堆积,从而产生动脉粥样硬化。
论文链接:
https://doi.org/10.1038/s42255-024-00984-2
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#动脉粥样硬化# #高蛋白饮食#
24