JCO:FOR46在转移性去势抵抗性前列腺癌中的应用,一种新型免疫调节抗体-药物偶联物的首次人体研究
2025-03-29 daikun MedSci原创 发表于陕西省
该研究旨在评估FOR46在mCRPC患者中的安全性、耐受性和初步疗效,研究结果显示,FOR46在mCRPC患者中表现出令人鼓舞的初步临床活性和可管理的安全性。
转移性去势抵抗性前列腺癌(mCRPC)是一种致命的疾病,尽管近年来治疗手段有所进步,但其仍然是美国和全球癌症相关死亡的主要原因之一。mCRPC通常发生在接受过雄激素信号抑制剂治疗的晚期前列腺癌患者中,这些患者对现有治疗产生了耐药性。目前,针对mCRPC的治疗选择有限,且大多数患者在疾病进展后预后较差。因此,开发新的治疗策略对于改善患者的生存和生活质量至关重要。在过去的几年中,抗体-药物偶联物(ADCs)在其他肿瘤类型中显示出显著的抗肿瘤活性,但在mCRPC中的应用仍然处于起步阶段。CD46是一种在多种肿瘤细胞表面高度表达的分子,尤其是在mCRPC中。CD46的表达与肿瘤的侵袭性和预后不良相关。因此,CD46成为了一个有吸引力的治疗靶点。FOR46是一种新型的ADC,通过将单甲基auristatin E(MMAE)有效载荷与特异性结合CD46的抗体YS5偶联而成。这种设计旨在通过靶向CD46来杀死肿瘤细胞,并可能引发免疫反应,从而增强治疗效果。

方法
本研究是一项I期、首次人体剂量递增/扩展试验,旨在评估FOR46在mCRPC患者中的安全性、耐受性和初步疗效。研究在美国的六个研究中心进行,纳入了在接受至少一种雄激素信号抑制剂治疗后病情进展的患者。研究分为剂量递增和剂量扩展两个阶段。剂量递增阶段采用加速滴定和3+3设计,起始剂量为每3周0.1 mg/kg。剂量扩展阶段则进一步评估FOR46在不同剂量下的疗效和安全性。研究的主要终点是确定FOR46的最大耐受剂量(MTD)。次要终点包括不良事件、药代动力学、复合缓解率、PSA50响应率、客观缓解率和无进展生存期。为了评估免疫反应,研究还使用了全血质谱细胞术来分析外周免疫反应和CD46在CRPC组织中的表达。
研究结果
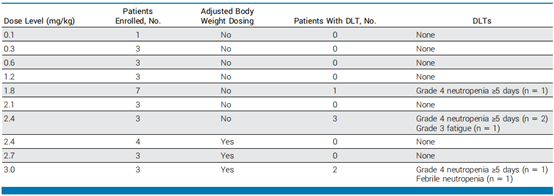
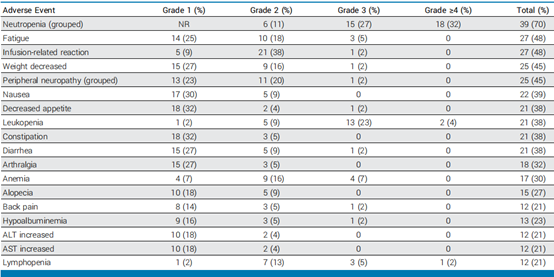
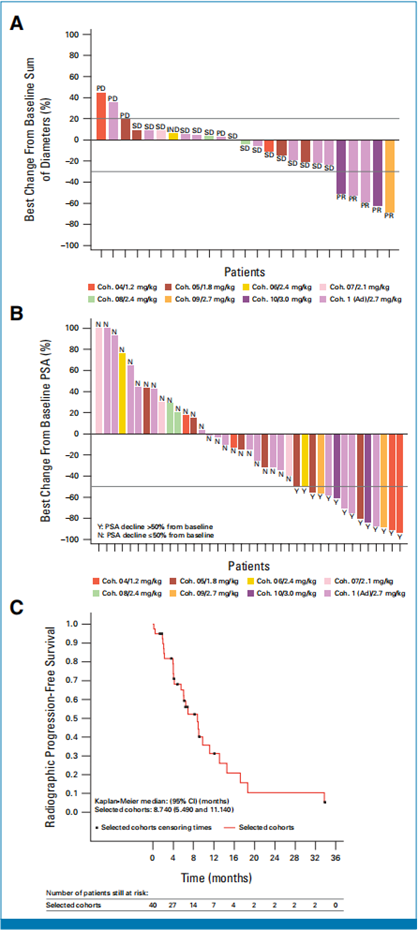
在研究的56名患者中,剂量限制性毒性(DLTs)包括中性粒细胞减少症(n=4)、发热性中性粒细胞减少症(n=1)和疲劳(n=1)。通过调整体重,确定了FOR46的MTD为2.7 mg/kg。最常见的≥3级不良事件包括中性粒细胞减少症(59%)、白细胞减少症(27%)、淋巴细胞减少症(7%)、贫血(7%)和疲劳(5%)。在疗效可评估的患者中(n=40),中位无进展生存期为8.7个月(范围0.1-33.9个月)。39名可评估患者中有14人(36%)实现了PSA50响应。在RECIST可评估的患者中,确认的客观缓解率为20%,中位缓解持续时间为7.5个月。响应者的治疗期间循环效应CD8+ T细胞的频率显著较高。
结论
FOR46在mCRPC患者中表现出令人鼓舞的初步临床活性和可管理的安全性。CD46靶向治疗引发了免疫启动效应,与临床结果相关。尽管研究中观察到了一些不良事件,但大多数患者能够耐受治疗。FOR46的中位无进展生存期与其他标准治疗相比具有竞争力,表明其在mCRPC治疗中的潜力。
原始出处
Aggarwal RR, et al. 2025. Phase I, First-in-Human Study of FOR46 (FG-3246), an Immune-Modulating Antibody-Drug Conjugate Targeting CD46, in Patients With Metastatic Castration-Resistant Prostate Cancer. Journal of Clinical Oncology 0:JCO-24-01989.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#mCRPC# #FOR46# #首次人体研究#
5