丁培荣教授:MSI-H结肠癌免疫治疗的临床实践以及思考
2024-09-03 肿瘤医学论坛 肿瘤医学论坛 发表于上海
本次肿瘤医学论坛特开设了精准精进结直肠治疗新策略为主题的系列公开课,并邀请中山大学肿瘤防治中心丁培荣教授给大家分享关于MSI-H结肠癌免疫治疗的一些临床实践以及思考。
导语:
为了响应国家2030年健康中国的号召,推进健康中国建设,提高人民健康水平,助力结肠癌规范化诊疗能力的提升,助力结肠癌专科发展,本次肿瘤医学论坛特开设了精准精进结直肠治疗新策略为主题的系列公开课,并邀请中山大学肿瘤防治中心丁培荣教授给大家分享关于MSI-H结肠癌免疫治疗的一些临床实践以及思考。
免疫治疗在dMMR肠癌的疗效差异——跨研究观察
免疫治疗是MSI-H结直肠癌的一个非常敏感优势的治疗手段,但是在仔细地去对比观察不同的MSI-H免疫治疗的这些研究,我们会有一个非常有意思的发现——不同的研究之间使用免疫治疗的ORR其实差别很大,从30%到60%,差别有一倍之多,那我们再换个角度来观察这些研究之间有什么异同,结果我们会发现不同的研究之间的PFS其实差别也非常大,最好的是CHECKMATE142的研究,它的三年的PFS接近80%,而KEYNOTE-177研究三年的PFS只有42%。虽然是跨研究之间的比较,可能不是那么可靠,但是差别这么大的PFS还是给我们一些提示的。
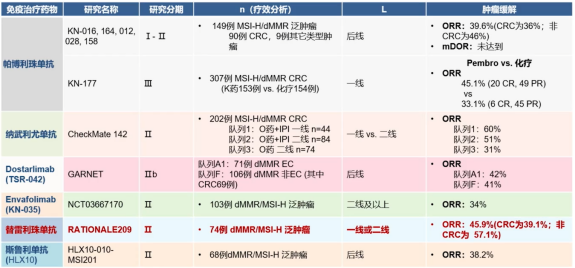
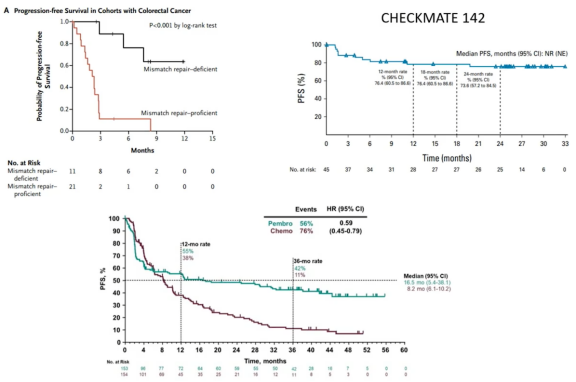

这些不同研究之间有一些相似的地方,有一部分患者可以获得非常持久的应答,在一线使用这个治疗手段比后线要更好。有一部分患者可能会在治疗的早期出现肿瘤的进展,不同的地方在于KEYNOTE-177研究的ORR跟DFS显著地低于其他的研究,同时,有一部分患者在治疗中或者停药后出现肿瘤的进展,那这一发现对我们的临床实践有什么样的启发呢?
第一点我们可以看到这种持久的应答意味着这些患者在停药之后仍然是无瘤生存的,因此有可能通过免疫治疗手段就获得了治愈的机会。那我们在临床实践中强调每一例MSI-H的患者都应该以治愈为目标。不仅如此,还要追求无化疗的生存。这对患者意味着什么呢?意味着花更少的钱,意味着更少的社会医疗的消耗,意味着他有更好的生存质量和自我的社会意识。
而在肿瘤治疗的早期出现进展提示有些患者是存在原发性耐药的现象,因此我们要去采用一些创新方法去克服原发性耐药,而KEYNOTE-177研究的ORR、PFS显著低于其他研究,提示我们在入组的时候,这种人群筛选的准确性非常重要,只有我们做到准确的筛选,这些进入免疫治疗研究的患者才能够从这个治疗手段里面获益。在治疗中或者停药后出现进展也提示这些患者存在继发性耐药的现象,那我们也要想方设法去消除这些继发性耐药的病灶。
一、每一例MSI-H都应以治愈为目标
病例1.免疫治疗停药2+年NED
此病例是一个36岁的年轻男性转移性结直肠癌患者。二线治疗失败,准备进入三线治疗,但是来找我重新看了之后,我发现他是林奇综合征筛查的dMMR的患者,那么像这样的一个患者,我们知道虽然在17年2月份的时候国内是没有药物的,没有PD-1抗体,但是在香港这个药物已经上市,因此我给他提供了这个信息,最后他也接受我们建议去接受了这个免疫治疗。
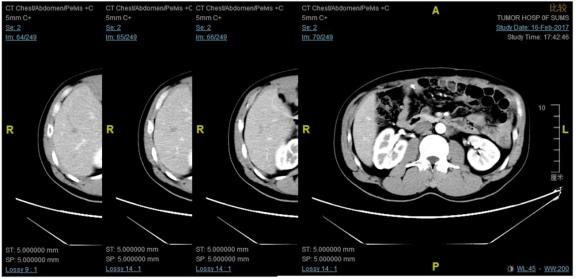
男性,36y,转移性结肠癌二线治疗失败,dMMR
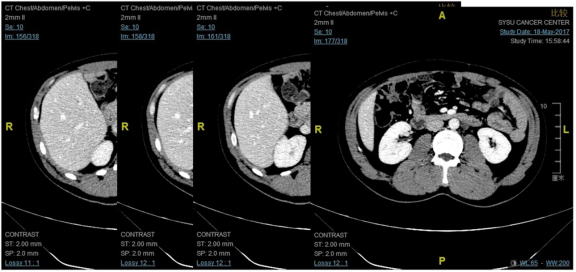
PD-1抗体治疗2017-02-28至2017-05-08
4疗程100mg每3周一次
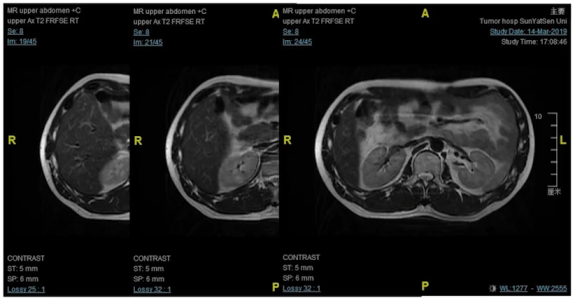
2019-03停药;2021.12随访NED
这些图片展示的是治疗之前腹膜后淋巴结多发的肿大,比较广泛,有融合。治疗3个月之后,腹膜后的淋巴结已经是基本消失,达到了临床完全缓解状态。治疗两年之后停药,在最近的一次复查2022年6月份仍然是一个NED状态,而且非常有意思的是,在停药一年多之后还生了一个非常健康的宝宝。这个是我们提倡的非常重要的目标,其实我们治疗过的患者比这个晚期的有很多,有一些是躺着进来的MSI-H的病人,经过我们积极治疗,完全回归到正常生活的病例也非常多。
病例2.
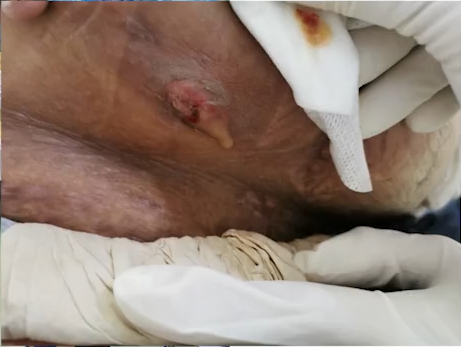
像这样的一个23岁非常年轻的患者,在全国4个省市的四五家大医院做了治疗,肿瘤仍然是持续进展的,初诊的时候肿瘤侵犯到腰大肌腹壁,穿透到腹壁外面,发热感染。这个患者在其他的病友的指导下找到我们,来了之后,我们给他做了一个综合的治疗,为他创造了一个接受免疫治疗的机会。
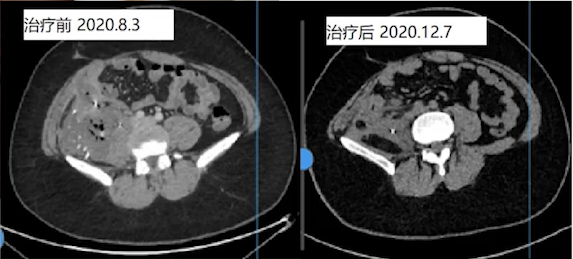
在治疗三个月之后,可以看到这个肿瘤已经得到非常好的缓解了。因为患者仍然是无法像正常一样走路,只能是趴着,依靠这个轮椅来生活,我们讨论准备给他做手术,切除病灶,让他能够恢复接近正常地走路。
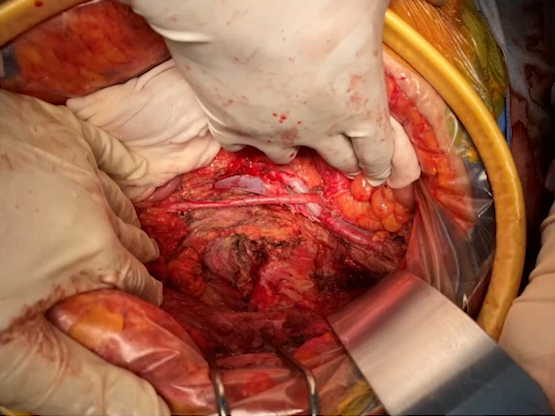
23岁林奇综合征,盲肠癌术后复发多线化疗及介入治疗后免疫治疗后R0切除,回结肠吻合口+腰大肌、髂腰肌+腹壁切除
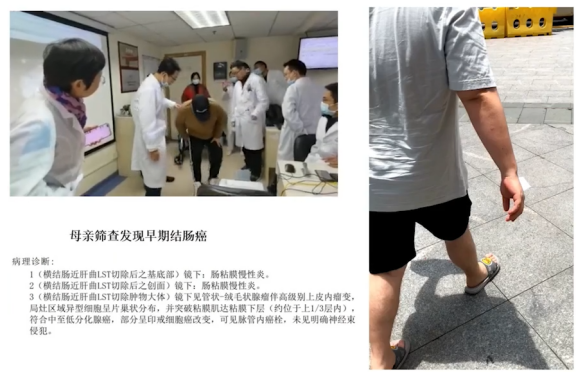
这个是患者手术后一个多月的情况,可以看到他虽然还是有一瘸一拐,但是基本可以不用轮椅了,最近他妈妈发的视频已经看不出这种一瘸一拐的这种情况了。非常有意思的是我们没有把眼光仅仅放在这个小孩,他治疗到肿瘤控制非常好的情况下,我们又提醒他的妈妈去做了筛查,结果发现他妈妈是一个非常早期的结肠癌,做了个手术就没事了。
二、克服原发耐药
(一)进一步精准筛选获益人群MMR/MSI不一致时疗效差,主要原因是检测不准确
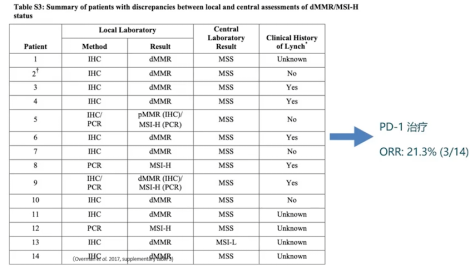
1.原发性耐药大多数情况下是因为检测的不准确或者不一致,在CheckMate 142的PI做的这个研究中,14例患者在地方医院检测是MSI-H或者dMMR,但在中心实验室是不一致的,结果发现这组患者用PD-1抗体的ORR只有21%[1],这比大多数研究的ORR低,这提示我们在治疗之前的检测上要做到更加全面,更加细致。
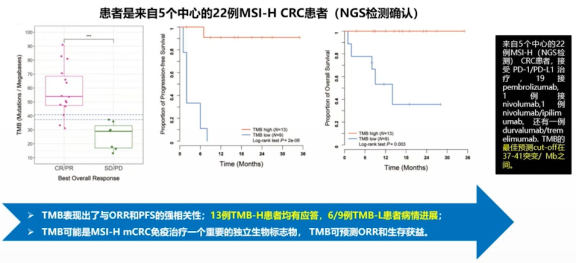
同样的,在MSI-H的人群里面,我们要进一步区分肿瘤突变负荷水平,也能够去筛选获益可能性更大的人群。这个是19年Annals of Oncology的一项研究[2],样本量虽然不大,但是效果非常好。如果是在MSI-H人群的TMB最佳预测cut-off在37-41突变/MB的,这种情况下这些患者基本上都能获益。而如果TMB水平低的,那么这些患者获益的可能性是比较小的。
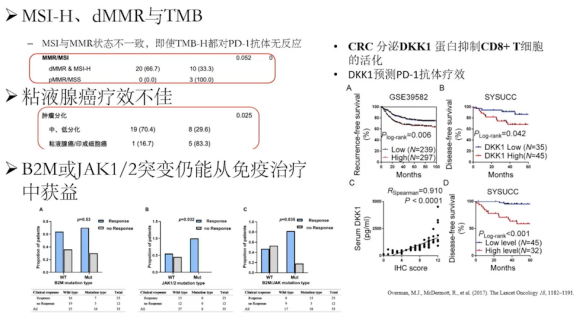
中肿这一两年也针对自己的数据做了一些研究,有一个非常有意思的现象——MSI跟MMR以及TMB这三个参数,如果有一个参数是不一致的,那免疫治疗疗效是不好的。比如说MSI跟MMR状态不一致,即使TMB水平很高,这种情况下的免疫治疗疗效也是不好的[3]。
2.粘液腺癌疗效也是很不好的,这是非常有意思的,不仅是我们发表的这个研究,我们有一个转化性研究是发在nature communications上面,样本量更大,也同样显示粘液腺癌对免疫治疗的疗效是不好的。
3.像B2M突变或者JAK1,JAK2的突变,在黑色素瘤或者是肺癌里面,有研究认为它是一个原发性耐药的突变,这种情况下这些患者可能不能从免疫治疗里获益,但是非常有意思的是在MSI-H的结直肠癌中,B2M或者JAK1、JAK2的突变,患者仍然能够从免疫治疗里面获益,这一点是值得我们注意的。
4.其他的一些靶点,比如说DKK1,一个分泌性蛋白,跟CD8+T细胞的活化是有关的[4]。通过我们的分析发现DKK1这个分泌蛋白的水平跟免疫治疗疗效也有非常密切的关系,我们正在做更大样本量的验证。
(二)联合治疗
第二个大的方面是我们有没有什么方法可以克服原发性耐药呢?这个目前为止其实没有太多的数据,只有这些零星个案的报道,但是我们通过跨研究的比较发现一个问题,像CHECKMATE142研究,双免疫的治疗的ORR是更高的,并且是在所有的MSI-H肠癌的免疫治疗里面的ORR最高的,比单免疫的治疗有高接近一倍之多[5]。
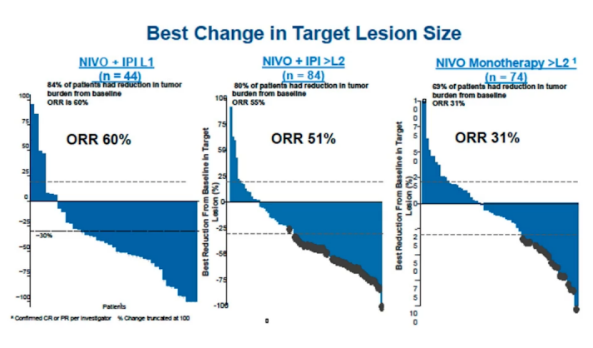
因此这个跨研究的比较也提示我们双免疫治疗联合有可能对一些发生原发耐药的人群来说能够降低原发耐药的风险,这些人群就包括刚才讲的MMR或者MSI的状态不一致,或者是粘液腺癌等这些病例,这些肿瘤的突变负荷非常高的情况下,我们可以考虑双免疫治疗的策略来降低原发性耐药的风险。
三、克服继发耐药:局部治疗的及时介入
病例3.
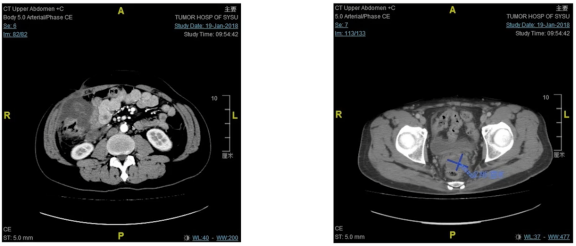
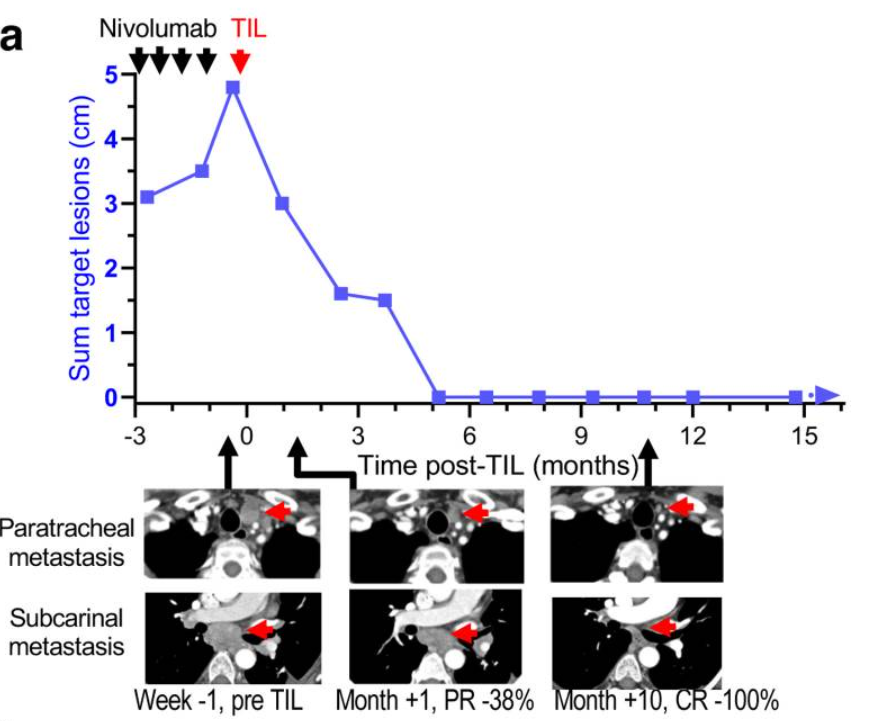
MSI-H结肠癌一二线化疗后进展,PD-1抗体免疫治疗15个月肿瘤显著退缩,但仍有可见病灶,近半年肿瘤未在退缩
这个病例是一个MSI-H的患者,伴有腹腔、腹膜后转移者,初始做了一二线的治疗,肿瘤持续进展,溃破到腹壁啊。到我们这里之后,我们确定他是个MSI-H的病人,给他做PD-1抗体治疗了15个月,这个是治疗15个月的肿瘤的情况,看起来已经好了很多,但是仍然有可见的病灶,我们按照目前的常用的治疗的时间周期准备治两年的时间,但是在治疗半年之后,我们可以看到这个肿瘤仍然是存在的,仍然可见,退缩不是特别明显。
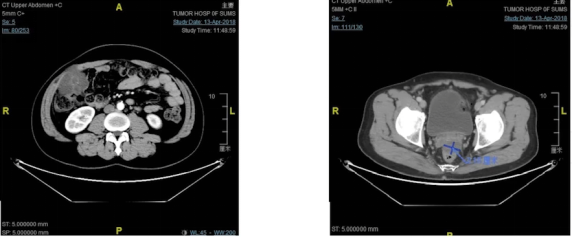
因此我们推测它可能存在一些继发耐药的病灶,所以我们给它做了一个大的手术,达到了R0切除。我们做了右半结肠切除+DIXON+腹壁部分切除+腹膜后中午切除+小肠部分切除+左精囊腺切除+回肠造瘘术,腹膜后的淋巴结跨挂在左侧肾静脉的前方,切除了差不多鸡蛋大小,结果大多数病灶还是有肿瘤细胞的残留,那么也印证了我们的推测。
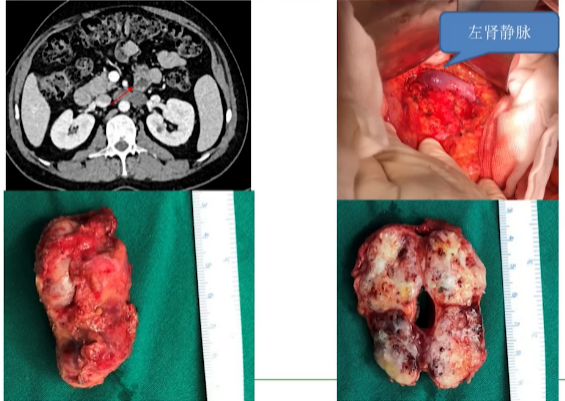
右半结肠切除+DIXON+腹壁部分切除+腹膜后中午切除+
小肠部分切除+左精囊腺切除+回肠造瘘术

术后病理:证实肿瘤残留
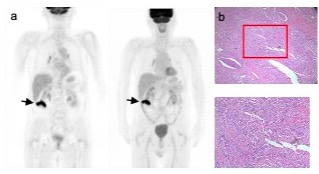
这个患者非常有意思的是,在做了这个手术之后不到一年的时间,又出现肿瘤标志物升高,我们做了PET-CT,发现主动脉跟腔静脉之间有一个高代谢,所以我们考虑这个淋巴结是我们第一次手术时,因为手术很大,所以没有做系统性的腹膜后淋巴结的清扫,有可能是当时的漏网之鱼,于是我们下定决心给他做了一个系统性的腹膜后淋巴结的清扫。那清扫的结果也证实这是一个转移的淋巴结。这个患者后面就没有再继续做其他的治疗,一直观察到现在已经是两年多,仍然是处于一个NED的状态。因此我们可以看到这样的一个及时的介入为这些非常晚期的患者消除了继发耐药病灶,达到NED而长期生存。因此我认为我们要非常密切地监测,该出手的时候就出手。
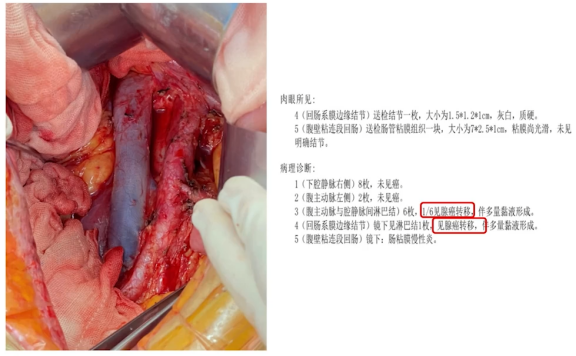
2020.7腹膜后淋巴结清扫术后,至今NED
矛盾现象:影像学评价与病理不一致
我们在临床实践中也观察到一些矛盾的现象,比如说一些转移瘤在免疫治疗之后是存在影像学的评价跟病理不一致的情况。
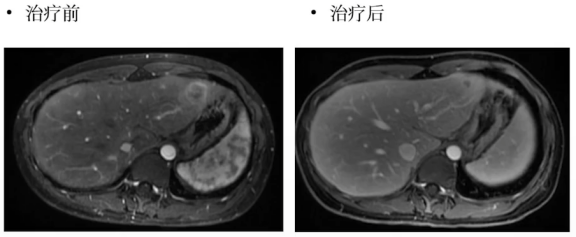
结肠癌术后肝多发转移,Lynch,PD-1抗体5程,pCR(2018)
这是一个非常年轻的林奇综合症的患者,出现了肝的多发转移,左边是治疗前,右边是治疗之后,可以看到免疫治疗让这个患者的病灶得到显著的退缩。但是这一些病灶仍然是影像学可见的,所以我们按照当时18年截止到今天,其实可能仍然是这样的一个治疗策略,把这些可见的病灶做了手术切除,非常意外的是它就是病理的完全缓解pCR。
这样的现象其实在2021JNCI一个权威的肿瘤学杂志中,MD Anderson Cancer Center的CHECKMATE142的PI团队也报道了一个类似的现象,在这里面总共有14例的患者,13例是转移性的结直肠癌[6]。
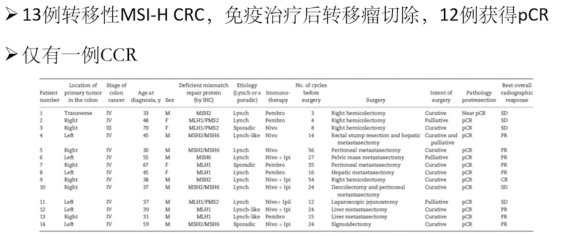
在免疫治疗肿瘤退缩之后,进行了转移瘤的切除,结果这有12例达到了一个pCR的状态,在这12例里面,只有一例临床评价是一个cCR,没有病灶的。因此这个作者提出了这MSI-H的转移性结肠癌免疫治疗退缩之后很可能不需要做局部治疗,那是不是真的是这样子呢?我们刚才那个病例跟这个现象就不一致,因此我们提出了这个疑问。MSI-H转移性结直肠癌治疗后需不需要局部治疗?
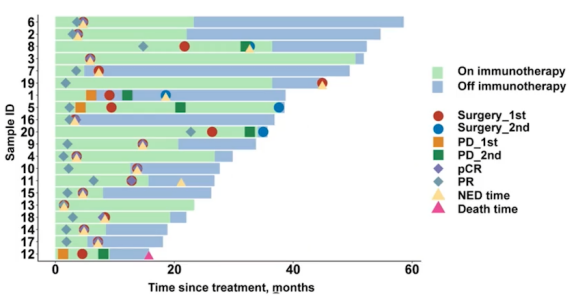
20例MSI-H mCRC免疫治疗后手术,40%见肿瘤残留
提出这个疑问之后,我们对自己的病例又做了一些研究。在我们的研究的20例里面,做了免疫治疗之后去做手术,其实有40%出现肿瘤残留。当然这里面有两例我认为可能是不合适的,因为他们免疫治疗之后,肿瘤是没有很明显退缩就去做手术。那我们最近收集全国多中心近40例患者,发现其实残留的比例虽然没有40%那么高,但也仍然不低。因此MD Anderson的这个研究的结论是值得商榷的,我们要非常慎重,希望这个研究结果尽早出来可以跟大家做一个分享。
四、克服局灶耐药:局部治疗的及时介入
其实局灶性耐药以前是没有关注的,但是我们在临床实践过程中观察到了一个非常有意思的现象。
病历4.这是一个35岁女性患者,降结肠癌多发肝转移,林奇综合征。她初始的时候因为自己治疗的延误,没有及时的去治疗,结果出现了病灶的穿孔,在当地医院做了造瘘手术后来到我们这里,确定她是林奇综合征的MSI-H后我们给予免疫治疗。
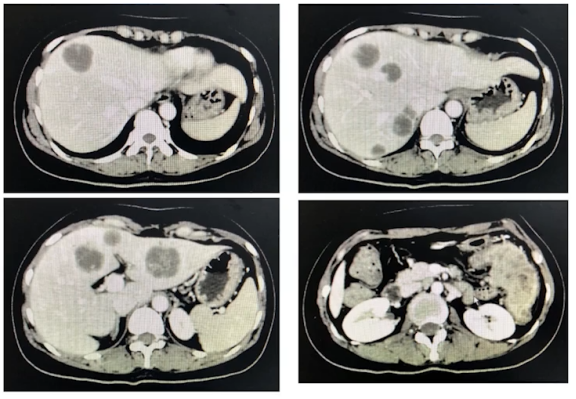
女性,35岁,降结肠癌肝多发转移,
MSI-H,林奇(2019-03)
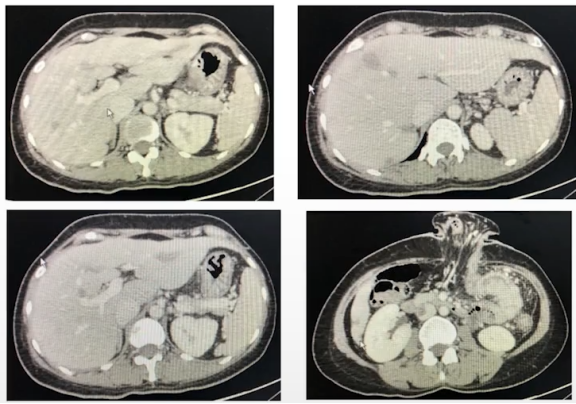
免疫治疗后肝转移瘤显著退缩,原发灶进展(2019-10)
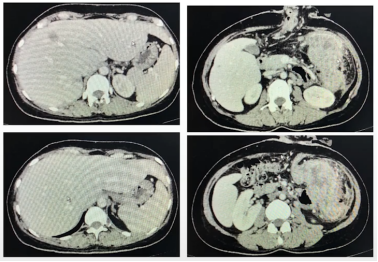
免疫治疗后肝转移瘤显著退缩,原发灶进展(2020-03)
非常有意思的是,免疫治疗之后肝脏的病灶退缩地非常好,基本达到cCR状态,但是可以看到原发灶的右下角没有退缩,反而逐渐增大。所以我们判断它是一个局限性的耐药。那怎么办?我们认为有可能是由于当时穿孔局部炎症反应导致了免疫细胞浸润以及它们的活化杀伤功能受限。所以我们决定给他做手术把这个病灶切掉。
局部治疗的及时介入,获得NED
2020-03-19于行“左半结肠切除+胃部分切除+胰腺部分切除+左肾周脂肪囊切除+空肠部分切除术”,
术后病理:癌组织穿透浆膜层累及空肠浆膜下层及胃黏膜下层,切缘阴性,淋巴结转移(2/26),退缩不良
2021.6 NED状态
我们以这个病例延伸出来做了一个研究,探讨了免疫治疗跟局部炎症状态的关系。这项研究被nature communications接收。这是非常有意思的——病例激发了我们的思考探索,我们的探索又进一步地反馈到临床实践里面。
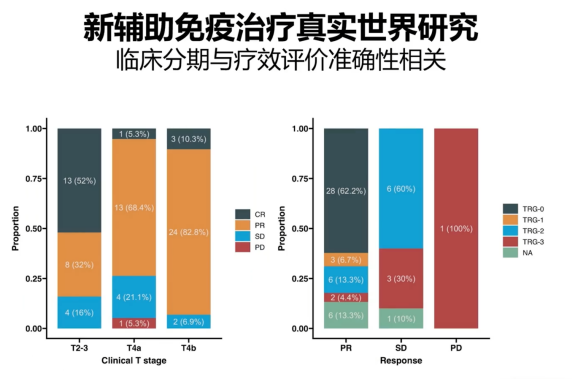
上述所述是晚期病例,而在早中期方面,我们现在知道新辅助免疫治疗的疗效是非常确切的,不管是NICHE研究或者PICC研究,以及这个我们早期的一项8例新辅助免疫治疗研究,都告诉我们新辅助免疫治疗对于MSI-H的优势人群的有效性非常高,pCR率可以接近70%,有效率接近100%,但这样的一种短期的疗效能不能转化成长期的疗效呢?其实目前为止没有研究告诉我们。
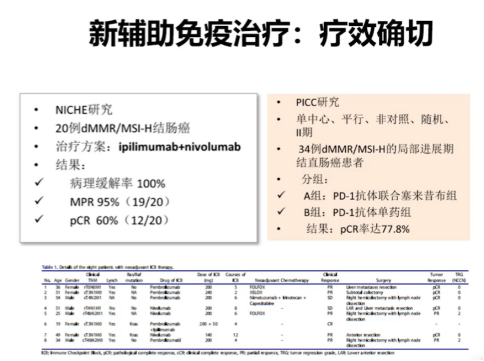
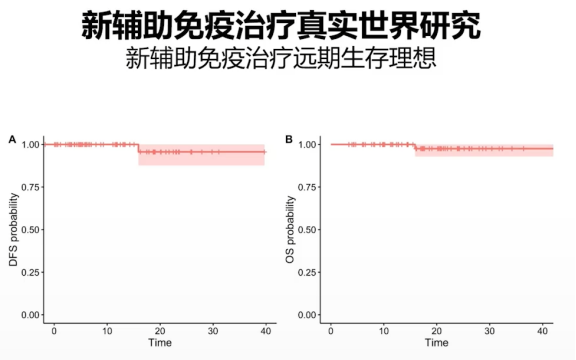
我们2022年做了一项真实世界的研究,收入近80例新辅助免疫治疗的患者,结果发现他们的短期疗效是能够转化成长期生存的,这项研究被JNCCN一个影响因子12分的杂志接收,2023年1月份见刊。我们可以看到生存曲线非常理想。在整个随访过程中只有一例出现复发转移,这一例复发转移的病例是新辅助免疫治疗退缩不良的病例,也告诉我们新辅助免疫治疗的短期疗效能够转化为长期疗效。
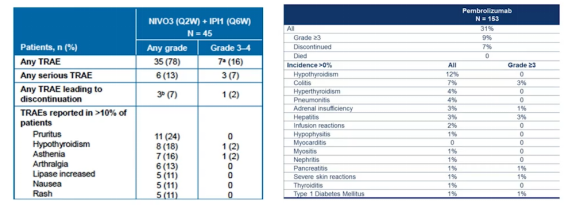
值得我们注意的是,新辅助免疫治疗有不可忽视的终生毒副作用[7],不说新辅助免疫治疗肺炎、心脏毒性、肝炎等等这些致命性的,像对内分泌的影响,对激素水平的影响,比如说甲状腺功能低下,糖尿病这些都会让患者终生用药。因此新辅助免疫治疗非常重要的一点是我们要平衡疗效跟毒性。确定治疗目标究竟是让肿瘤缩小,让手术做得更干净,还是为了获得完全缓解,进行器官功能保全?只有确定了目标,对应的这个目标人群之后,我们才可以给这个患者施加这一个恰当的治疗。
我们非常警惕过度的新辅助免疫治疗。治疗方案方面,目前主流还是单免疫治疗,当然当有一些高危因素,比如说MMR、MSI结果不一致的,或者粘液腺癌,或者是肿瘤负荷很大的情况下,可以考虑双免疫治疗。治疗的时间周期是6周还是12周还是更长时间?根据我们的治疗目标的不同来确定。

实际上我们在临床实践中有一些很好的技巧来识别这些能够从免疫治疗里面获益的人群。如果在临床实践里看到一个大肿瘤,这种情况下其实MSI-H的比例是很高的。我们做了一个研究[8],这个研究非常简单——我们临床中观察到的这些T4b大肿瘤的患者,切除之后是MSI-H的可能性非常高,因此我们收集了268例T4b的结直肠癌,去看这个MSI-H、MMR的比例,结果我们可以看到T4b的结肠癌MSI-H的比例是28%。28%是什么概念呢?普通的非选择性人群d MMR的比例大概是9%到10%,也就是通过这个简单的T4b的指标,我们可以富集三倍的患者。
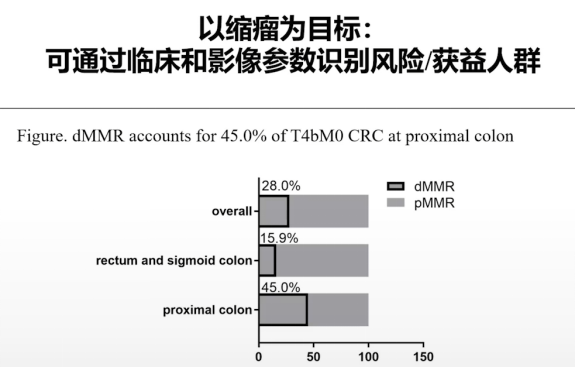
如果我们再把肿瘤的部位加进去——近端结肠癌T4b,那么MSI-H的比例达到45%,也就是通过这两个参数,我们可以富集5倍的MSI-H的病人,而这些患者又刚好是有非常重的新辅助治疗需求的人群。
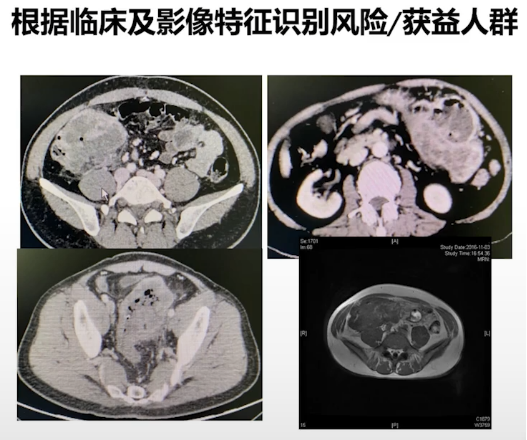
像这四个病例共同特征就是T4b大肿瘤,分子检测全部都是MSI-H的病人,他们全部都做了免疫治疗最后达到了pCR,那么我们进一步的去比较这种新辅助免疫治疗跟传统的直接手术或者是放化疗,可以看到新辅助免疫治疗可以让手术做的更小,安全性更高。
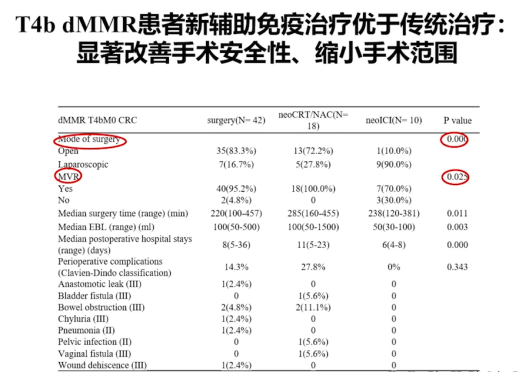
更加重要的是它能够转化成远期的生存获益,我们可以看到如果直接做手术,生存曲线是最差的,做新辅助放化疗居中,而新辅助免疫治疗人群里面没有1例出现肿瘤的复发转移。
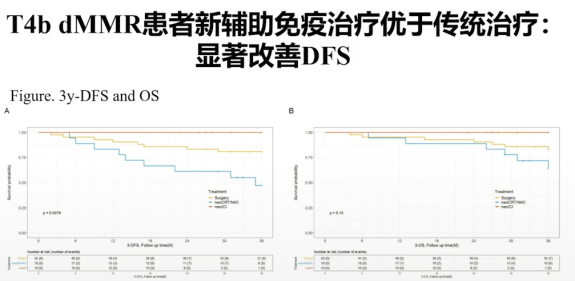
因此我们只需要通过最简单的临床参数就可以识别这一些能够从治疗里面获益的人群,这是一个非常简单的一个技巧。该研究发在Diseases Of The Colon & Rectum——一个结直肠领域的权威杂志。
以器官保全为目标的新辅助免疫治疗
那么我们又进一步思考一个问题,既然免疫治疗对于MSI-H人群疗效那么好,那我们有没有可能把它的这个疗效应用到极致?其实很简单,我们知道新辅助免疫治疗有非常高的pCR率,那我们在新辅助放化疗的领域,当做了放化疗达到cCR的时候,我们可以去观察等待器官保全。那么新辅助免疫治疗是不是也可以借鉴这个概念呢?

病例5.这是我们在19年1月份的一个病例,女性,18岁,非常低位的直肠癌,距肛缘4公分。我们可以看到局部的情况其实非常糟糕,系膜多发的弥漫的淋巴结,环周切缘阳性,侧方淋巴结阳性,EMVI所有的ESMO风险分层里面极高危的特征全部都有。
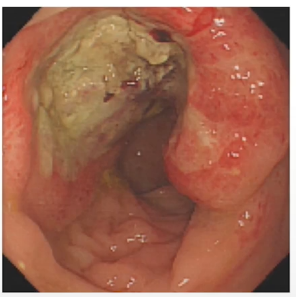
女,18y,T4N2低位直肠癌,dMMR,Lynch PD-1抗体+CTLA-4治疗2程
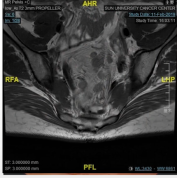
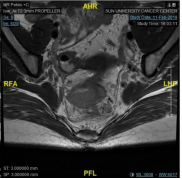
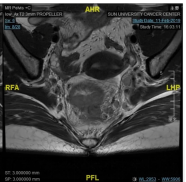
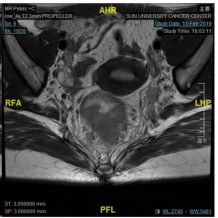
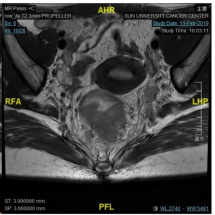
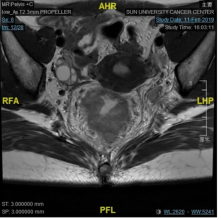
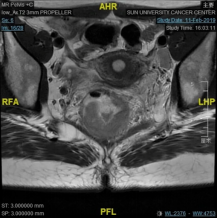
我们知道这个患者如果是按照那个时间点标准治疗应该行新辅助放化疗,这意味着她可能会丧失生育功能,盆腔纤维化,意味着她以后不可能有一个非常满意的家庭生活,但即使按照这个策略去治疗她治愈的可能性不会超过50%。在19年1月份的这个时间点,实际上新辅助免疫治疗没有多少证据,她的家族史也不是很明显,但是我们没有放过这个蛛丝马迹,她非常年轻这个证据,我们还是给她做了筛查,结果发现她是dMMR的林奇综合征。
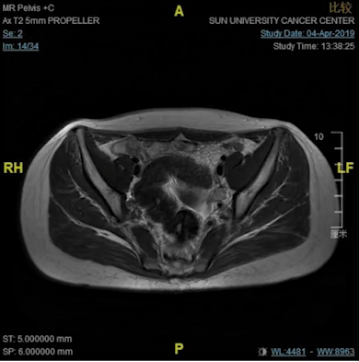
女,18y,T4N2低位直肠癌,dMMR,Lynch(2019.1)
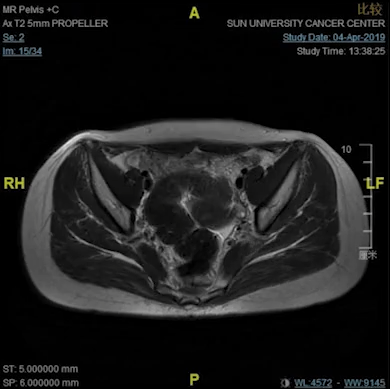
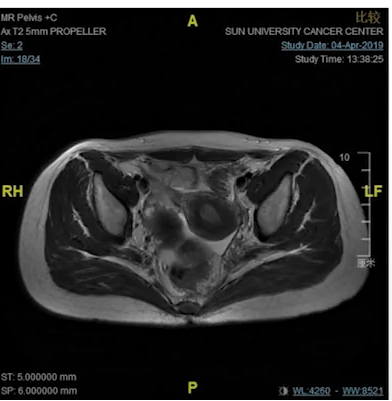
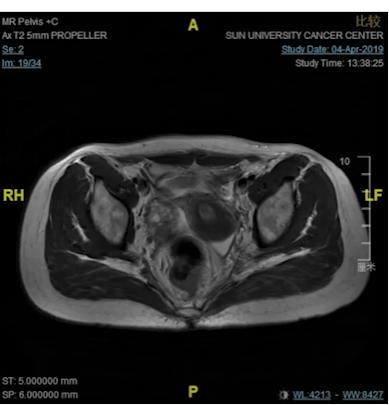
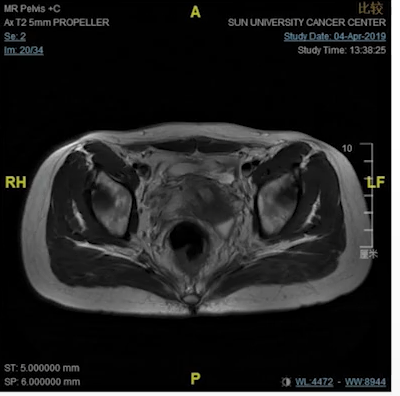
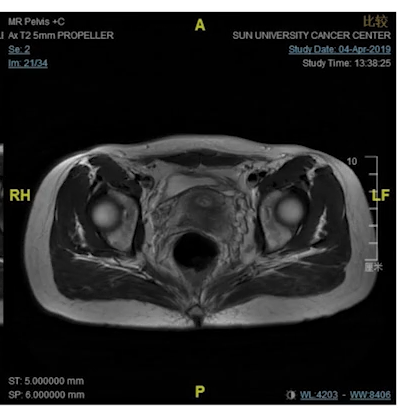
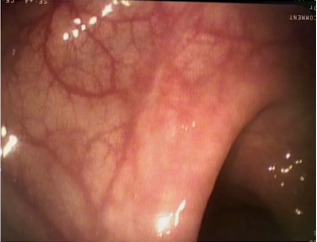
因此我们跟她家人做了非常充分的沟通,因为那个时间点的确证据很少的,我们沟通的一个依据就是在晚期的MSI-H的病人免疫治疗效果非常好,甚至有一部分病人能治愈,实际上对这个小女孩我们是提早的把她当成晚期的病人来治疗,因为局部非常晚期,实际上有潜在的风险转移到其他地方去。最后他们接受了我们的建议,去做了这个治疗啊。我们可以看到六个星期之后肿瘤已经达到临床完全缓解状态了,这三个月之后是确定了一个临床完结缓解,那么这个时间点该怎么办呢?继续给她做手术?还是给她用这种借鉴放化疗之后完全缓解的治疗策略?最后我们非常充分地沟通,选择了做观察等待不做手术。那小女孩一直观察到今天仍然是无瘤生存,像正常人一样生活学习。
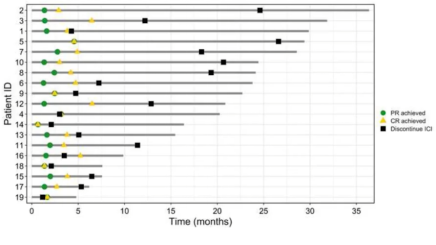
在这个思路的指导下,我们积累了一系列病例,从2021年我们一直在投稿,2022年这个研究终于被接收发在了European Journal of Cancer——一个非常权威的肿瘤学杂志。总共有19例做了新辅助免疫治疗,然后达到cCR没有做手术的个病例中位的随访时间大概18个月,那么没有一例出现肿瘤的复发再生长,这是非常不错的。
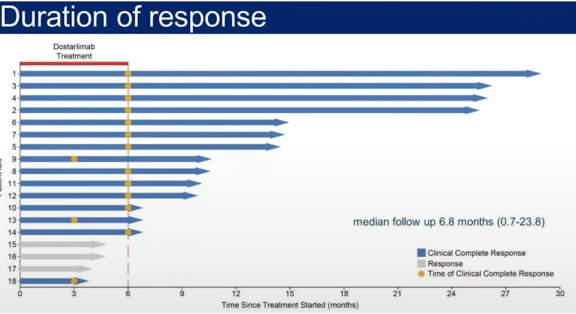
2022 ASCO MSKCC dMMR直肠癌研究
2022年ASCO报道了MSKCC研究,12例做了新辅助免疫治疗,达到cCR观察等待的中位随访时间实际上只有6.8个月,而我们这项研究是一个更大的样本量,更长的随访时间,告诉大家这样的一个方法是可行的,安全的,有效的。
小结
对于晚期MSI-H的结肠癌患者,我们强调每一例MSI-H的病人都应该以治愈为目标,而且要追求无化疗的长期生存,对于一些高危的患者,要考虑使用联合治疗方式来克服原发耐药的风险。在治疗之初,要提高筛选的准确性,有一些检查结果有疑问的,要通过另外一个检测手段去复核。在治疗过程中要及时地监测,如果发现有潜在的继发耐药病灶,要及时地去做局部治疗干预。
对于新辅助免疫治疗,我们强调要平衡好疗效跟毒性,有所为,有所不为。可以通过临床或影像学参数识别风险,筛选能够从新辅助免疫治疗里面获益的人群。对于一些有重要部位器官保全需求的的患者,通过有效的新辅助免疫治疗之后达到完全缓解,是可以做器官功能保全的,不仅治好肿瘤,而且获得正常人一样的生活。
这是我们中山大学肿瘤医院遗传性肠癌工作组团队的一些相关的信息,一直以来都非常关注遗传性肠癌的筛查、免疫治疗和精准治疗,是一个致力于遗传性肠癌防治的团队。大家如果有什么问题,也欢迎随时跟我们交流探讨。
参考文献:
[1] Overman,M.J.,McDermott,R,et al.(2017).The Lancet Oncology 18,1182-1191.
[2] Annals of Oncology 30:1096-1103,2019 doi:10.1093/annonc/mdz134
[3] Journal of Immunotherapy2022
[4] J ImmunoTher Cancer,2021
[5] van Velzen MJM,Derks S,van Grieken NCT,Haj Mohammad N,van Laarhoven HWM.MSI as a predictive factor for treatment outcome of gastroesophageal adenocarcinoma.Cancer Treat Rev.2020;86:102024.doi:10.1016/j.ctrv.2020.102024
[6] Ludford K,Cohen R,Svrcek M,et al.Pathological Tumor Response Following Immune Checkpoint Blockade for Deficient Mismatch Repair Advanced Colorectal Cancer.J Natl Cancer Inst.2021;113(2):208-211.doi:10.1093/jnci/djaa052
[7] N Engl J Med.2015 Jun 25;372(26):2509-20.
[8] Han K,...,Ding PR,Dis Colon Rectum.2022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#结肠癌# #免疫治疗#
75