程颖教授:阿得贝利单抗局限期SCLC研究数据的深入解读
2024-03-26 梅斯肿瘤新前沿 网络 发表于上海
2024年3月欧洲肺癌学术大会(ELCC)在捷克召开,会议中由吉林省肿瘤医院程颖教授牵头开展的阿得贝利单抗联合同步放化疗治疗局限期小细胞肺癌的随机、双盲对照、多中心 III 期临床研究公布了安全导入期
2024年3月欧洲肺癌学术大会(ELCC)在捷克召开,会议中由吉林省肿瘤医院程颖教授牵头开展的阿得贝利单抗联合同步放化疗治疗局限期小细胞肺癌的随机、双盲对照、多中心 III 期临床研究公布了安全导入期数据,安全性与疗效并优,惊艳海内外肺癌学者。

本项研究设计包含两个阶段:第一阶段(图1所示):安全性导入研究;第二阶段:随机对照、双盲III期研究。本次公布的是安全导入研究结果,纳入了28例患者,中位年龄58.5岁(范围:34-73岁),96.4%患者ECOG评分为1分,92.9%临床分期为III期。截至2023年10月31日,中位随访时间为29.4个月(范围:6.5-33.3个月),10例患者完成35周期阿得贝利单抗治疗。安全导入期数据有两大亮点:
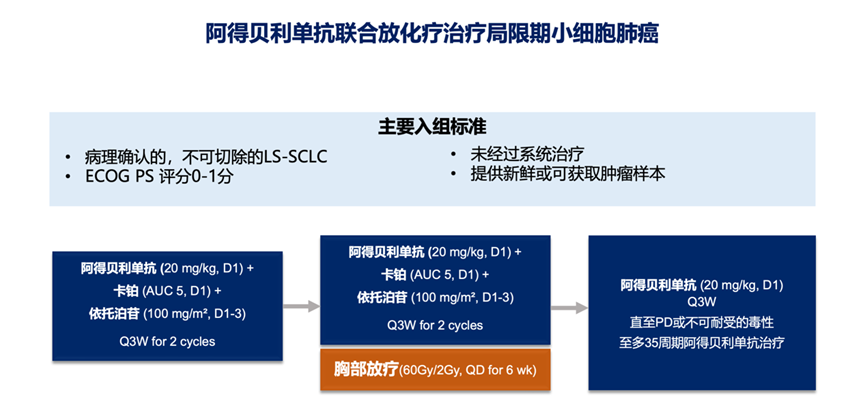
图1. 安全导入期研究设计
亮点1:疗效数据优异:阿得贝利单抗联合放化疗ORR率92.9%,DCR率100%,中位PFS达到了17.9个月(95%CI:8.8- NR),mOS尚未达到,2年OS率达到了64.3%,接近2/3的患者生存突破2年。该研究与局限期SCLC同步放化疗历史疗效数据相比(ORR为75%~80%左右,2年OS率48%~56%左右),阿得贝利单抗联合放化疗的初步疗效已经体现出更好的获益趋势。
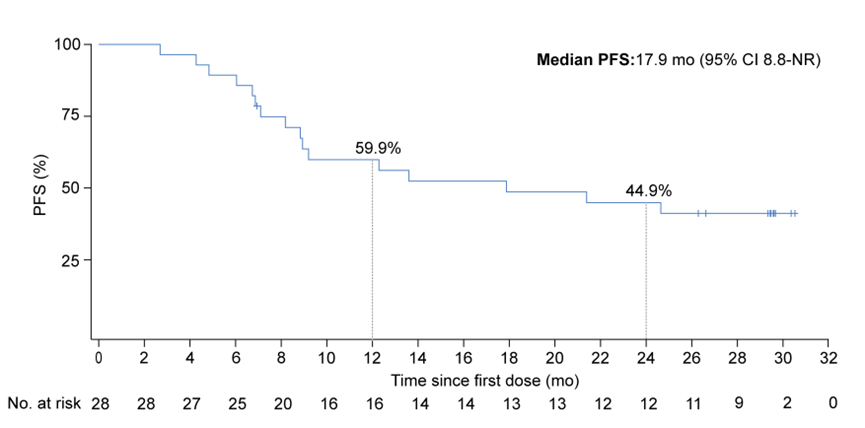
图2 安全导入期PFS KM曲线
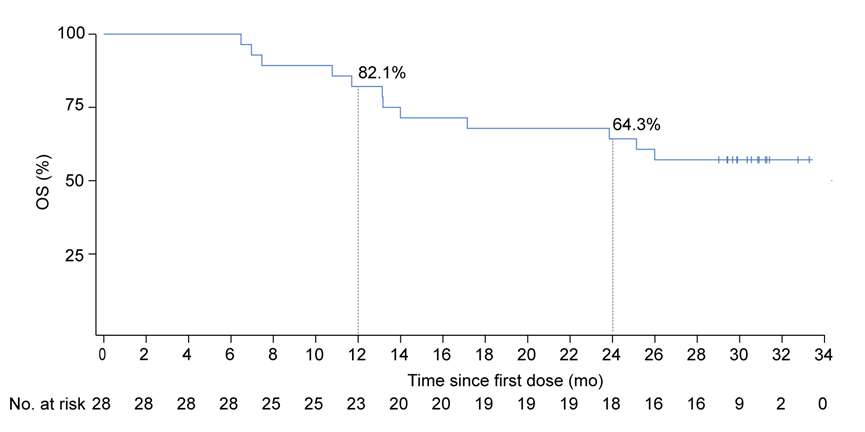
图3 安全导入期OS KM曲线
亮点2:安全性数据卓越:在免疫联合放化疗的治疗模式中,该研究的不良反应谱未发现超出预期的不良反应。发生率≥10%的3级及以上TRAE全部为血液学毒性,无治疗相关的死亡事件。此外,4例(14.3%)患者发生肺炎,仅有1例患者发生治疗相关的免疫性肺疾病(均为2级)。均体现出阿得贝利单抗联合放化疗卓越的安全性。
梅斯医学特别邀请Leading PI程颖教授接受专访,分享研究成果,详细解读阿得贝利单抗联合放化疗治疗局限期SCLC数据公布的重要意义。
专家简介
程颖 教授
一级教授,博士研究生导师,博士后工作站导师
享受国务院特殊津贴,卫生部突出贡献中青年专家
吉林省癌症中心主任
吉林省肺癌诊疗中心主任
中国临床肿瘤学会(CSCO) 副理事长
国际肺癌联盟(IASLC)罕见肿瘤专委会委员
CSCO小细胞肺癌专业委员会主任委员
CSCO临床研究专家委员会候任主任委员
中国抗癌协会肺癌专业委员会候任主任委员
CSCO非小细胞肺癌专业委员会副主任委员
CSCO肿瘤大数据专家委员会副主任委员
中华医学会肿瘤学分会肺癌专委会副主任委员
中国医师协会肿瘤多学科诊疗专委会副主任委员
国家卫生、计生委常见肿瘤规范化诊疗专家组成员
吉林省医师协会肿瘤医师分会主任委员
吉林省医学会肿瘤专业委员会主任委员
2023年临床医学领域“全球高被引科学家”
近期的ELCC大会中由您牵头开展的免疫联合放化疗的III期研究公布了安全导入期数据,为小细胞肺癌患者带来了潜在的新型治疗模式,请您谈一谈该研究结果对SCLC治疗领域的价值与意义。
程颖教授:小细胞肺癌的发病率约占肺癌的15%~20%,侵袭性强,恶性程度高,是一类预后极差的难治性肿瘤。SCLC易发生远处转移,初诊时仅约三分之一的患者处于局限期,近年来随着体检意识的增强,局限期SCLC的检出率有所增加。对于局限期SCLC,除了少数患者(T1-2N0M0)有手术机会外,绝大部分患者治疗以放化疗为主,近三十年来缺乏更为有效的治疗模式,患者的中位生存期在16~24个月左右。因此,对于局限期SCLC仍存在巨大未被满足的临床需求,亟需探索更多有效的治疗策略来改善患者生存获益。
近年来随着免疫治疗药物在肿瘤领域的开发应用,也为SCLC患者带来了希望。我们团队率先在国内进行广泛期SCLC免疫治疗的探索,牵头开展的阿得贝利单抗联合化疗对比安慰剂联合化疗一线治疗广泛期SCLC的III期研究获得阳性结果,阿得贝利单抗成为第一个在中国上市治疗SCLC的国产PD-L1抑制剂。2023 ESMO IO大会中,我们发布了CAPSTONE-1研究的3年OS率,经过长期生存随访,更加确认了阿得贝利单抗联合化疗能够为ES-SCLC患者带来长期生存的获益。阿得贝利单抗联合化疗3年OS率达到了21.1%,较对照组提升了1倍以上,让1/5的患者生存期超过了3年。
基于阿得贝利单抗在广泛期SCLC展现的良好疗效和安全性,我们牵头开展了阿得贝利单抗联合同步放化疗治疗局限期SCLC的III期研究。在研究设计上,患者首先接受2周期的阿得贝利单抗联合化疗诱导治疗,然后阿得贝利单抗联合化疗同时使用胸部放疗(60Gy/2Gy, QD 6周),随后使用阿得贝利单抗维持治疗。通过诱导治疗我们希望减少由于肿瘤放疗野过大引起的放射性肺损伤,期望免疫联合放化疗可以具有更好的协同作用,以获得更高的ORR,进而达到延长患者生存的目的。同时考虑放疗和免疫治疗带来间质性肺炎的问题,我们十分严谨的将该研究分为两个阶段:第一阶段(图1所示):安全性导入研究,以评估此种联合策略的安全性;第二阶段:通过第一阶段确认安全性后,开展随机对照、双盲的III期研究。目前公布的是安全导入研究结果:ORR达92.9%,mPFS达到了17.9个月,2年OS率是64.3%,初步疗效已经优于历史数据,且肺炎的发生可控,未发生超出预期的不良反应,此种治疗策略展现出了作为新的治疗模式的潜力。目前III期研究患者入组已经完成,我十分期待在未来的国际大会中,与国际上的专家同道分享该III期研究的疗效数据。
目前针对局限期SCLC仍有多种治疗模式和创新药物正在探索中,例如ADRIATIC研究是一项随机、双盲、安慰剂对照、全球多中心的III期研究,旨在评估度伐利尤单抗±tremelimumab在同步放化疗后未进展的局限期SCLC患者中的巩固疗效;斯鲁利单抗联合同步放化疗治疗局限期SCLC的III期研究,帕博利珠单抗联合同步放化疗后给予帕博利珠单抗±奥拉帕利巩固维持治疗的III期研究,特瑞普利单抗+Tifcemalimab(BTLA抑制剂)在同步放化疗后未进展的局限期SCLC患者中巩固治疗的III期研究,替雷利珠单抗+Ociperlimab(TIGIT抑制剂)联合同步放化疗治疗局限期SCLC的II期研究以及Tarlatamab(DLL3/CD3双抗)在同步放化疗后未进展的局限期SCLC患者中巩固治疗的III期研究均正在进行中,未来有望为局限期SCLC患者带来更多的治疗选择。
请您谈谈阿得贝利单抗作为我国自主研发的全新PD-L1抑制剂,有什么样特点可以使其在联合放化疗的治疗模式中,疗效可靠同时也展现出色的安全性。
程颖教授:阿得贝利单抗不同于已经上市的2个进口PD-L1抑制剂,其选择了与FcγR结合能力较弱的IgG4抗体类型。IgG4型抗体本身无补体依赖的细胞毒性作用(CDC)效应,同时阿得贝利单抗进一步通过Fc段234A/235A定点突变改造,进一步降低了其和免疫效应细胞表面FcγR结合的能力,从而消除了抗体依赖的细胞介导的细胞毒性作用(ADCC)效应、抗体依赖的细胞介导的吞噬作用(ADCP)效应,通过抗体Fc段的改造很好地避免了由FcγR受体介导的效应功能对免疫细胞的杀伤,抗体功能更加纯净。而且234A/235A定点突变改造,还去除了阿得贝利单抗与免疫效应细胞表面FcγRI结合的能力,从而降低了ADCR效应(抗体依赖性细胞因子释放)。ADCR效应的降低就意味着IL-6释放的减少,从而减少免疫相关的不良反应的发生,同时也意味着IL-8释放的减少,可以提升免疫疗效。此外,其Fab段采用S228P突变改造,避免lgG4抗体的Fab段置换,抗体更加稳定[2,3,4]。
从分子结构角度看,相比于既往上市的PD-L1抗体,阿得贝利单抗具有独特的与PD-L1的结合表位,其结合的角度更加居中,结合区域与结合面积更接近天然配体PD-1。同时阿得贝利单抗与PD-L1结合的解离常数Kd值仅为0.27*10-10mol/L,亲和力相较于已上市的PD-L1抗体更强。临床前研究提示阿得贝利单抗刺激T细胞释放IFN-γ的EC50值更低,激活DC细胞和T细胞能力更强,具有良好的抗瘤活性。
从临床研究数据来看,在阿得贝利单抗联合放化疗研究开展期间,研究者最担心的就是放射性肺炎与免疫性肺炎的发生。安全导入期数据显示:没有治疗相关的死亡事件的发生,4例(14.3%)患者发生治疗相关肺炎,1例出现治疗相关的免疫性肺疾病,且均为2级,无≥3级肺炎的发生,体现出了阿得贝利单抗卓越的安全性。我十分期待III期研究数据的未来公布,改写局限期SCLC患者的治疗模式。
由您带领吉林省肿瘤医院专家团队完成的创新成果“小细胞肺癌精准治疗的创新性研究与推广应用”荣获吉林省科技进步奖一等奖,您如何看待中国在全球学术界越来越重要的角色与意义?
程颖教授:小细胞肺癌(SCLC)是全球肿瘤诊疗领域的棘手难题,被公认为是最难治的肿瘤类型之一,我国SCLC在全球范围内属于发病比例较高的肿瘤,我和我的团队20年来一直奋战在抗击肿瘤一线,为了提高治疗疗效和患者生活质量,让更多SCLC患者获得新生,团队从基础到临床转化研究做了一系列的探索。限于当时对SCLC机制的认识和药物研发缓慢的限制,早期在SCLC的研究主要是对高效低毒化疗药物的探索,研究进展多年来举步维艰,为了尽快提升我国SCLC的诊疗水平和研究能力,我们与全国专家共同携手专门致力于小细胞肺癌研究。
随着近些年来抗肿瘤药物研发的快速发展,中国的创新型药企迅速崛起,CDE快速审评审批等一系列鼓励创新的政策不断推出,我们有了更多的机遇去攻克SCLC这个临床难题,让中国的临床研究在全球学术界发挥越来越重要的作用。目前在SCLC临床研究领域我们已经走在世界前列,对于SCLC三线及三线以上治疗的患者,国际上尚没有标准的治疗方案,我国自主研发的小分子抗血管多靶点TKI药物安罗替尼建立了新的治疗标准,在2019年附条件批准后我们在III期研究中进一步验证了安罗替尼的疗效;在SCLC一线治疗方面,中国患者具有更多且更优的免疫治疗选择,除了阿替利珠单抗、度伐利尤单抗两款进口PD-L1抑制剂以外,由我和王洁教授牵头开展的我国自主研发的PD-L1抑制剂阿得贝利单抗联合化疗一线治疗广泛期SCLC 的III期研究也取得成功,且3年OS率数值上更好,达到了21.1%。我们团队牵头开展的研究在全球首次证实了PD-1抑制剂斯鲁利单抗联合化疗同样可以改善广泛期SCLC的生存,并且另两款国产PD-1抑制剂替雷利珠单抗和特瑞普利单抗再次证实了PD-1抑制剂在SCLC的疗效,今年有望获批小细胞肺癌的适应症。此外,我们牵头的安罗替尼联合免疫及化疗的III期研究也取得了成功,开创了SCLC一线治疗新的模式,将广泛期SCLC患者的生存期推向历史新高。我们的研究结果多次在ASCO、WCLC、ESMO、ELCC、AACR等国际学术会议报告,在《JAMA》,《Lancet Oncology》,《JTO》等国际顶级学术期刊发表,这些都体现了中国研究者主导的临床研究在全球发挥着举足轻重的作用。
针对SCLC的发病机制和肿瘤微环境十分复杂的特点,多年来我们团队在基础研究和转化研究领域也进行了深层次的探索。我们围绕SCLC肿瘤成分、免疫微环境及基质成分等方面进行了大量探索,包括耐药机制、表型可塑性和CTC等;巨噬细胞、NK细胞等免疫成份;肿瘤相关成纤维细胞等基质成分。在已积累的对SCLC肿瘤及微环境深层次的研究成果和深刻理解之上,我们还将对SCLC肿瘤生态环境进行研究,结合患者临床数据,探索对SCLC复杂生态环境的精准分型,指导SCLC适应性治疗新策略。同时,对液态标志物探索,推动实现实时、动态监测以指导临床治疗,有效转化为临床应用,期待未来在基础和转化研究领域获得突破,为SCLC患者带来更加精准有效的治疗途径。
参考文献
[1]Ying C, et al. ELCC 2024:198P
[2]Ying C, Wang J, Zhou C, et al. ESMO IO, 2023: 84P
[3]Wang J, Zhou C, Yao W, et al. The Lancet Oncology, 2022 Jun;23(6):739-747
[4]Xu D, et al. Cell Immunol. 2000 Feb 25;200(1):16-26.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#阿得贝利单抗#
6