iNKT细胞通过激活JAK/STAT途径促进巨噬细胞向M1极化,并释放大量TNF-α细胞因子,从而对机体进行保护
6小时前 《基因启明》公众号 《基因启明》公众号 发表于上海
衣原体是一类专性细胞内寄生病原体,可导致呼吸道、眼部和性传播疾病。
亮点
1.iNKT细胞介导沙眼衣原体小鼠肺炎株(Chlamydia muridarum, C.m.)感染下小鼠肺巨噬细胞数量的增加,在三种巨噬细胞亚群(AM、IM、Mo/Mφ)中,iNKT细胞更偏向于促进IM和Mo/Mφ的扩增。
2.iNKT细胞主要介导巨噬细胞向M1极化,释放大量TNF-α细胞因子,以抵抗肺部衣原体感染。
衣原体是一类专性细胞内寄生病原体,可导致呼吸道、眼部和性传播疾病。抗菌药物虽然有效控制衣原体感染,但无法彻底清除细胞内衣原体,持续性胞内感染状态是导致肺炎复发、过敏性哮喘及心血管系统疾病的危险因素。
巨噬细胞是人体最重要的免疫细胞之一,在感知和控制细菌感染方面起着关键作用。巨噬细胞的极化状态被广泛定义为1型(M1)和2型(M2)巨噬细胞。其中M1巨噬细胞能促进局部Th1反应。已有研究表明M1巨噬细胞可以限制衣原体的生长。
恒定自然杀伤T(iNKT)细胞,具有T细胞和自然杀伤(NK)细胞的特性,在免疫应答的早期阶段发挥重要作用。已有研究证明iNKT细胞是肺部衣原体感染的关键调节因子。
那么,iNKT细胞抵抗衣原体感染是否与巨噬细胞活化有关呢?
近期,一项题为Enhancement of Macrophage Immunity against Chlamydial Infection by Natural Killer T Cells的研究揭示了这一问题的答案。研究发现机体内iNKT细胞能够介导衣原体感染下的肺巨噬细胞活化,使巨噬细胞向M1极化,并释放大量TNF-α细胞因子,进而增强肺巨噬细胞的杀伤能力,抵抗外界的衣原体感染。

首先,研究人员构建了iNKT细胞敲除鼠模型(iNKT KO),随后令小鼠感染沙眼衣原体小鼠肺炎株(Chlamydia muridarum, C.m.)。通过检测巨噬细胞含量,他们发现C.m.肺部感染强烈的诱导了小鼠肺部巨噬细胞数量增加,并在感染后第7天达到峰值,然后在感染后第14天迅速下降到基线水平。然而,相比于正常小鼠,iNKT KO小鼠肺部巨噬细胞增加程度更低。这表明,iNKT细胞介导了衣原体感染对巨噬细胞的刺激作用。
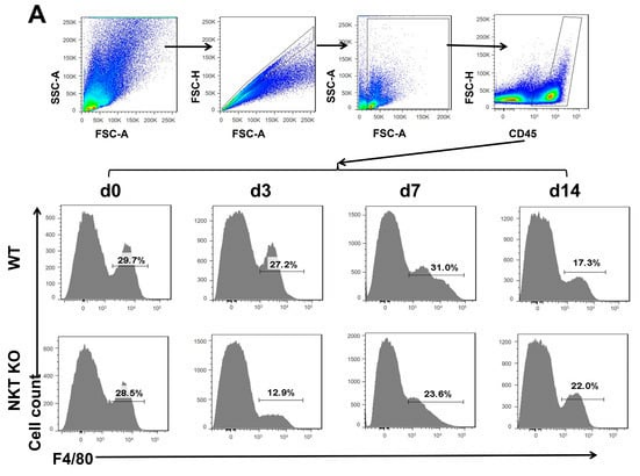
iNKT KO小鼠C.m.感染后肺部巨噬细胞反应降低
随后,他们进一步研究了感染C.m.对巨噬细胞亚群的影响。有趣的是,在正常小鼠中,C.m.感染后IM和Mo/Mφ数量显著增加,且IM增加得更多;与正常小鼠相比,iNKT KO小鼠的IM和Mo/Mφ亚群增加的比例偏低;在感染期间,AM 数量并没有显著变化,且iNKT细胞的有无不影响AM数量。这表明,在C.m.感染肺部后,iNKT细胞更偏向于促进肺部巨噬细胞亚群IM和Mo/Mφ的扩增。
注:肺泡巨噬细胞(AM)位于气道腔内,高表达CD11c,在维持肺的免疫稳态方面起着重要作用;间质巨噬细胞(IM)驻留在肺实质中,低表达CD11c,在肺内具有调节功能。单核细胞和未分化巨噬细胞(Mo/Mφ)不表达CD11c,在炎症和感染期间分化为巨噬细胞。
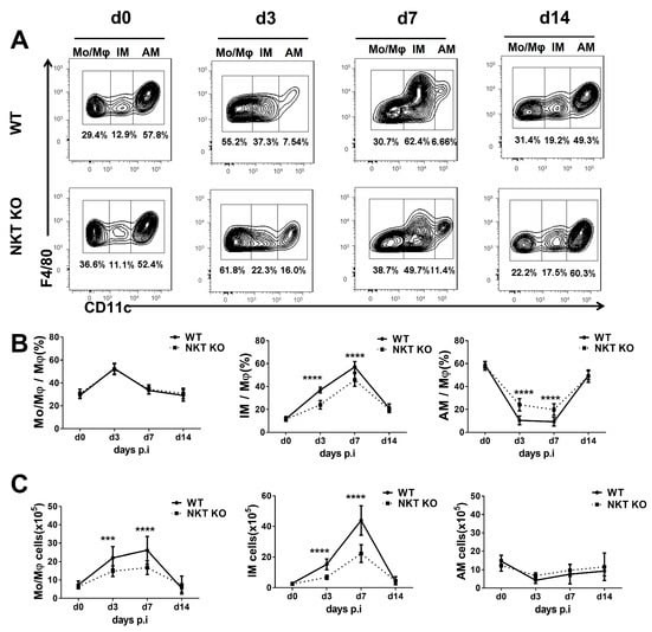
WT和iNKT KO小鼠C.m.感染期间巨噬细胞亚群变化的动力学
众所周知,巨噬细胞的极化状态与免疫功能有关。为了检查衣原体肺部感染后巨噬细胞的功能变化,研究人员使用iNOS和CD206分别作为M1和M2巨噬细胞标志物。有趣的是,他们发现正常小鼠感染C.m.后,三种巨噬细胞亚群的iNOS巨噬细胞的频率和数量都显着增加,表明M1极化状态增强;但iNKT KO小鼠在感染后却表现出较少的M1极化。这一发现表明,iNKT细胞主要介导巨噬细胞向M1极化,从而抵抗外界衣原体感染。
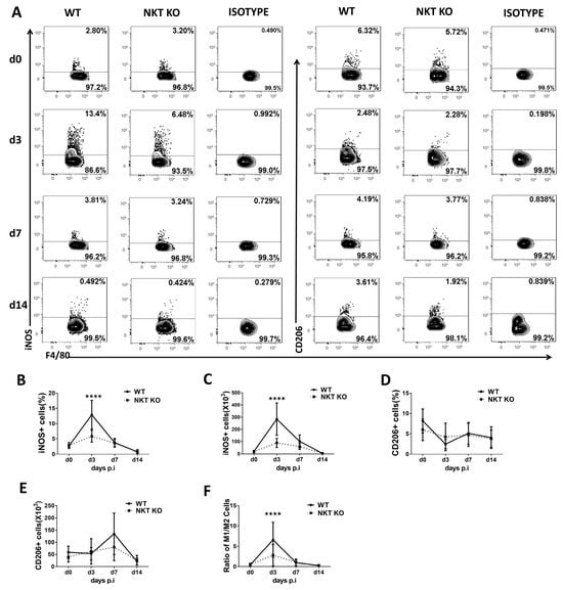
C.m.感染期间WT或iNKT KO小鼠Mo/Mφ的极化状态
此外,肿瘤坏死因子α(TNF-α)是M1巨噬细胞产生的典型细胞因子,有助于增强巨噬细胞杀伤能力、刺激免疫系统增强抵抗力。研究人员检测了感染后第7天巨噬细胞亚群(AM、IM和Mo/Mφ)中TNF-α含量,发现与正常小鼠相比,衣原体感染后iNKT KO小鼠的IM和Mo/Mφ群体中产生TNFα的数量显着减少,表明iNKT细胞增强巨噬细胞产生TNF-α的能力。
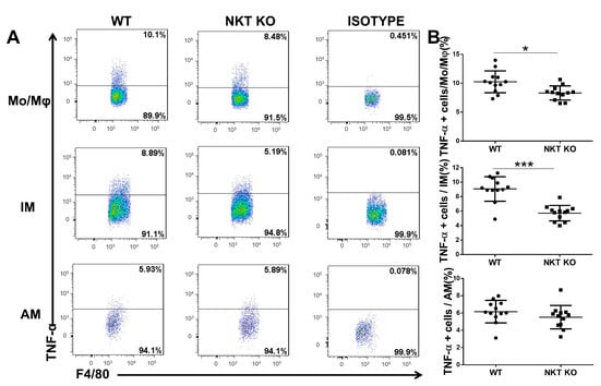
C.m.感染后AM、IM和Mo/Mφ亚群中的TNF-α数量
综上,以上结果表明iNKT细胞对衣原体肺部感染中巨噬细胞M1极化具有明显的促进作用。那么,iNKT细胞最终是否能够增强巨噬细胞在宿主防御中的功能呢?
为解答这个疑问,利用过继转移法,研究人员将C.m.感染后正常小鼠的Mφ细胞(WT-Mφ)或iNKT KO小鼠的Mφ细胞(iNKT KO-Mφ)分别转移到同基因型的小鼠体内,然后再用C.m.感染这些同基因型小鼠。不出所料,他们发现在感染C.m.后,与接受iNKT KO-Mφ小鼠相比,接受WT-Mφ小鼠体重下降程度更小;此外,WT-Mφ小鼠在感染后的炎症和病理评分明显更低;更重要的是,WT-Mφ小鼠肺部的衣原体载量远低于iNKT KO-Mφ小鼠。这表明,WT-Mφ比iNKT KO-Mφ更能赋予机体保护性免疫,证实了iNKT细胞在增强巨噬细胞对抗衣原体肺部感染功能方面具有至关重要的作用。
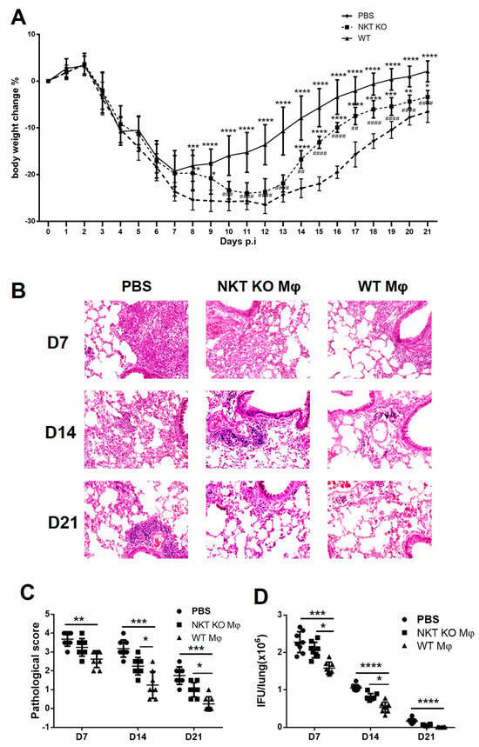
WT-Mφ和iNKT KO-Mφ过继转移以测试它们在体内的功能
目前,巨噬细胞M1的极化包括四种信号通路(JNK通路、JAK/STAT通路、PI3K/Akt通路和Notch通路),为确定iNKT细胞促进M1极化的具体机制,研究人员分离了小鼠的肺巨噬细胞进行了实时PCR检测,结果表明iNKT细胞可能在C.m.感染期间通过激活JAK/STAT途径促进M1极化。
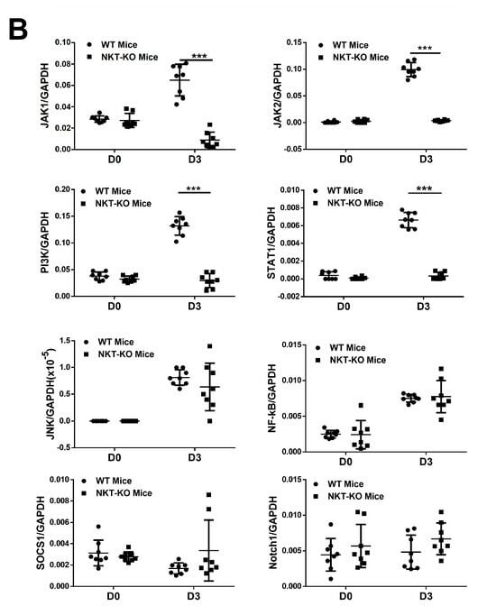
qRT-PCR检测肺巨噬细胞中JAK1、JAK2、PI3K、STAT1、JNK、NF-κB、SOCS1和Notch1的mRNA水平
总的来说,iNKT细胞通过促进肺巨噬细胞M1极化,增强了巨噬细胞的杀伤力,提高了机体抵御肺部衣原体感染的能力,这对于衣原体肺炎等相关疾病的治愈具有“里程碑式”意义。
来源:
微信公众号: 基因启明
参考文献:
Peng Y, Qiao S, Wang H, Shekhar S, Wang S, Yang J, Fan Y, Yang X. Enhancement of Macrophage Immunity against Chlamydial Infection by Natural Killer T Cells. Cells. 2024 Jan 11;13(2):133. doi: 10.3390/cells13020133. PMID: 38247825; PMCID: PMC10813948.
Brennan PJ, Brigl M, Brenner MB. Invariant natural killer T cells: an innate activation scheme linked to diverse effector functions. Nat Rev Immunol. 2013 Feb;13(2):101-17. doi: 10.1038/nri3369. Epub 2013 Jan 21. PMID: 23334244.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#衣原体#
2