胰腺癌研究表明,iNKT细胞的瘤内积累通过刺激IFN-I产生、协调免疫细胞浸润,介导肿瘤免疫反应
2024-11-21 《基因启明》公众号 《基因启明》公众号 发表于上海
胰腺癌是一种起源于胰腺导管上皮及腺泡细胞的恶性肿瘤,被医学界称为“癌中之王”。 胰腺导管腺癌(PDA)是最常见的胰腺癌,其5年总生存率仅为9%左右,是癌症相关死亡的常见原因。
亮点
1.iNKT细胞是形成免疫反应性肿瘤微环境和胰腺癌适应性免疫所必需的。
2.iNKT细胞通过表面CD40L分子与髓系细胞表达的CD40相互作用,从而刺激IFN-I的产生,介导胰腺癌免疫反应。
3.亚叶酸(FA)通过诱导iNKT细胞积累,有望成为治疗胰腺癌的候选药物。

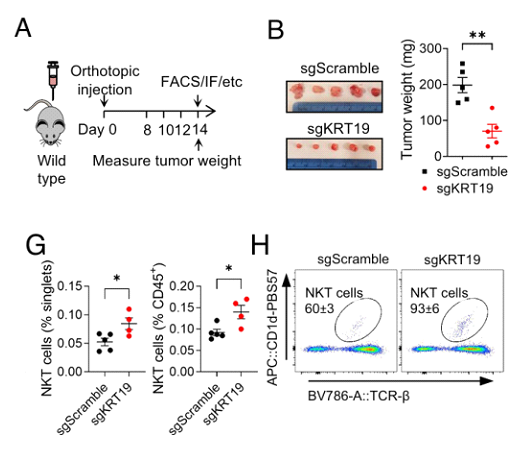
KRT19缺陷小鼠的肿瘤尺寸及免疫细胞含量
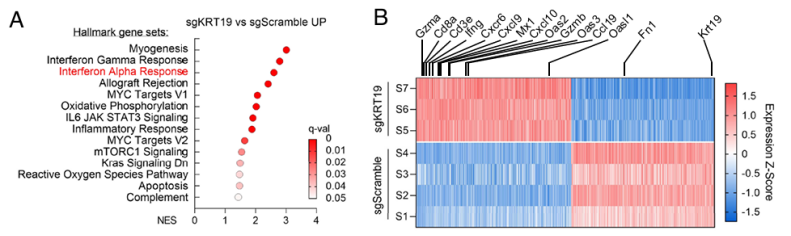
PDA中的抗肿瘤免疫
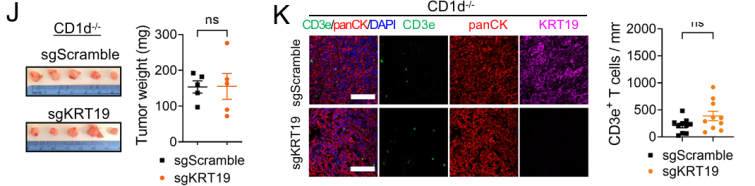
sgKRT19编辑肿瘤中的iNKT细胞和I型IFN
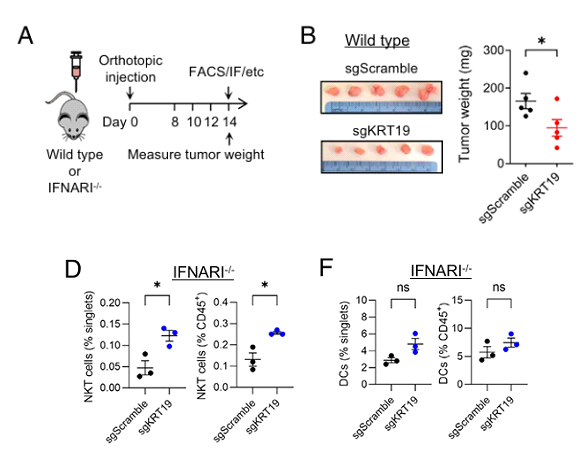
IFN-I和KRT19对PDA肿瘤的免疫控制
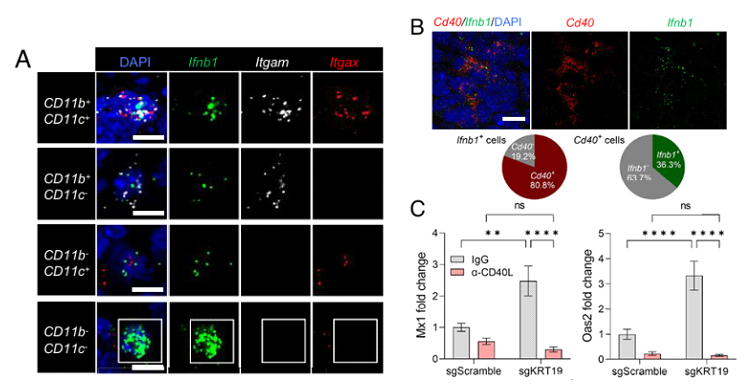
分子信号的荧光定位
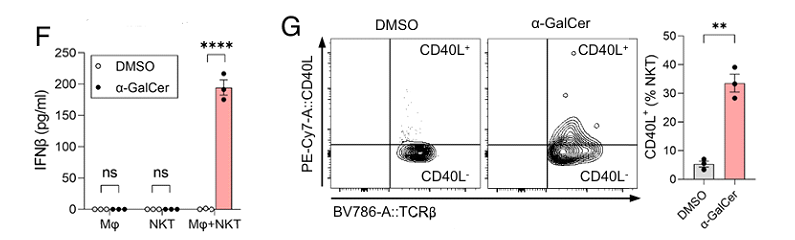
IFN产生和CD40L含量
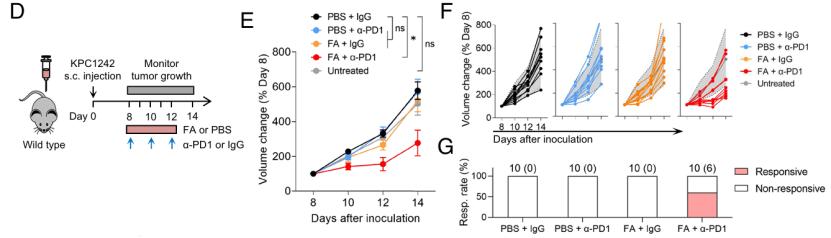
FA、与抗PD-1抗体联合治疗缓解肿瘤
来源:
微信公众号: 基因启明
参考文献:
Li J, Moresco P, Fearon DT. Intratumoral NKT cell accumulation promotes antitumor immunity in pancreatic cancer. Proc Natl Acad Sci U S A. 2024 Jul 16;121(29):e2403917121. doi: 10.1073/pnas.2403917121. Epub 2024 Jul 9. PMID: 38980903.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













胰腺导管腺癌(PDA)是最常见的胰腺癌,其5年总生存率仅为9%左右,是癌症相关死亡的常见原因。
4
#胰腺癌#
9