重启还是终止?肝癌免疫治疗相关肝损伤的有效治疗策略探索
2025-01-02 肝癌在线 肝癌在线 发表于陕西省
近期,首都医科大学附属北京地坛医院江宇泳教授作“肝癌免疫治疗相关肝损伤”专题报告。肝癌在线特将精华内容整理成文,以飨读者。
目前,免疫检查点抑制剂(ICIs)已成为肿瘤治疗领域的突破性进展之一。但随着ICIs的广泛应用,这类药物的不良反应也引起了临床的重视。近期,首都医科大学附属北京地坛医院江宇泳教授作“肝癌免疫治疗相关肝损伤”专题报告。肝癌在线特将精华内容整理成文,以飨读者。
目前,免疫治疗在肿瘤治疗中进展迅速,免疫治疗和局部治疗大大提高了肝癌的治疗效果,使肝癌患者生存期更长,生活质量更好。其中,免疫检查点在机体免疫的负向调节中起重要作用,可以防止机体免疫系统过度活化。而肿瘤组织则利用这一负向调节机制,通过高表达CTLA-4受体或PD-1配体,并与活化的淋巴细胞表面的CTLA-4或PD-1结合,从而摆脱淋巴细胞杀伤作用,实现免疫逃逸。
ICIs通过阻断CTLA-4和PD-1/PD-L1,打破人体免疫耐受机制,激活机体的免疫系统,促进对肿瘤组织的杀伤作用。以PD-1为作用靶点的ICIs纳武利尤单抗、帕博利珠单抗、信迪利单抗、卡瑞利珠单抗、替雷利珠单抗先后获批,用于肝癌的免疫治疗。而值得注意的是,ICIs过度激活免疫系统可以引起机体组织器官损伤。
一项来自WHO药物警戒数据库(VigiLyze)2009-2018年1月的数据,筛选了31059份ICIs相关病例报告,确定了613例致命免疫相关不良反应(irAE)。其中124例(20.2%)发生了药物性肝损伤(ILICI):包括31例CTLA-4治疗,74例PD-1/PD-L1治疗,19例联合治疗。肿瘤免疫治疗的严重不良反应中,肝损伤病例数排在第三位,其中死亡病例数占报告肝损伤病例数的22%。因此,与ICI相关的致命irAEs应该引起我们的高度重视。
一、肝癌免疫治疗相关不良反应
irAEs通常发生在治疗过程的早期,大多数在最初的12-16周内。富含淋巴细胞的组织(皮肤和肠道)经常受到影响,症状出现较早,大约在PD-1/PD-L1抑制剂治疗开始后的第3周或第4周。肝、肺和内分泌毒性平均出现在PD-1/PD-L1抑制剂治疗或联合检查点阻断开始后的6-10周。联合检查点阻断的患者比接受PD-1/PD-L1抑制剂治疗的患者更早发生irAEs。
特异性自身免疫T细胞克隆识别正常和肿瘤组织中的共同抗原,导致irAEs,这与T细胞介导机制、B细胞介导机制、在垂体的特殊情况下组织中的CTLA-4表达、炎症和细胞因子介导的机制以及肠道微生物组的作用有关。
一项注册临床试验表明,单药治疗时,CTLA-4抑制剂肝毒性发生率最高。肝炎发生率(任何级别)在接受标准剂量(3mg/kg)伊匹木单抗治疗的患者中仅为3%-5%,而接受高剂量(10mg/kg)治疗的患者则为15%-16%。在PD-1抑制剂的大型试验中,免疫治疗相关肝炎(ICH)发生率总体为1%-17%,3/4级为3%-5%。PD-1抑制剂的单一疗法导致ICH的发生率最低,在0%-3%(大部分为1%-2%)之间,并且3/4级反应极少<1%。与CTLA-4抑制剂不同,继发于PD-1和PD-L1抑制剂的irAE的发生率似乎与剂量无关。CTLA-4和PD-1阻断的联合治疗会导致更高的irAE发生率,包括ICH。在该组中,任何级别的ICH发生率为18%-22%,其中8%-11%为严重肝炎。
在其他的风险因素中,黑色素瘤发生肝毒性的可能性更高。针对已患有自身免疫性疾病的患者的小型研究观察到,在伊匹木单抗治疗后,irAE的发生率很高(33%经历了3-5级事件)和自身免疫性疾病恶化(27%经历了需要治疗的发作)。然而,这些患者都没有自身免疫性肝病,也没有经历过ICH。从Child-Pugh A级或早期Child-Pugh B级肝硬化患者的有限初始数据来看,ICH的发生率似乎并不明显高于没有肝病的患者。在一个ICI之后遇到的irAE再切换到不同类别的ICI时似乎无法预测相同的irAE。同时,乙肝再激活非常罕见,但是应当重视,需要提前检测乙肝五项,应该提前抗病毒。
二、ILICI的治疗
1、ILICI临床表现
免疫检查点抑制剂相关免疫性肝炎(ILICI)发病的中位时间最常为8-12周,但它最早可在ICI治疗开始后2-3周出现,多数为无症状的肝功能异常,病情较重的患者临床可表现为发热、黄疸、右侧腹痛、尿色深、出血倾向,甚至发生急性肝功能衰竭。与抗PD-1或抗PD-L1抗体相比,发热是继发于CTLA-4抑制剂的ILICI更突出的特征。肝功能异常,以ALT升高多见,也可以有TBIL升高。胆管炎表现在PD-1或PD-L1治疗更多见。
2、ILICI分型
ILICI分型分为ICIs相关免疫介导的肝炎和ICIs相关免疫介导的胆管炎。CTLA-4单抗、PD-1/PD-L1单抗均可引起ICIs相关免疫介导的肝炎,以肝细胞为主要损伤靶点,生化表现转氨酶升高为主,病理学为小叶内炎症及坏死。ICIs相关免疫介导的胆管炎以胆管上皮细胞为损伤靶点,又分为大胆管损伤型、小胆管损伤型、混合型,多由PD-1/PD-L1单抗引起,肝生化学提示以ALP、GGT升高为主。大胆管型还可出现类似硬化性胆管炎的表现,如局部肝外胆管狭窄、上游胆管扩张、胆管壁及胆囊壁增厚,但磁共振胆胰管造影及经内镜逆行性胆胰管造影可证实无占位性病变。小胆管型损伤影像学无明显改变,肝脏病理表现为汇管区水肿、炎症细胞浸润以及小胆管上皮破坏的征象。
3、ILICI病理变化
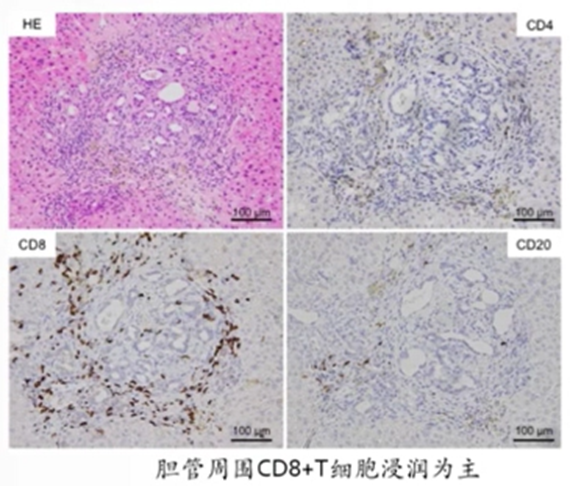
病理上,ILICI主要是小叶和/或门静脉周围炎症,也可能存在小叶中心坏死和中央静脉内皮炎。ILICI中的炎症漫润主要是活化的T淋巴细胞(主要是CD8+)和组织细胞,几乎没有浆细胞。相比之下自身免疫性肝炎肝组织中的CD20+B淋巴细胞和CD4+T淋巴细胞比例较高。
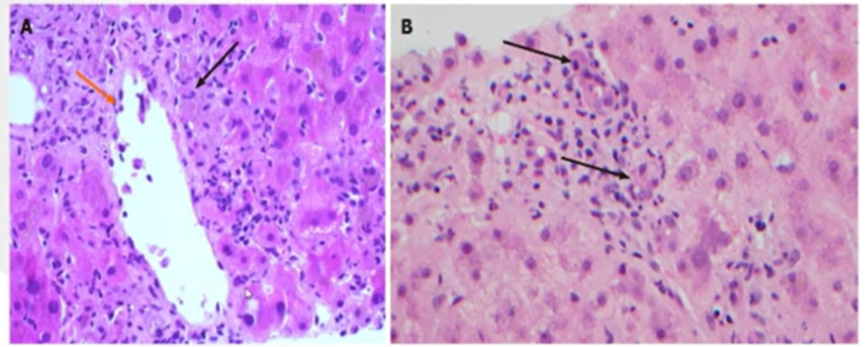
A:伊匹木单抗相关肝毒性中明显的内周炎(橙色箭头);
B:淋巴细胞性胆管炎,继发于尼鲁单抗的明显胆管损伤(黑色箭头)。
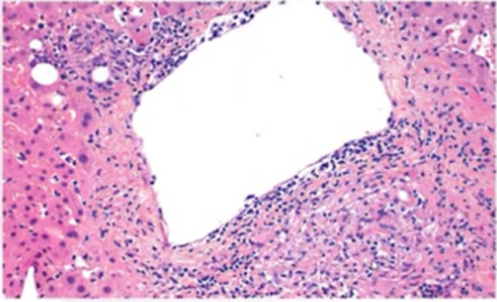
被单核炎症细胞和肉芽肿性炎症包围的肝静脉
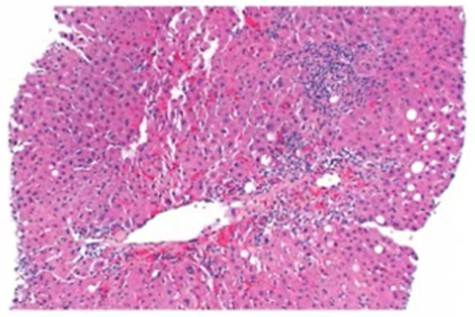
小叶3区肝炎和坏死,在受伤的中央静脉附近有大量组织细胞
病例:
75岁,男性,非小细胞肺癌,经纳武单抗治疗。MRCP提示胆总管弥漫性扩张和多灶性狭窄,并伴有从肝门周围到肝内胆管的狭窄前扩张,符合硬化性胆管炎。
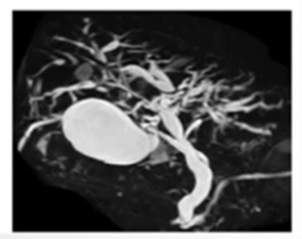
一项包含117名患者的多中心队列研究中,分析了免疫检查点抑制剂诱导的肝损伤。患者平均年龄为63岁,男性占53.8%,其中82%为3级或4级肝损伤。37%为胆汁淤积型肝损伤,肝细胞型占38%,混合型占25%。使用不同的治疗方式,如激素治疗、熊去氧胆酸盐(UDCA)治疗、激素+UDCA治疗,患者稳定恢复的占56%(66例),肝炎复发者占23.5%(12例)。在这组患者中,49名患者(41.9%)进行了肝活检,其中胆汁淤积型20例(41%),肝细胞型23例(47%),混合型6例(12%)。
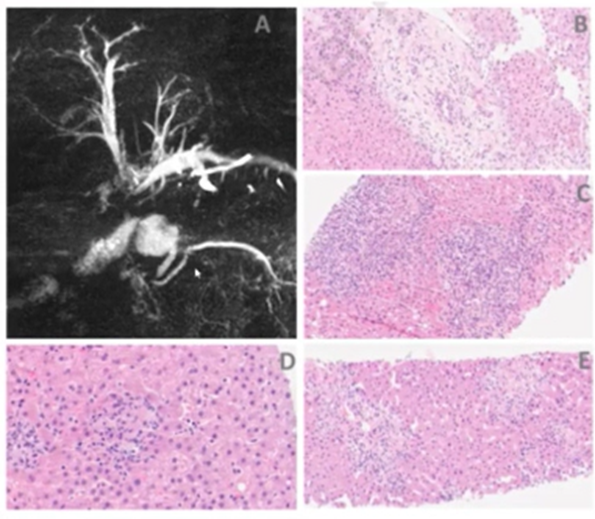
A胆管狭窄而无梗阻
B淋巴细胞性胆管炎
C嗜中性粒细胞性胆管炎
D肉芽肿性肝炎
E小叶中心周围坏死和内皮炎
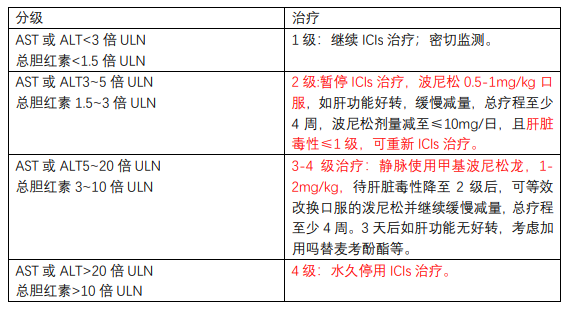
4、ILICI管理建议
5、难治性ILICI治疗
在口服和静脉注射皮质类固醇均无效情况下,吗替麦考酚酯是首选的二线药物,剂量为500-1000mg,每天两次。对于皮质类固醇和吗替麦考酚酯难治性ILICI,三线药物钙调神经磷酸酶抑制剂(他克莫司和环孢素)在自身免疫性肝炎中的应用取得了不同程度的成功,并构成了肝移植排斥治疗的支柱,它们对抗T细胞介导的肝脏炎症的作用机制使它们成为治疗难治性ILICI的合理选择。ILICI也可表现为免疫介导的胆管病,尤其是在接受PD-1/PD-L1抑制剂的患者中,对类固醇治疗的反应通常为中度至差,在免疫抑制中添加熊去氧胆酸可能会有所帮助。
6、持续监测
一旦达到反应,患者应持续监测症状及肝功能。监测频率(从每天到每周)根据肝病的严重程度和开始治疗后的改善率进行商定。在肝炎明显消退和免疫抑制完成后,应继续监测肝功能(每两周至每月一次),多达三分之一的患者出现肝炎反弹。
关于是否重启或永久停止ICI的决定是一个艰难的决定。多个案例报告描述,尽管最初有3/4级肝毒性,但重新引入ICI时没有肝损伤复发。其他有希望的策略包括在重新使用ICI时联合使用布地奈德或在因ICI联合治疗产生严重毒性的患者中恢复抗PD-1单药治疗。这些方法需要经过验证性研究才能被广泛采用。目前,是否与ICI再次挑战仍需通过多学科讨论逐案确定。
小结
1、ILICI排在肿瘤免疫治疗严重不良反应的第三位,死亡病例占肝损伤病例的22%。
2、ILICI临床表现多样,自应用ICI 3-12周均可出现,可以无症状仅为肝功能异常,也可以黄疸迅速上升;肝功能变化迅速,一旦发现,需要密切监测。
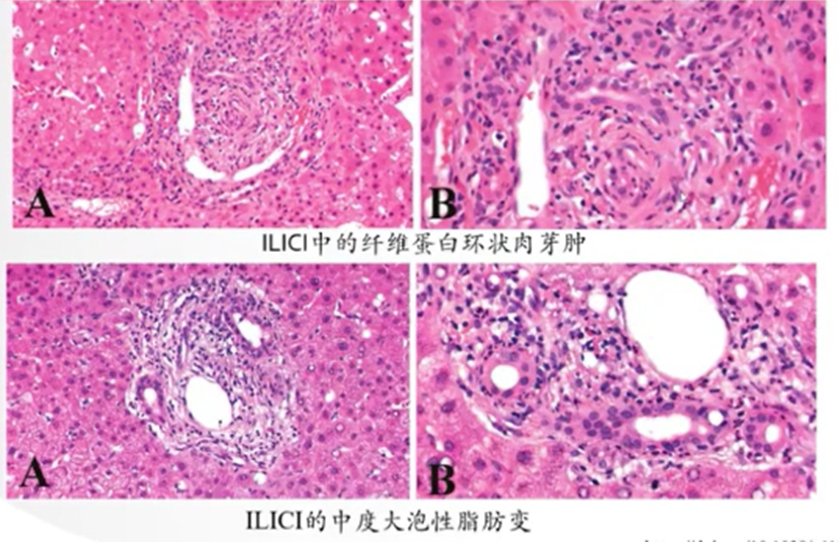
3、ILICI肝组织病理可见到CD8+T细胞浸润为主的炎性肉芽肿、血管内皮炎症、胆管炎(小胆管、大胆管)、脂肪变等。
4、根据肝损伤严重程度分级治疗:2级肝损伤:停用ICI,口服泼尼松0.5-lg/Kg;3-4级肝损伤:立即停用ICI,静脉滴注甲基泼尼松龙1-2mg/Kg。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#肝癌# #免疫治疗相关肝损伤#
13