上海大学陈雨/陈付学/冯炜团队AM: 六氰高铁酸钙(III)纳米催化剂实现自闭症谱系障碍治疗的氧化还原稳态
2024-08-06 BioMed科技 BioMed科技 发表于上海
研究设计工程化纳米酶CaH NCs用于治疗自闭症谱系障碍,能清除ROS、调节氧化还原平衡、减轻炎症和细胞凋亡,改善动物模型症状,为治疗开辟新途径。
自闭症谱系障碍(ASD)是一种在儿童早期出现的神经精神疾病,其特征是社交沟通受损、兴趣减退和刻板重复行为。自闭症谱系障碍(ASD)是一种具有高度异质性的复杂神经发育障碍,过量产生的活性氧(ROS)会引发一系列病理变化,包括细胞凋亡和炎症反应。病因涉及遗传因素、环境暴露、大脑结构变化和免疫系统的贡献。鉴于ASD的复杂病因,目前尚无有效的治疗方法。
在这项研究中,上海大学陈雨教授、陈付学教授及冯炜教授设计并工程化了一种特定的催化纳米酶——六氰基铁酸钙(III)纳米催化剂(CaH NCs),用于高效治疗ASD。CaH NCs可以模拟天然酶的活性,包括超氧化物歧化酶、过氧化物酶、过氧化氢酶和谷胱甘肽过氧化物酶,能够减轻细胞内过量的ROS并调节氧化还原平衡。这些CaH NCs调节线粒体膜电位,提升B细胞淋巴瘤-2(Bcl-2)水平,抑制促凋亡蛋白,包括胱天蛋白酶-3(Caspase-3)和B细胞淋巴瘤-2相关X蛋白(Bax),从而有效减少细胞凋亡。重要的是,CaH NCs通过上调抗炎细胞因子白细胞介素-10(IL-10)和下调促炎因子来减轻炎症,导致小胶质细胞和星形胶质细胞的激活减少,继而减少神经炎症。随后,CaH NCs通过调节炎症和抑制细胞凋亡,增强ASD动物模型的社交能力,减少焦虑水平,改善重复行为,并提高学习和记忆能力。在管理和预防ASD方面,CaH NCs代表了一种治疗自闭症的范式转变,为神经系统疾病的临床干预开辟了一种替代但高效的途径。该研究以题为“Calcium Hexacyanoferrate (III) Nanocatalyst Enables Redox Homeostasis for Autism Spectrum Disorder Treatment”的论文发表在最新一期《Advanced Materials》。

自闭症谱系障碍(ASD)是一种在儿童早期出现的神经精神疾病,其特征是社交沟通受损、兴趣减退和刻板重复行为。ASD病理生理学的分子机制仍未完全理解。最近的研究表明,氧化应激是自闭症的关键病理,细胞(包括大脑)中不断发生氧化还原反应。活性氧(ROS),包括过氧化物、超氧化物、羟基自由基(·OH)、单线态氧(1O2)和过氧化氢(H2O2),是氧代谢的天然副产物,在细胞信号转导和维持体内平衡中起重要作用。在正常情况下,内部氧化还原平衡由各种生物酶调节,包括超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GPx)和过氧化物酶(POD)。然而,由活细胞产生的具有高特异性和高催化效率的蛋白质或RNA在高温或酸性等条件下容易变性。近年来,人工纳米酶将纳米材料的独特性质与酶功能结合起来,在癌症、神经退行性疾病、胃肠疾病和心血管疾病的治疗中显示出显著的潜力。尽管如此,纳米酶在神经发育障碍的治疗中仍未得到充分探索。
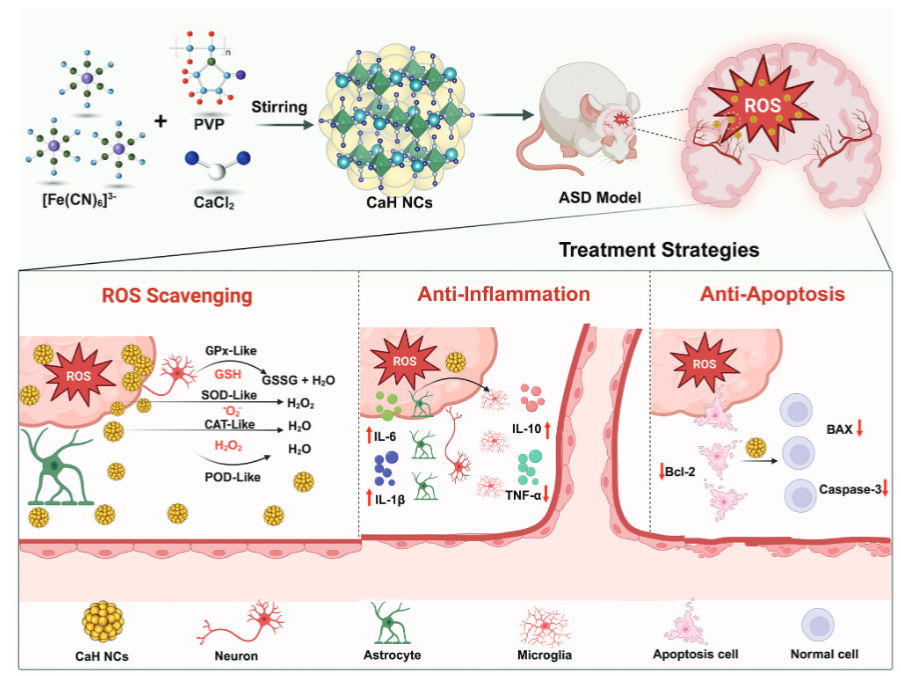
CaH NCs治疗ASD的示意图
在此,作者报告了一种工程化的六氰基铁酸钙(III)纳米催化剂,称为CaH NCs,显示出良好的生物相容性和高效的ASD治疗效果,能够有效清除过量的ROS。CaH NCs通过简便的水相置换法合成,TEM图像显示其近球形形状,直径为2.6纳米。在H2O、PBS和DMEM中的zeta电位分别为-9.4、-21.0和-9.8 mV。CaH NCs在不同条件下表现出稳定性,DLS分析显示其水动力学直径约为5.6纳米。XRD图谱表明其具有弱晶体结构,FTIR显示C≡N和C═O的特征峰,XPS分析确认了C 1s、Fe 2p和Ca 2p的存在,UV吸收显示PVP中C═O共轭双键的存在。
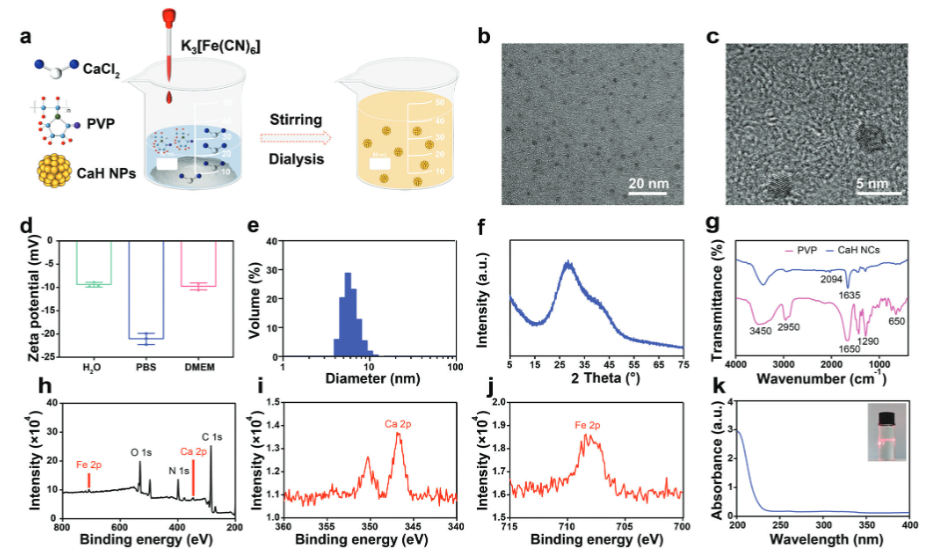
图1. CaH NCs的合成与表征
通过使用天然酶的典型底物评估了CaH NCs的酶模拟活性。总抗氧化能力(TAC)反映了样品中所有抗氧化剂的累积抗氧化能力。CaH NCs展示了多种酶模拟活性。TAC值随CaH NCs浓度增加,SOD样活性抑制福尔马赞形成。CAT是一种将H2O2转化为H2O和O2的酶,提供抗氧化防御机制。CAT样活性通过O2生成评估。POD是一种以H2O2为电子受体催化底物氧化的酶,消除H2O2和酚胺的毒性。POD样活性通过TMB显色评估,吸收随CaH NCs浓度增加。谷胱甘肽过氧化物酶(GPx)是生物体内广泛分布的重要过氧化物酶,作为抗氧化能力的重要指标。GPx样活性通过催化H2O2转化为H2O和GSH转化为GSSG展示。CaH NCs有效消除·O2−和·OH,总体表现出多种酶模拟活性和卓越的抗氧化效果。
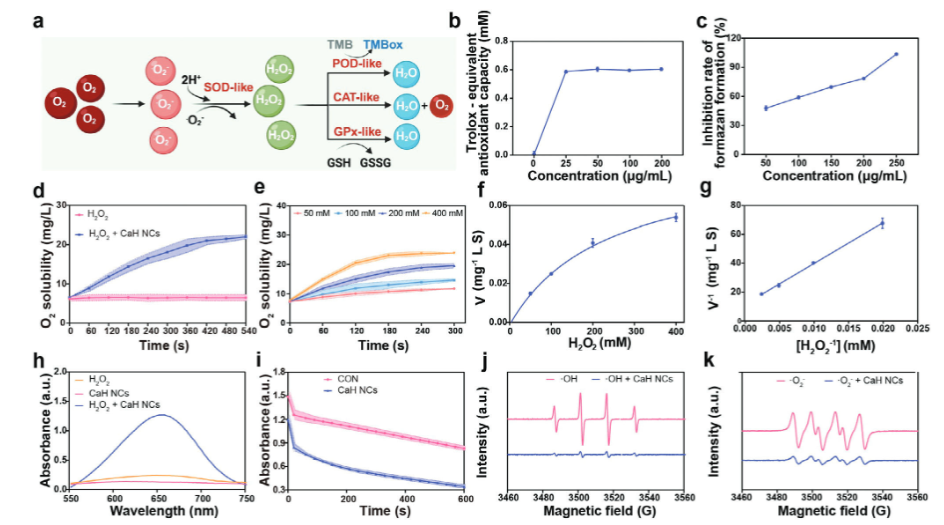
图2. CaH NCs的多种酶模拟活性和ROS清除特性
使用人和大鼠神经细胞系研究CaH NCs的细胞毒性。CCK-8结果显示,CaH NCs在高浓度下无明显毒性,表现出良好的生物相容性。红细胞溶血实验显示无显著溶血。CaH NCs显著提高H2O2和丙戊酸(VPA)诱导的氧化应激细胞存活率。DCFH-DA检测显示CaH NCs可降低ROS水平,其Cy5.5标记显示在细胞内定位于线粒体,可能有助于清除细胞内ROS。
氧化应激通过损害线粒体膜完整性诱导内源性凋亡。线粒体膜电位丧失是线粒体凋亡途径的关键事件。JC-1测定显示CaH NCs可减轻线粒体膜电位下降。Annexin V-Alexa Fluor 647/PI检测显示,CaH NCs显著降低细胞凋亡率。此外,CaH NCs减少了caspase-3和BAX的表达,上调了Bcl-2的表达。体外实验表明,CaH NCs显著降低了促炎细胞因子IL-1β、IL-6和TNF-α的水平,同时增加了抗炎因子IL-10的表达,展示了良好的抗炎效果。
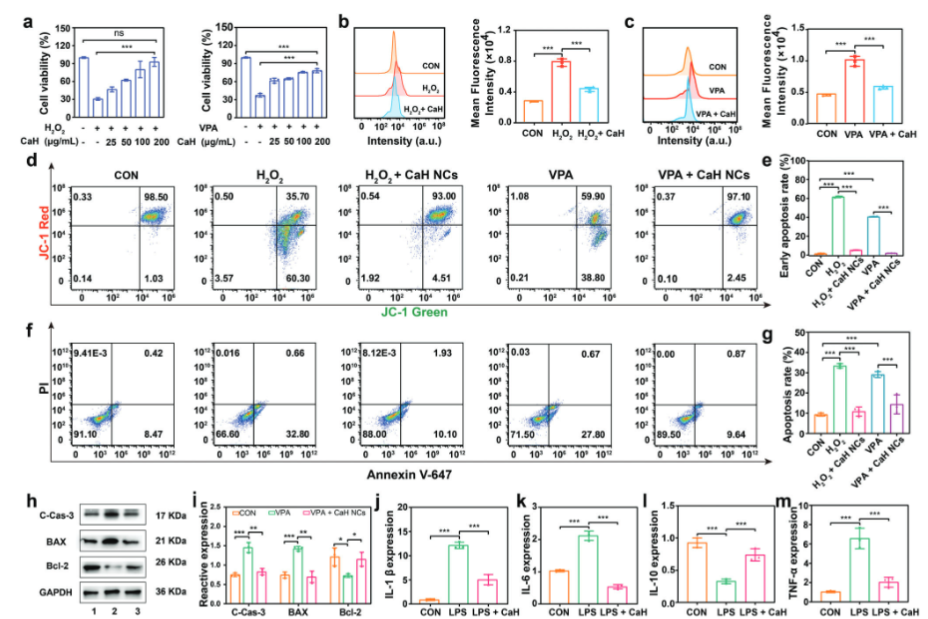
图3. 体外研究CaH NCs的细胞保护、抗氧化性能、细胞凋亡缓解和抗炎症
在评估ASD治疗效果前,首先评估CaH NCs的体内生物相容性。H&E染色和血清检测显示,注射CaH NCs后主要器官和系统无明显损伤。分布分析显示,CaH NCs主要集中在大脑,并逐渐排出体外。良好的体内生物相容性为其在ASD治疗中的应用奠定基础。使用VPA建立大鼠自闭症模型,行为评估显示,CaH NCs治疗组的社交能力、自发交替率、焦虑行为、运动和探索行为均显著改善,学习和空间记忆能力提高。
单细胞RNA测序显示,VPA诱导的大鼠脑内ROS相关基因表达显著上调。免疫荧光染色和TUNEL染色表明,CaH NCs有效降低了脑内ROS水平,减少海马区神经元凋亡。CaH NCs还减少了小胶质细胞和星形胶质细胞的激活,减轻神经炎症,保护神经细胞。治疗后,促炎标志物下调,抗炎标志物上调,表明CaH NCs有效抑制M1型胶质细胞极化。
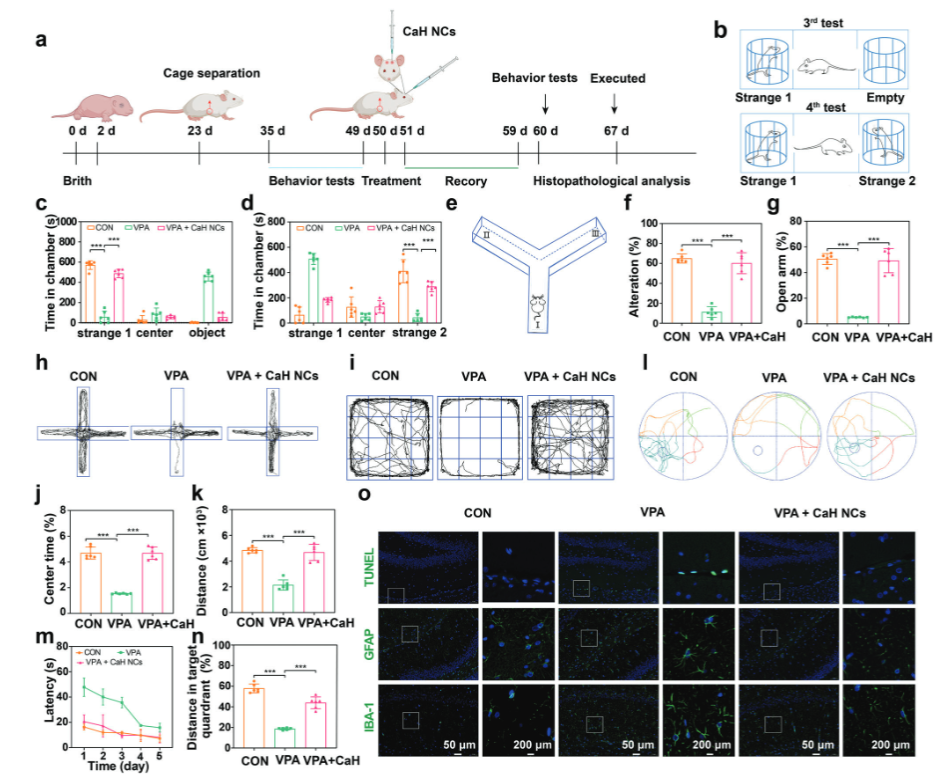
图4. CaH NCs激活ASD的体内治疗
通过mRNA测序揭示了CaH NCs在调控氧化应激、抑制凋亡和炎症中的机制。发现VPA组与CON组有373个显著差异基因,VPA + CaH NCs组与VPA组有280个差异基因。KEGG分析显示,炎症(如Toll样受体和NF-kappa B信号)及凋亡相关通路显著上调。抗凋亡和抗炎基因上调,促凋亡和促炎基因下调,蛋白-蛋白相互作用网络进一步证实了这些调控作用。
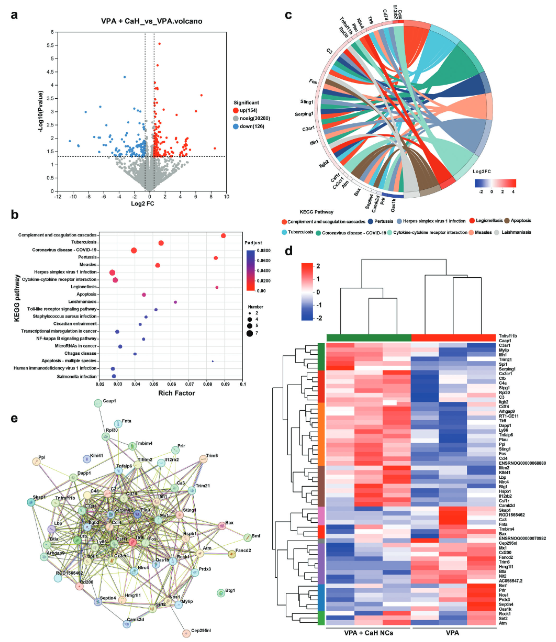
图5. CaH NCs治疗ASD的机制
对比生理盐水、VPA和VPA + CaH NCs处理的大鼠胚胎,评估CaH NCs是否能预防ASD。结果显示,VPA组的体重和睁眼评分显著低于对照组,CaH NCs组体重增加,睁眼评分提高。神经反射功能指标显示,VPA组表现差,CaH NCs改善了这一延迟。游泳测试显示CaH NCs对方向感和运动功能的改善有限。免疫荧光结果表明,CaH NCs预防组的绿色荧光显著降低,显示出其在抗凋亡和抗炎方面的显著预防效果。
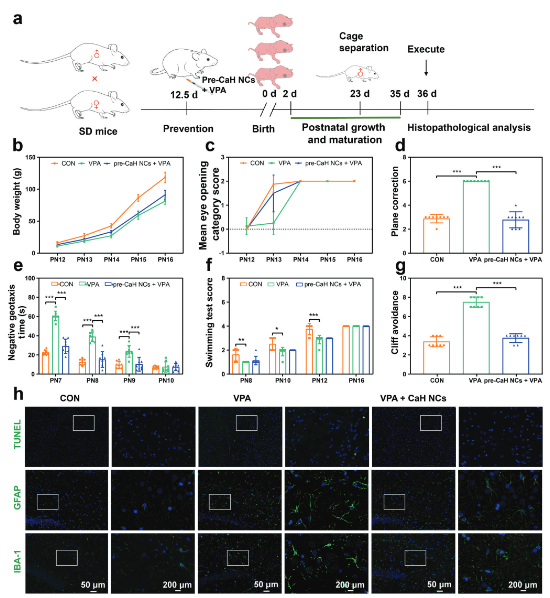
图6. CaH NCs对ASD的预防作用
总而言之,作者成功设计并制造了具有超小尺寸且稳健的CaH NCs,这些纳米催化剂能够模拟自然酶的功能,如SOD、CAT、POD和GPx。CaH NCs的多酶特性有效调控脑内ROS水平,维持线粒体膜电位,抑制细胞凋亡,并缓解神经炎症反应。这些多方面的作用协同减轻了ASD大鼠模型中的各种自闭症行为,具体表现为社交互动、运动功能、焦虑水平、重复行为、学习和空间记忆能力的改善。此外,CaH NCs在预防ASD方面也表现出显著效果,尤其是在增强神经反射功能和防止运动功能及方向感异常方面。本研究结果为利用具有ROS调节能力的多功能纳米催化剂在ASD治疗中的应用提供了明确的理论基础和具体视角。
原文链接:
https://doi.org/10.1002/adma.202405655
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#细胞凋亡# #氧化应激# #自闭症谱系障碍# #纳米酶#
70