论文解读|Chen R/Chen Z/Wang K教授团队揭示SETDB1介导的CD147-K71二甲基化促进NSCLC细胞凋亡
2024-08-15 Genes and Diseases Genes and Diseases 发表于上海
。该研究首次揭示了CD147-K71二甲基化(CD147-K71me2)通过促进细胞凋亡来抑制NSCLC进展的新机制。
非小细胞肺癌(NSCLC)作为常见的肺癌类型,其临床治疗策略已经将靶向细胞凋亡缺陷的方法应用于实践,并证实了其安全性与有效性。蛋白质翻译后修饰(PTMs),包括磷酸化、甲基化、泛素化和乙酰化等,在调控肿瘤发展过程中起着至关重要的作用。肿瘤生物标志物CD147,其多样的PTMs被发现能够促进肿瘤的转移和代谢重编程。尽管如此,CD147的PTMs与细胞凋亡之间的直接联系尚未完全阐明。
第四军医大学的Ruo Chen/ Zhinan Chen/ Ke Wang教授团队在本刊发表了题为“SETDB1-mediated CD147-K71 di-methylation promotes cell apoptosis in non-small cell lung cancer”的研究论文。该研究首次揭示了CD147-K71二甲基化(CD147-K71me2)通过促进细胞凋亡来抑制NSCLC进展的新机制。
01 CD147-K71me2抗体的制备及鉴定
研究团队通过二甲基化肽段免疫,制备了特异性的CD147-K71me2抗体,并在NSCLC组织中鉴定了其表达水平,发现CD147-K71me2在肿瘤组织中的表达低于邻近正常组织,提示其可能与NSCLC的进展呈负相关(图1)。
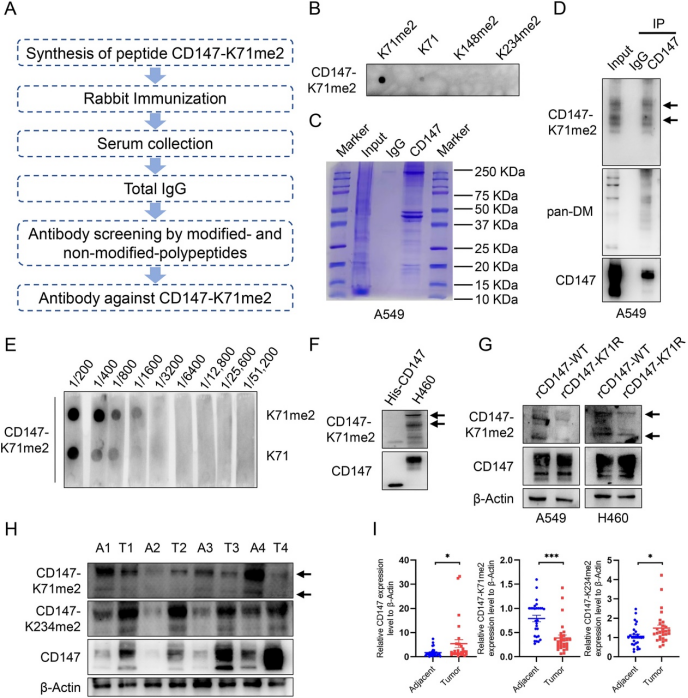
图1.抗CD147-K71me2抗体的制备及其在NSCLC中的鉴定(原文中Figure 1)。
02 SETDB1作为CD147-K71me2的甲基转移酶
通过siRNA库筛选,研究团队发现SETDB1是催化CD147生成CD147-K71me2的甲基转移酶,并通过共免疫沉淀和免疫荧光实验验证了两者之间的相互作用,SETDB1的过表达能够增强CD147-K71me2的表达水平(图2)。
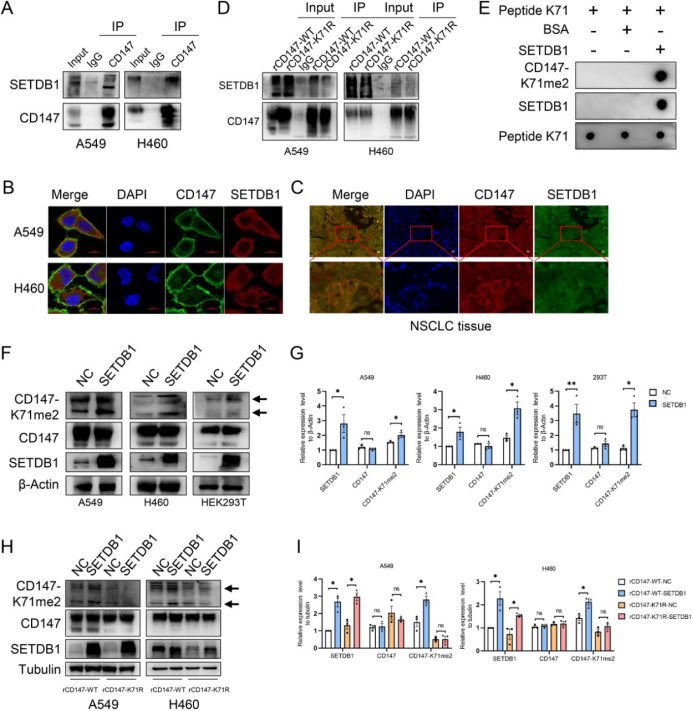
图2.SETDB1催化CD147生成CD147-K71me2(原文中Figure 3)。
03 CD147-K71me2通过FOSB促进肿瘤细胞凋亡
RNA测序分析发现,FOSB是野生型CD147 (CD147-WT) 和突变型CD147 (CD147-K71R) 细胞之间差异表达最显著的基因。进一步实验表明,CD147-K71me2通过增强p38的磷酸化,促进FOSB的表达,进而触发肿瘤细胞的凋亡过程(图3)。
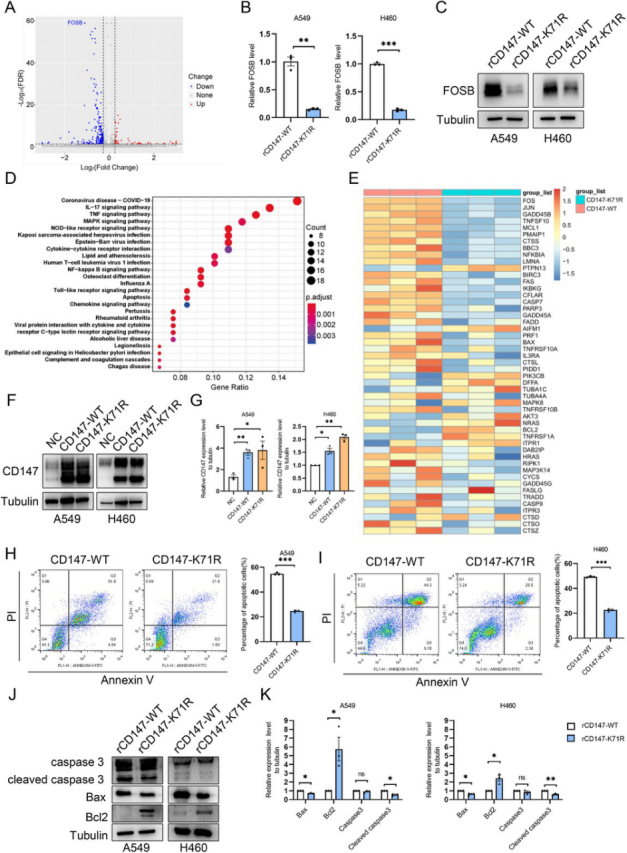
图3.CD147-K71me2上调FOSB表达并促进肿瘤细胞凋亡(原文中Figure 4)。
04 CD147-K71me2在体内抑制NSCLC进展
通过在裸鼠中进行的体内实验,研究团队进一步证实了CD147-K71me2能够显著抑制肿瘤的体积和重量增长,并通过促进细胞凋亡来实现这一效果。与野生型CD147相比,突变型CD147组的肿瘤体积和重量均显著增加,而凋亡水平则相对较低(图4)。
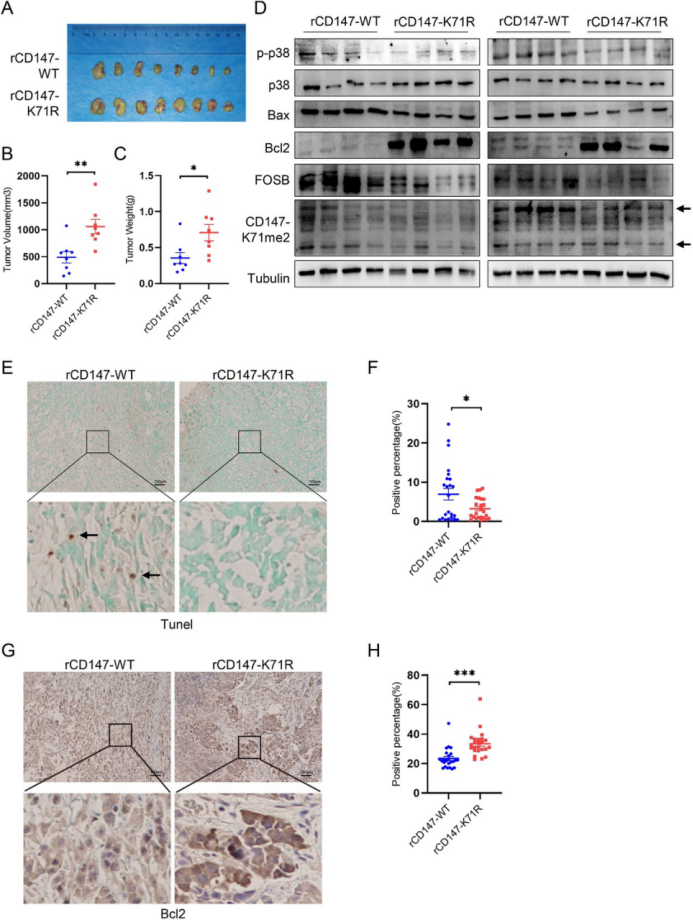
图4.CD147-K71me2通过促进细胞凋亡抑制NSCLC的进展(原文中Figure 7)。
该研究揭示了SETDB1介导的CD147-K71me2在NSCLC进展中通过促进细胞凋亡来抑制肿瘤的新机制,不仅为理解CD147在NSCLC进展中的作用提供了新的视角,而且为开发新的肿瘤治疗策略提供了潜在的分子靶标。
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304223000673
引用这篇文章:
Shi MY, Wang Y, Shi Y, et al. SETDB1-mediated CD147-K71 di-methylation promotes cell apoptosis in non-small cell lung cancer. Genes Dis. 2024;11(2):978-992.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#非小细胞肺癌# #NSCLC# #细胞凋亡#
67