增强NK细胞疗法的纳米技术
7小时前 小药说药 小药说药 发表于陕西省
本文阐述 NK 细胞免疫疗法现状及局限,介绍纳米技术在提升其免疫治疗效率的五个领域作用,包括辅助免疫调节等,指出纳米颗粒助 NK 细胞免疫治疗前景广阔。
前言
自然杀伤(NK)细胞是抵御感染和恶性肿瘤的第一道防线之一。基于NK细胞的免疫疗法正在成为基于T细胞的免疫治疗的替代方案。在过去的几十年中,基于NK细胞的免疫疗法的临床前和临床研究在恶性血液肿瘤展现了有希望的结果。
然而,基于NK细胞的免疫疗法仍有局限性,例如在实体瘤中的表现有限/治疗效率低、NK细胞的寿命短、过继转移和基因修饰的特异性有限、患者免疫系统对NK细胞的排斥、NK细胞向肿瘤微环境(TME)的浸润、以及治疗的昂贵费用。新兴的纳米技术可以提高NK细胞的功能、实时分析其性能并提高免疫治疗效率,潜在地帮助激活、增殖并增强NK细胞的细胞毒性活性。目前,纳米技术在五个不同领域可以提高免疫治疗效率:纳米颗粒辅助免疫调节以提高NK细胞活性、纳米颗粒增强NK细胞归巢、纳米颗粒递送RNAi以增强NK细胞活性,基于纳米颗粒的NK细胞遗传调节,以及纳米颗粒激活NKG2D。因此,纳米技术可能会增强基因NK细胞的免疫疗法,并克服各种实体癌的免疫抑制环境。
纳米颗粒辅助免疫调节增强NK细胞活性
作为免疫调节剂的纳米颗粒可以提高免疫治疗的效果,并克服传统癌症治疗方法的局限性。一些纳米颗粒可用于递送抗癌药物、趋化因子和细胞因子,基于脂质的纳米颗粒可以包裹这些分子,并有效地将其输送到肿瘤部位。
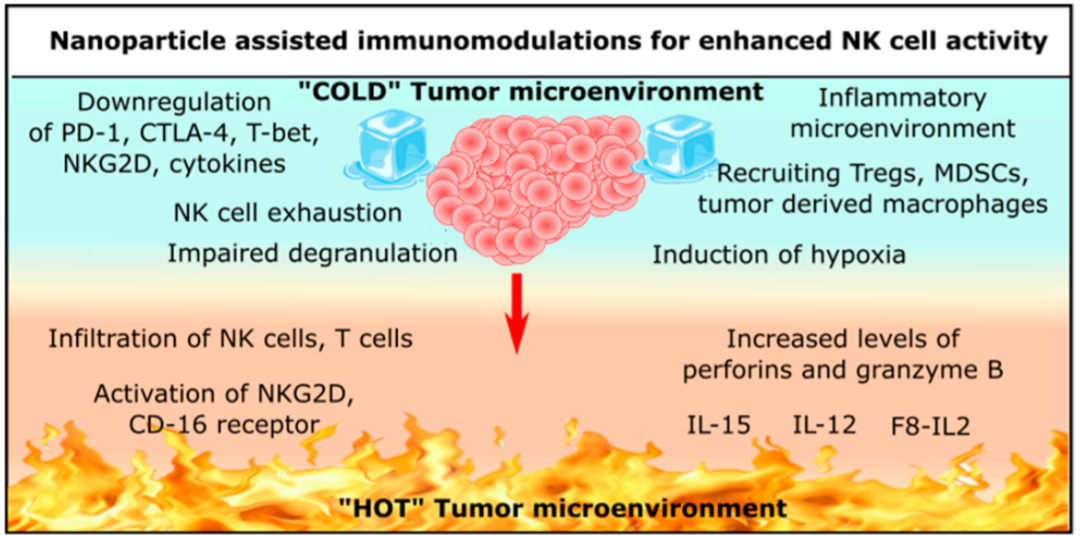
另一种策略涉及使用表面工程纳米颗粒;聚合物或金属基纳米颗粒可以被修饰,使得肿瘤抗原或抗体可以对接到表面上。例如,硒基纳米颗粒可以增强NK细胞的功能,还诱导非特异性体液和细胞介导的免疫反应,并提高IL-17和IFN-γ表达。钌纳米颗粒用双特异性抗体(SSFc、抗CD16和抗CEA)修饰,这些抗体通过刺激NK细胞诱导坏死和凋亡来触发免疫反应。
纳米颗粒增强NK细胞归巢
归巢是免疫细胞上的归巢受体和肿瘤分泌归巢配体之间的一种信号传导模式,肿瘤微环境中的这些相互作用可以招募更多的效应免疫细胞,并增强免疫细胞浸润。癌细胞分泌细胞因子和趋化因子,如TNF-α和ROS,这些信号可以诱导炎症或激活细胞毒性活性。其中一些细胞因子诱导效应免疫细胞,通过激活T细胞、B细胞和NK细胞来杀死癌细胞。NK细胞在细胞毒性介导的肿瘤细胞杀伤中起着至关重要的作用,因此,在肿瘤微环境中诱导NK细胞归巢对于有效遏制肿瘤至关重要。
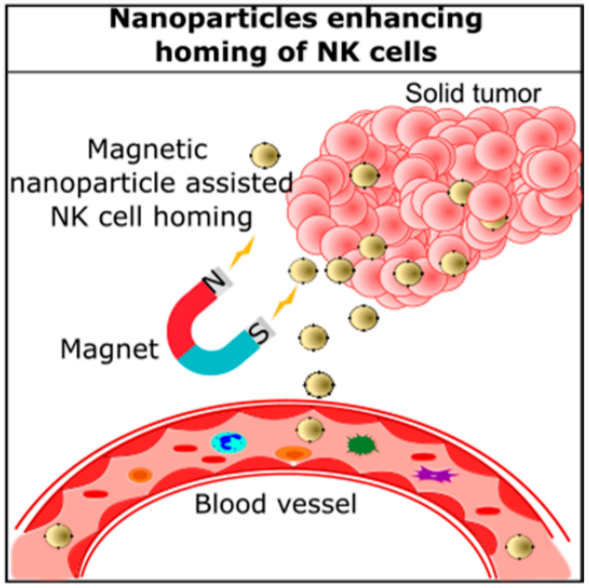
纳米颗粒,特别是磁性纳米颗粒,用于归巢免疫细胞的用途已经被广泛探索。例如,氧化铁纳米颗粒在原代NK细胞表面的结合将显著增强NK细胞在肿瘤微环境中的归巢。与未修饰的NK细胞相比,这些纳米颗粒通过增加神经母细胞瘤细胞中颗粒酶和穿孔素的表达,显示出显著的抗肿瘤功效。此外,NK细胞对癌细胞的杀伤与NK细胞的归巢以及外部磁引导相关。
基于纳米颗粒的NK细胞归巢的发展有多种策略。其中一些策略涉及使用磁性纳米颗粒递送效应分子,如颗粒酶、膜结合热休克蛋白和细胞因子,如IL-12,这不仅增强归巢,还激活NK细胞或杀死肿瘤细胞。
纳米颗粒递送RNAi以增强NK细胞活性
RNA效应物如siRNA、miRNA和shRNA可以沉默特定基因,从而改变基因组功能并增强抗肿瘤活性。使用这些RNA效应物可以增强NK细胞活性,例如,二氧化锰(MnO2)纳米颗粒系统用于递送靶向转化生长因子β受体-2(TGFBR2)的小干扰RNA(siRNA),已知其抑制NK细胞的功能。这些负载有TGFBR2 siRNA的纳米颗粒通过抑制TGFBR2保护NK细胞免受免疫抑制。
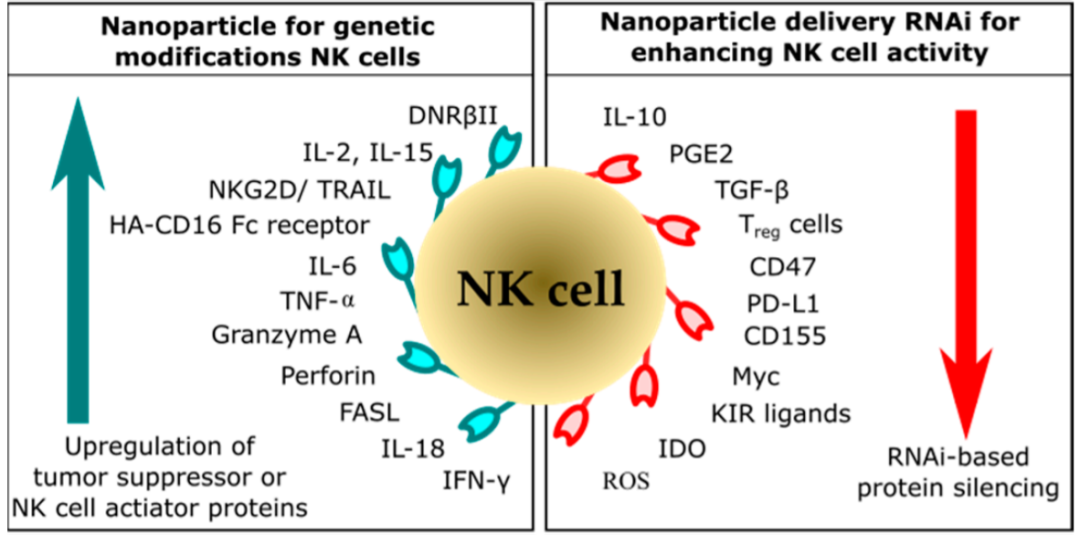
靶向EpCAM含有si-CD47和si-PD-L1的阳离子脂质体已用于阻断免疫抑制CD47和PD-L1。这些脂质体有效地阻止了4T1荷瘤小鼠的肿瘤生长并减少了肺转移。这些siRNA可以略微增加NK细胞的百分比,促进NK细胞反应,也可以增加抗体的产生。
此外,通过将NK细胞衍生的外泌体与miRNA负载的仿生纳米颗粒相结合,开发了一种新的鸡尾酒策略,用于将治疗性miRNA靶向递送至神经母细胞瘤细胞。他们将NK细胞衍生外泌体与miRNA-186结合,这些外泌体对MYCN基因扩增的神经母细胞瘤细胞系表现出显著的细胞毒性。此外,细胞毒性依赖于miRNA-186的表达。体外研究表明,这些外泌体诱导TGF-β的下调。这些结果表明,负载miRNA-186的NK细胞衍生外泌体是一种有前途的治疗方法,可促进NK细胞的细胞毒性,并阻断肿瘤细胞的免疫逃逸。
用于NK细胞遗传修饰的纳米颗粒
了解NK细胞生物学及其与肿瘤微环境的相互作用,有助于修饰NK细胞,以实现更好的NK细胞免疫治疗。基于纳米颗粒的遗传修饰和嵌合抗原受体(CAR)-NK细胞也在开发之中。
负载IL-2和NKG2D基因的壳聚糖纳米颗粒在体外可以激活NK细胞和细胞毒性T细胞。与体外结果一致,在CT-26荷瘤小鼠中也观察到肿瘤体积减少和存活时间延长。
在另一项独立研究中,壳聚糖纳米颗粒成功地将IL-15和NKG2D基因输送到癌细胞中。这些含有NKG2D-IL-15融合蛋白基因的纳米颗粒与细胞毒性T细胞和NK细胞的NKG2D受体结合并有效激活NK细胞。IL-15和NKG2D融合蛋白通过激活>5%的细胞毒性T细胞和>50%的NK细胞,增强了B16BL6黑色素瘤细胞的抗肿瘤免疫应答。
激活NKG2D受体的纳米颗粒
NKG2D是一种在NK细胞、NKT细胞和细胞毒性T细胞上表达的C型凝集素样激活受体。NKG2D的配体可以启动NKG2D信号通路,从而导致免疫细胞的激活和增殖。
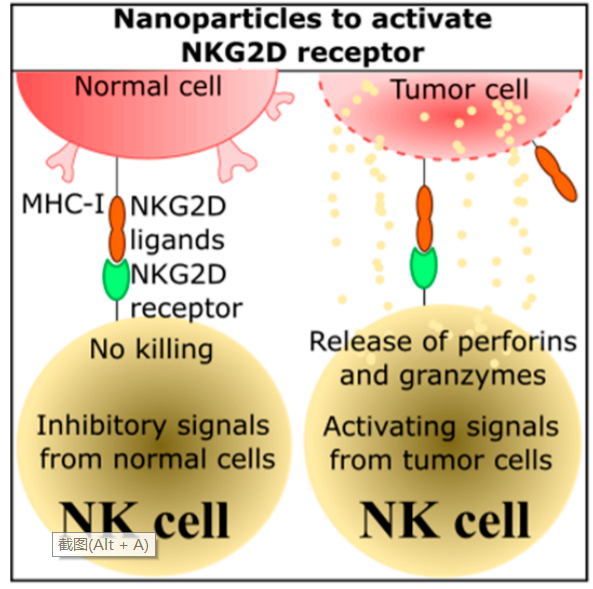
NKG2D受体启动ITAM(基于酪氨酸的激活基序)信号传导。一旦信号被触发,共刺激分子CD28和ICOS被触发,并导致一系列反应,最终导致PI3K的激活,包括涉及转录因子的反应。这些途径的激活需要靶向递送NKG2D配体或某些细胞因子,纳米颗粒可以有效介导这些配体的递送。
小结
纳米颗粒在各种临床前研究中已经被证明具有巨大的潜力,纳米颗粒可以在许多方面帮助NK细胞,包括其活化、增殖、释放肿瘤抗原和抵抗肿瘤的免疫抑制微环境。辅助免疫治疗的纳米颗粒由于其尺寸小和纳米颗粒的多样性而具有很好的应用前景。
虽然纳米颗粒与NK细胞的相互作用还有很多有待了解,但目前的研究表明,在开发基于纳米颗粒的免疫调节药物以进一步提高免疫治疗的有效性方面,前景广阔。
参考文献:
1.Nanoparticle Enhancement of Natural Killer (NK) Cell-Based Immunotherapy. Cancers (Basel).2022 Nov 4;14(21):5438
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#免疫疗法# #NK细胞#
2