【JCO】奥加伊妥珠单抗+低强度化疗治疗新诊断老年CD22+ Ph阴性BCP-ALL
2024-10-24 聊聊血液 聊聊血液 发表于上海
研究评估奥加伊妥珠单抗联合低强度化疗治疗老年费城染色体阴性急性淋巴细胞白血病,结果显示有效性和耐受性良好,或可成新标准治疗。
奥加伊妥珠单抗
老年费城染色体阴性急性淋巴细胞白血病 (Ph- ALL)在当前化疗下预后不佳,存在未满足的治疗需求。在大多数前体B细胞(BCP) ALL患者(>90%)表达表面CD22抗原,因此可作为免疫治疗干预的理想靶点。奥加伊妥珠单抗 (InO)是一种偶联抗CD22单克隆抗体,正在成为老年ALL患者中一种有希望的一线治疗方法。因此学者开展一项II期研究中,纳入131例新诊断CD22+ Ph- BCP-ALL老年患者,评估了5次分剂量InO(总剂量2.8 mg/m2)联合低强度化疗的安全性和有效性。近日发表于《Journal of Clinical Oncology》,该研究也是评估InO作为新诊断CD22+ Ph- BCP-ALL老年患者一线治疗的最大样本多中心前瞻性研究。

研究方法&结果
EWALL-INO是一项开放标签、前瞻性、多中心II期研究,在欧洲三个国家开展,纳入≥55岁新诊断CD22+费城染色体阴性B细胞前体(BCP)ALL。在类固醇激素前期阶段后,第一次诱导包括长春新碱、地塞米松和三次注射InO (第1天0.8mg/m2,第8天/第15天0.5mg/m2),随后第二次诱导包括环磷酰胺、地塞米松和两次注射InO (第1天/第8天0.5mg/m2)。缓解患者接受6个周期的化疗巩固和18个月的化疗维持。三次巩固后允许异基因移植。主要终点为1年总生存期(OS)。

共纳入131例患者(中位年龄68岁)。3例患者在诱导1期间死亡(n=130接受诱导1),2例死于多器官功能衰竭,1例死于出血,诱导2期间无患者死亡(n=120接受诱导2)。诱导2后,90%的患者达到完全缓解(CR)或CR伴血小板不完全恢复(CRp),80%的患者达到可测量残留病(MRD2) <10-4。
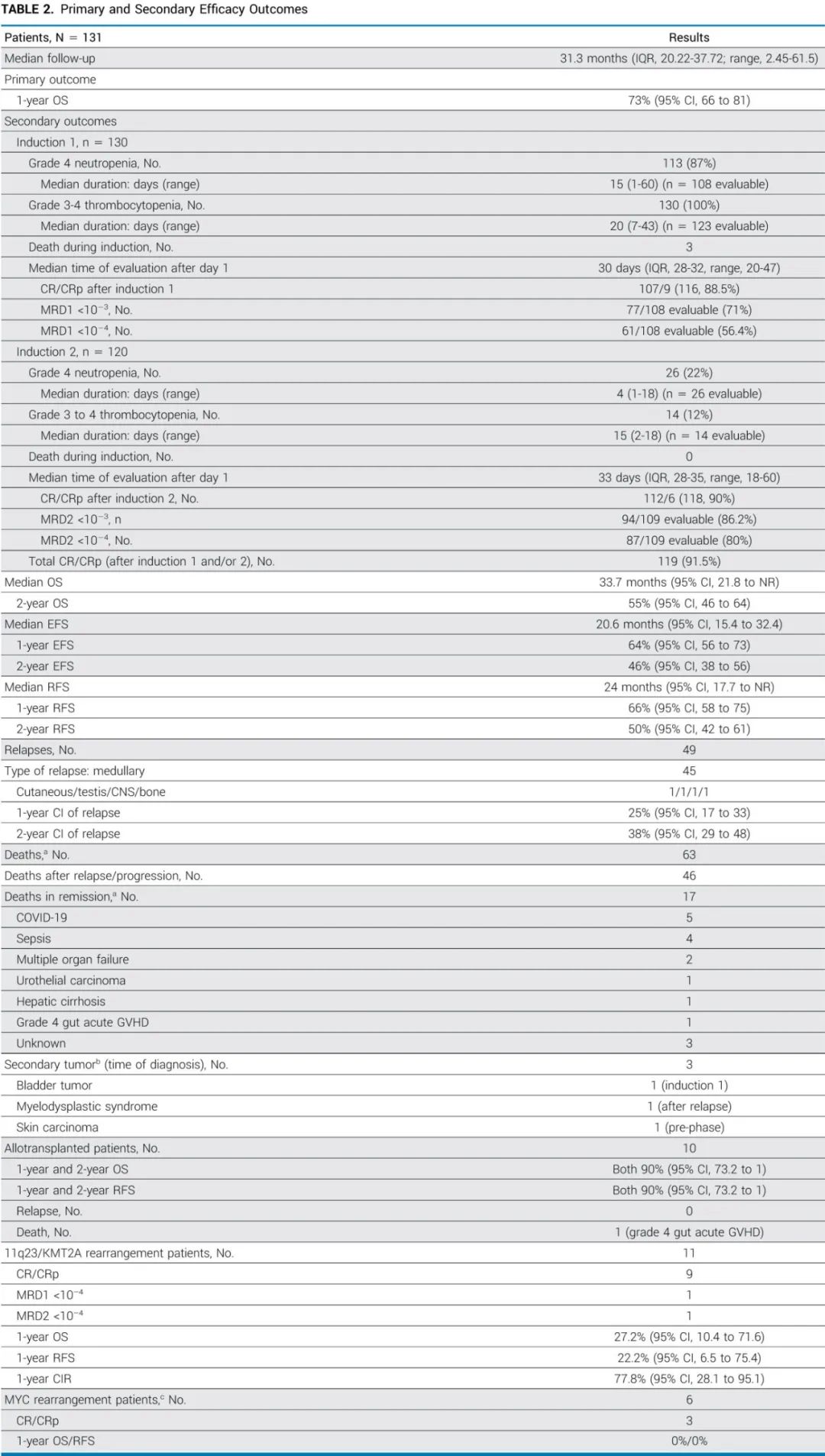
中位随访31.3个月,中位OS为33.7个月,1年和2年OS为73%和55%,达到主要终点。中位无事件生存期(EFS)为20.6个月,1年和2年EFS为64%和46%。
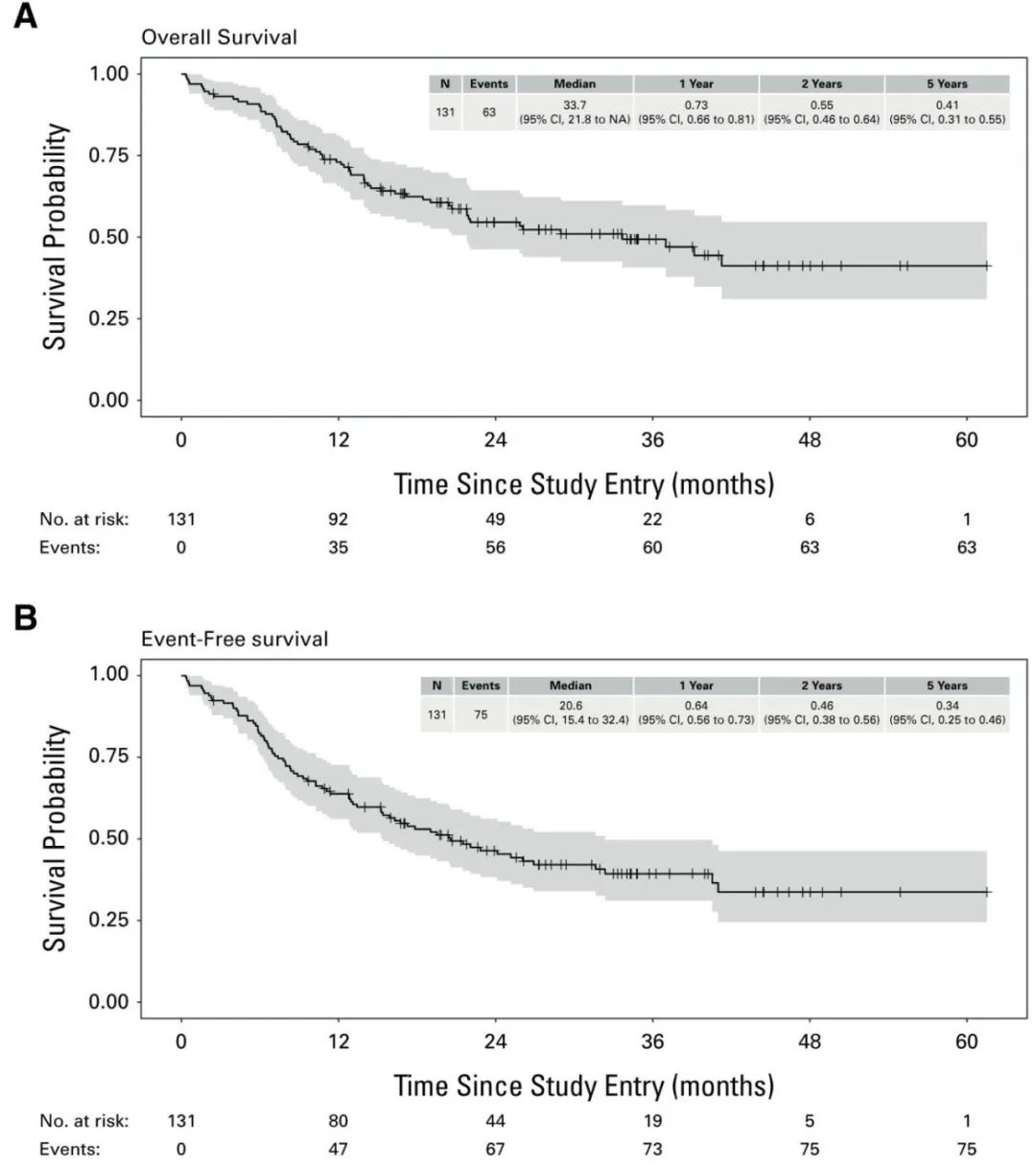
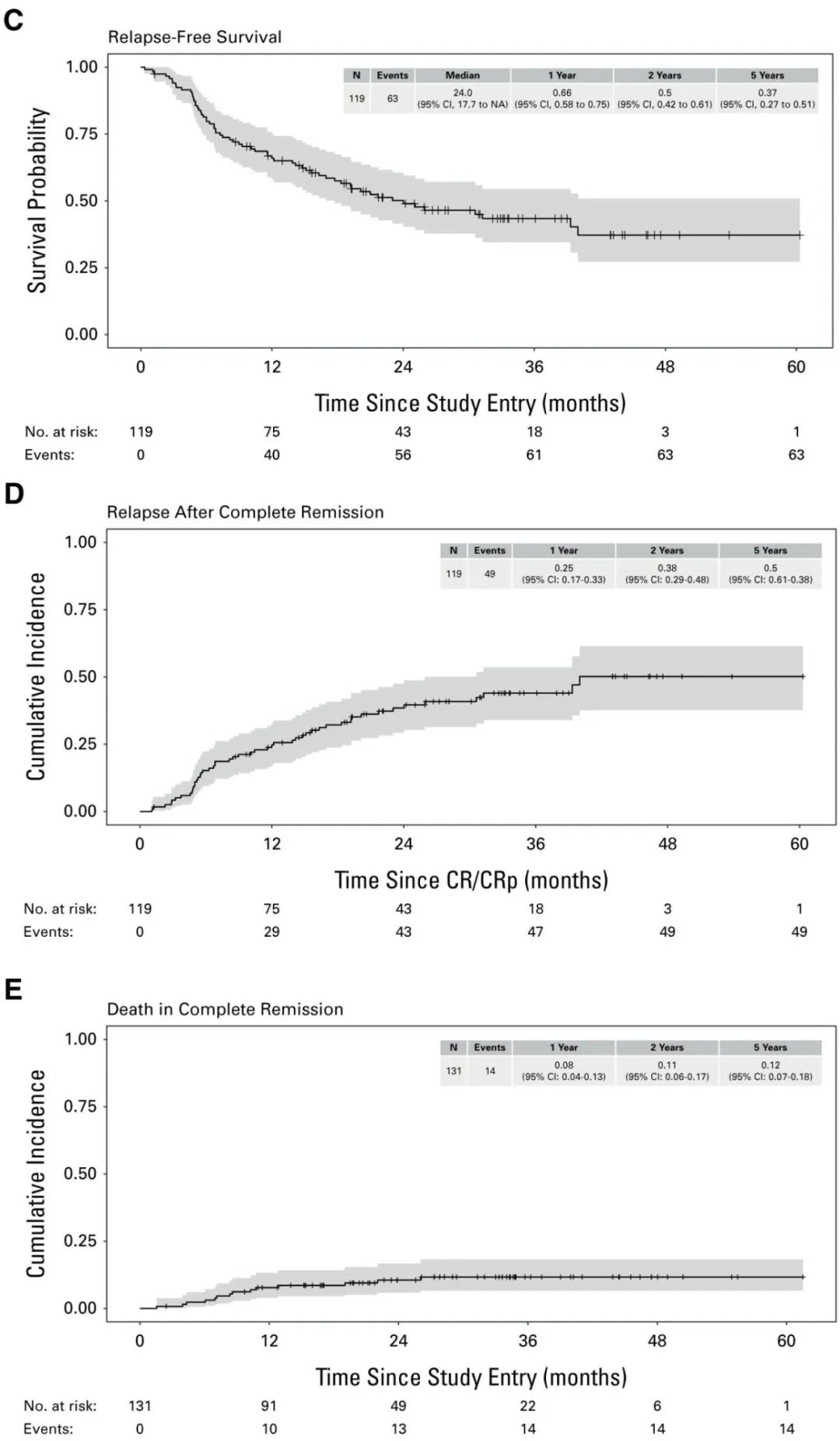
在CR/CRp缓解者(n=119)中,47例复发,14例在CR/CRp期间死亡,中位OS为39.1个月,中位无复发生存期(RFS)为24个月;1年OS、RFS和累积复发率(CIR)分别为73.2%、66%和25%,2年RFS为50%。CR/CRp期间死亡的1年和2年发生率分别为8%和 11%。10例异基因移植患者的预后非常好(2年OS/RFS均为90%,无复发)。
高危细胞遗传学和低CD22表达(<70%)与较差的OS相关,而高危细胞遗传学和MRD2≥10-4与较低的RFS和较高的CIR相关。
诱导1期间4级中性粒细胞减少和3-4级血小板减少的发生率分别为87%和100%,诱导2期间为22%和12%。所有AE中,7%发生于前期、44%在诱导1期、11.5%在诱导2期、24%在巩固期、7.5%在维持期、6%在末次给药后;3-4级AE中分别为7%、41%、8%、28%、11%、5%;5起5级AE均发生于诱导2之后。研究仅记录一例非致命性肝窦阻塞综合征(SOS)。
总结
该研究结果优于传统化疗,证实对于老年CD22+ Ph- BCP-ALL患者,分次InO联合低强度化疗是一种非常有效且耐受性良好的一线治疗方案,如果在III期前瞻性研究中得到证实,则或许可以作为新的标准治疗。
参考文献
Chevallier P,et al.Inotuzumab Ozogamicin and Low-Intensity Chemotherapy in Older Patients With Newly Diagnosed CD22+ Philadelphia Chromosome–Negative B-Cell Precursor Acute Lymphoblastic Leukemia.J Clin Oncol . 2024 Oct 17:JCO2400490. doi: 10.1200/JCO.24.00490.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#急性淋巴细胞白血病# #奥加伊妥珠单抗#
16