European Radiology:通过深度学习实现全剂量脑PET容量的定量评估
6小时前 shaosai MedSci原创 发表于陕西省
近年来,卷积神经网络(CNN)在从LD数据中恢复FD PET图像方面显示出了巨大的潜力。最近,生成式对抗网络(GAN)通过使用判别器网络进行对抗训练,展示了保留高频结构细节的能力。
现阶段,正电子发射断层扫描(PET)广泛应用于临床诊断、治疗评估和预后预测。高质量的PET图像通常伴随着相对高剂量的放射性示踪剂,这引起了人们对辐射暴露风险的担忧。为了将辐射风险降到最低,一种策略是减少注射剂量。然而,这将导致低质量的PET图像,这可能会降低诊断效率。因此,研究如何从低剂量(LD)数据中恢复全剂量(FD) PET图像,在保证图像质量的同时将辐射风险降至最低,具有重要的临床意义。
近年来,卷积神经网络(CNN)在从LD数据中恢复FD PET图像方面显示出了巨大的潜力。最近,生成式对抗网络(GAN)通过使用判别器网络进行对抗训练,展示了保留高频结构细节的能力。有学者提出了使用条件生成对抗网络(C-Gan)从LD数据中恢复FD PET图像,并验证了C-Gan的性能优于基于cnn的方法。也有学者提出使用C-Gan对LD数据中的FD PET图像进行交叉扫描和交叉示踪恢复。然而,这些方法只侧重于恢复二维轴向图像,而忽略了PET体积的三维特征。当沿着矢状面和冠状面切片观察时,由恢复的轴向切片堆叠的3D PET体积会丢失细节。
高质量的3D PET体积对于准确诊断非常重要。据观察,从不同的图像方向检查病变可以提高诊断的可靠性。然而,3D PET体积恢复的3D方法的发展并非没有挑战。具体来说,体积数据很大,需要大量的GPU(图形处理单元)内存来训练DL模型,有时超出了硬件资源的可用性。因此,与2D模型相比,3D DL模型的深度或输入样本大小必须协调一致。

最近,发表在European Radiology 上的一篇文章提出了一种深度学习(DL)方法来减少PET研究的放射性示踪剂剂量,同时保证了诊断质量。
本项研究对456名参与者进行了回顾性研究,分别使用三种不同的PET扫描仪和两种不同的示踪剂进行扫描。研究提出了一种空间感知降噪网络(SANR)从LD数据中恢复三维全剂量PET体积的DL方法。将SANR的性能与以常规FD PET体积为参考的2D DL方法进行比较。采用Wilcoxon符号秩检验比较不同深度去噪方法的图像质量指标。为了进行临床评估,由两位核医学医生使用5分评分方案(5 =优秀)检查了恢复的FD PET体积,并给出了诊断质量评估的二元决定(阴性或阳性)。
在图像质量指标方面,SANR与2D DL方法比较差异有统计学意义(p < 0.05)。对于临床评价,SANR的病变检测准确率为95.3% (95% CI: 90.1%, 100%),而参考全剂量PET体积的病变检测准确率为98.4% (95% CI: 95.4%, 100%)。在阿尔茨海默病的诊断中,参考FD PET体积和通过SANR恢复的FD PET体积具有相同的准确性。
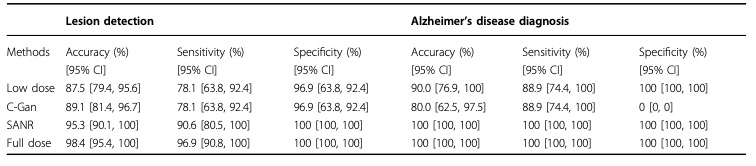
表 剂量减少因子(DRF)为20时摄取状态读数的准确性、灵敏度和特异性
本项研究表明,与参考FD PET相比,该方法降噪后的LD PET显着降低了示踪剂剂量,在脑病变检测和阿尔茨海默病诊断中具有良好的诊断效果。
原始出处:
Rui Guo,Jiale Wang,Ying Miao,et al.3D full-dose brain-PET volume recovery from low-dose data through deep learning: quantitative assessment and clinical evaluation.DOI:10.1007/s00330-024-11225-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#深度学习# #脑PET#
3