Rheumatology:从依那西普原研药转换至生物类似药的类风湿性关节炎(RA)患者的药物持续性及疾病活动性变化
2024-08-27 潘华 MedSci原创 发表于上海
转换至生物类似药的患者与继续使用原研药的患者在药物持续性和疾病活动性方面没有显著差异。
依那西普是一种TNF抑制剂,自2000年代初被批准用于治疗类风湿性关节炎(RA)以来,一直是常用的生物制剂。随着依那西普原研药专利于2015年到期,生物类似药进入市场,这种低成本的替代品使得许多已接受依那西普原研药治疗的患者出于成本考虑被转换至生物类似药。然而,由于生物类似药和原研药在制造工艺上存在差异,临床效果可能存在不确定性。因此,本研究旨在评估因非医疗原因从依那西普原研药转换至生物类似药的RA患者的药物持续性及疾病活动性变化,并与继续使用原研药的患者进行比较。

本研究使用英国类风湿性关节炎生物制剂注册(BSRBR-RA)数据库的数据,选择了直接从依那西普原研药转换至生物类似药的1024名RA患者,并与1024名继续使用原研药的匹配患者进行比较。匹配标准包括性别、年龄、疾病持续时间和原研药开始治疗的年份。药物持续性通过Kaplan-Meier生存估计法计算,并使用Cox比例风险模型评估两组患者在药物持续性上的差异。此外,还比较了两组患者在转换后6个月和12个月的疾病活动性(通过DAS28评分)变化。为了处理数据中的缺失值,研究采用了多重插补方法。
研究结果显示,转换至生物类似药的患者与继续使用原研药的患者在药物持续性和疾病活动性方面没有显著差异。在三年后,约65%的患者仍在接受依那西普治疗。此外,9%的生物类似药组患者在转换后的第一年内切换回原研药。6个月和12个月后,转换至生物类似药的患者在DAS28评分上的恶化概率并不高于继续使用原研药的患者。具体而言,转换后6个月,生物类似药组的DAS28中位数为3.1,原研药组为2.8;转换后12个月,两组的DAS28中位数分别为2.8和3.0。
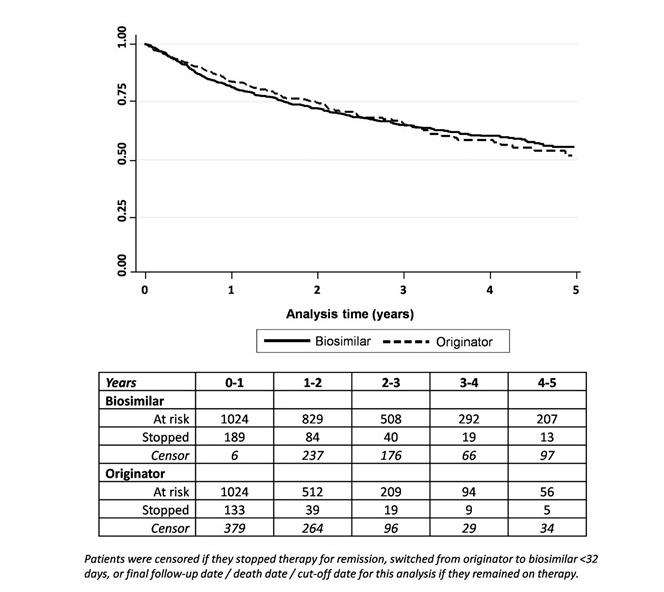
按队列分层的依那西普自索引日期(生物类似药患者转换日期,原研药患者匹配日期)的治疗持续性
本研究是关于RA患者从依那西普原研药转换至生物类似药的对比研究。结果表明,这些患者在药物持续性和疾病控制方面与继续使用原研药的患者表现相当,这对临床医生和患者在面临非医疗原因转换时具有重要的参考价值。
原始出处:
Outcomes following switching from etanercept originator to etanercept biosimilar in 1024 patients with RA: a matched-analysis of the BSRBR-RA, Rheumatology, Volume 63, Issue 8, August 2024, Pages 2082–2092, https://doi.org/10.1093/rheumatology/kead470
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















依那西普是一种TNF抑制剂,自2000年代初被批准用于治疗类风湿性关节炎(RA)以来,一直是常用的生物制剂。
71
#生物类似药# #类风湿性关节炎(RA)#
86