Adv Sci:西南医科大学欧贤红/尹世刚/谭晓秋合作发表通过单细胞测序解读心力衰竭机制的综述
2024-08-21 iNature iNature 发表于上海
该综述重点关注单细胞测序技术对HF潜在机制的见解,并讨论当前心血管研究中遇到的挑战。
心力衰竭(HF)是一种常见的心血管疾病,在世界范围内具有较高的发病率和死亡率。由于心脏结构复杂、细胞类型多样以及HF的复杂发病机制,需要进一步深入研究其潜在机制。阐明心肌细胞的异质性和细胞间通讯网络尤为重要。传统的高通量测序方法只能提供基因表达的平均测量值,无法捕捉细胞之间的“异质性”,影响基因功能知识的准确性。相比之下,单细胞测序技术可以在单个细胞水平上扩增整个基因组或转录组,从而以无与伦比的精度检查基因结构和表达。这种方法为了解疾病机制提供了宝贵的见解,能够识别与HF相关的肥大过程中细胞成分和基因表达的变化。此外,它揭示了HF微环境中不同的细胞群及其独特作用,从而全面了解HF发病机制背后的细胞格局。
2024年8月19日,西南医科大学欧贤红、尹世刚、谭晓秋共同通讯在Advanced Science 在线发表题为“From Cell to Gene: Deciphering the Mechanism of Heart Failure With Single-Cell Sequencing”的综述文章,该综述重点关注单细胞测序技术对HF潜在机制的见解,并讨论当前心血管研究中遇到的挑战。

心力衰竭(HF)是许多心脏疾病的终末阶段,是心脏功能障碍的严重过程。心脏细胞损伤的不可逆性使治疗心脏病,尤其是HF变得极具挑战性。多种异质性细胞精细地整合在心脏中,在细胞水平上了解各种细胞类型的发育过程、细胞类型和基因表达模式更有利于HF的精准治疗。单细胞测序(SCS)近年来取得了长足的发展。
第一种单细胞RNA测序(scRNA-seq)方法于2009年开发,但直到2015年,scRNA-seq技术才得到广泛应用。此后,已经开发了多种SCS方法,包括DNA和RNA测序。这些进展为研究人员在单细胞水平上探索以前未知的细胞类型、隐藏的基因表达模式和基因突变的影响开辟了新的机会,从而可以深入分析具有HF的高度异质性的心脏组织。此外,SCS能够进行细胞轨迹分析,这对于阐明心脏发育和祖细胞分化过程中的细胞状态转变以及基于基因表达预测配体-受体结合的细胞间通讯至关重要,为疾病的发生、结果和治疗提供新的见解。
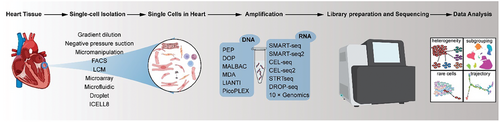
图1 单细胞测序的基本流程(图源自Advanced Science )
SCS的基本流程如图1所示,细胞的质量是SCS成败的先决条件,因此单细胞分离和样品制备对整个流程至关重要。根据样品的类型、状态和分析目的,已经开发出各种单细胞分离和提取方法,主要包括梯度稀释法、负压抽吸法、显微操作法、荧光激活细胞分选(FACS)、激光捕获显微切割(LCM)、微阵列技术、微流控技术、液滴技术以及ICELL8 cx单细胞系统。表1显示了这些方法的详细比较。然而,心脏致密的结构组织和胶原蛋白的存在使心肌细胞(CM)对缺氧特别敏感,对它们的分离提出了重大挑战。为了解决心脏scRNA-seq研究中的这个问题,See等人修改了一个成熟的单核RNA测序(snRNA-seq)微流控平台。尽管细胞质RNA丢失了,snRNA-seq成功保留了新生的初始转录本类型并产生了丰富的非编码RNA。与细胞对应物相比,细胞核的稳定性,同时保留了CM的异质性,使得snRNA-seq成为心脏SCS的广泛使用的方法。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202308900
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#心力衰竭# #单细胞测序#
162