Cell子刊:恒定自然杀伤T(iNKT)细胞参与肠道神经元和肠道蠕动的激活,改善全身稳态
17小时前 《基因启明》公众号 《基因启明》公众号 发表于上海
此研究详细阐明了iNKT细胞在肠道中的作用机制,包括调节肠道5-HT释放、改善血小板活性、促进肠道蠕动等。
亮点
1.脂质抗原通过肠嗜铬(EC)细胞上的CD1d与恒定自然杀伤T(iNKT)细胞结合,促进外周5-羟色胺(5-HT)释放,从而调节肠道蠕动和止血。
2.肠道化学感应细胞通过CD1d与iNKT细胞接触,选择性感知脂质抗原,调控5-HT释放并调节肠道和全身稳态。
3. iNKT细胞对脂质介导的肠道蠕动至关重要,并且在调控局部和全身神经内分泌反应中扮演了重要角色。
肠道是人体重要的内分泌场所,肠神经系统被认为是肠道不可或缺的组成部分,在受到环境因素刺激后,肠道将其转化为神经内分泌信号,从而维持肠-脑交流;此外,肠道中存在大量微生物群,免疫系统是维护肠道健康和整体代谢活动的重要部分。在肠道组织中,免疫细胞与神经细胞的解剖学位置非常靠近,越来越多的研究表明,肠神经系统与免疫系统的相互作用对于维持肠道微环境稳态、抑制疾病发生及调控疾病预后等多个过程都至关重要。
那么,微生物抗原是如何利用免疫细胞实现内分泌信号传导的呢?
针对这一问题,近期,一项发表在Immunity题为“Lipids regulate peripheral serotonin release via gut CD1d”的研究表明,微生物的脂质抗原能够通过肠嗜铬(EC)细胞上的CD1d,与iNKT细胞结合,促进外周5-羟色胺(5-HT)释放,从而导致肠道神经元和肠道运动的激活,改善全身稳态。

首先介绍一下恒定自然杀伤T(iNKT)细胞。它是T细胞的一个罕见亚群,可以识别依赖CD1d的自身抗原和微生物脂质抗原以实现免疫稳态和宿主防御。在胃肠道内,肠上皮细胞在感染期间将脂质抗原呈递给iNKT细胞,从而导致iNKT细胞活化并释放细胞因子(如干扰素等),进而启动肠道免疫反应。
在肠道炎症过程中,免疫反应通常会通过激活肠蠕动来排出有害物质。基于此,研究人员对结肠炎小鼠腹腔注射α- GalCer(一种合成糖脂,可模拟微生物脂质抗原),发现与对照组小鼠相比,α- GalCer组小鼠的结肠运输时间大大缩短,结肠组织也快速收缩。随后,他们构建了iNKT 细胞缺乏的小鼠模型,以研究肠道蠕动是否依赖于iNKT 细胞。令人惊讶的是,与野生型(WT)小鼠相比,敲除小鼠的菌株肠道转运时间延长,并且结肠组织表现出蠕动收缩受损。这表明iNKT细胞对脂质介导的肠道蠕动至关重要。
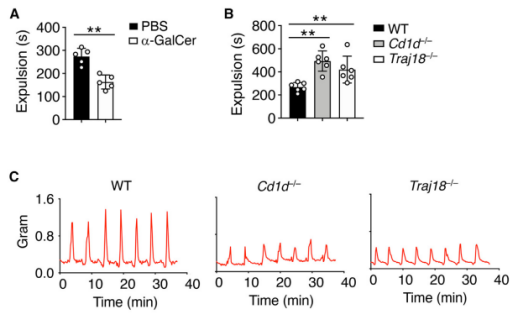
iNKT 细胞调节肠道运动
已有研究表明,免疫刺激能够促进肠嗜铬细胞(EC)衍生的肠源性血清素(5-羟色胺,5-HT)的释放,从而导致肠道神经元和肠道运动的激活。那么,这一过程是否与iNKT调节的肠蠕动有关呢?
针对此想法,研究人员又构建了5-HT缺失小鼠模型,随后腹腔注射a- GalCer,发现与对照小鼠相比,5-HT缺失小鼠肠道转运时间延迟、肠道运动受损。此外,EC细胞中iNKT细胞识别抗原——CD1d的缺失,竟也导致a-GalCer诱导下的肠道运动受损。这表明,脂质抗原与EC细胞中的CD1d结合可诱导5-HT快速释放,随后促进肠道蠕动。
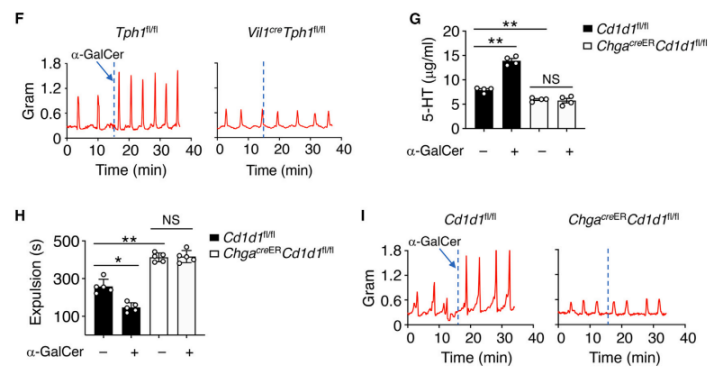
脂质诱导EC细胞分泌5-HT促进肠道运动
已有研究表明,肠源性5-HT主要由血小板吸收,并在损伤部位激活以促进止血。为明确这一过程是否同样依赖于iNKT细胞,研究人员选取iNKT免疫缺陷小鼠并注射a-GalCer,发现与对照组小鼠相比,iNKT免疫缺陷小鼠出血时间延长,活化血小板更少,这表明脂质介导的血小板活性依赖于iNKT细胞,从而调节肠道的凝血功能。
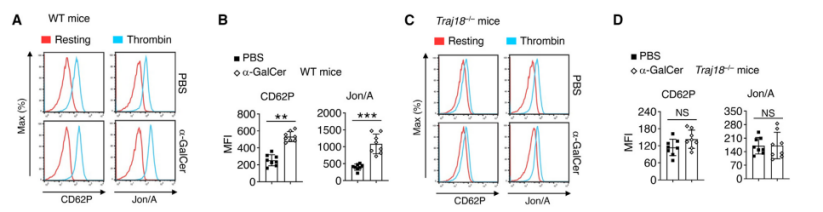
脂质介导的血小板止血功能依赖于iNKT细胞
基于以上结论,研究人员的脑海迸发出一个问题,iNKT细胞为何能够调节5-HT功能呢?他们将目光聚焦在了EC细胞的5-HT释放过程中。
令人意外的是,他们发现当EC细胞与iNKT细胞接触时,施加a-GalCer会在EC细胞中诱发强烈的Ca2+反应,随后Ca2+在邻近的生物传感器细胞中内流,引发5-HT释放。而iNKT细胞的缺失则完全消除了EC细胞和生物传感器细胞中a-GalCer诱导的Ca2+反应。
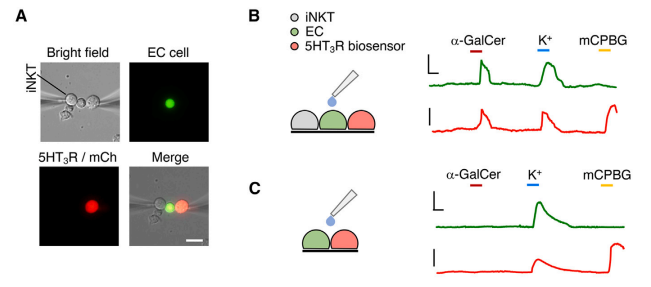
Ca2+反应的代表性图像与轨迹
最后,除了文中提到的脂质a-GalCer,肠道中常见的细菌产物是否真正参与iNKT-EC轴从而释放5-HT呢?为此,研究人员特地构建了脆弱芽孢杆菌突变小鼠模型,以研究脆弱拟杆菌的产物——抑制性鞘脂抗原能否介导iNKT细胞依赖的5-HT反应。不负所望的是,他们惊喜的发现,这种抑制性抗原的突变能够刺激结肠iNKT细胞活性,引发血清5-HT含量升高,并促进小鼠的肠道蠕动!这更加表明,iNKT细胞在调控局部和全身神经内分泌反应中扮演了重要角色。
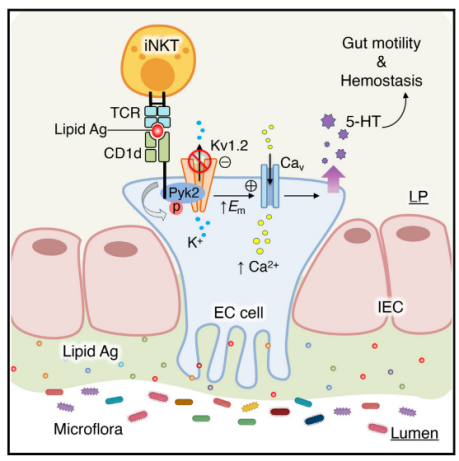
肠腔内容物中的糖脂被识别并通过CD1d与EC细胞连接,从而释放5-HT调节内分泌
综上所述,此研究详细阐明了iNKT细胞在肠道中的作用机制,包括调节肠道5-HT释放、改善血小板活性、促进肠道蠕动等。相信未来,针对iNKT细胞的免疫疗法必将在肠道相关疾病中大放异彩。
来源:
微信公众号: 基因启明
参考文献:
Luo J, Chen Z, Castellano D, Bao B, Han W, Li J, Kim G, An D, Lu W, Wu C. Lipids regulate peripheral serotonin release via gut CD1d. Immunity. 2023 Jul 11;56(7):1533-1547.e7. doi: 10.1016/j.immuni.2023.06.001. Epub 2023 Jun 23. PMID: 37354904; PMCID: PMC10527042.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








好文章,值得一读。
0