Ann. Oncol | 来那替尼和恩美曲妥珠单抗联合治疗HER2阳性脑转移乳腺癌:一项前瞻性临床试验的结果
2024-08-11 daikun MedSci原创 发表于上海
该研究旨在评估来那替尼联合恩美曲妥珠单抗(T-DM1) 在HER2阳性BCBMs患者中的疗效和安全性,来那替尼联合恩美曲妥珠单抗在 HER2阳性BCBMs 患者中表现出一定的颅内活性且安全性可控。
目前HER2阳性乳腺癌脑转移(BCBMs)的治疗选择仍然有限,因为许多治疗药物无法有效穿过血脑屏障进入大脑,这导致BCBMs患者的预后较差,急需新的治疗策略,许多传统化疗药物和靶向药物难以穿过血脑屏障,限制了它们在脑转移瘤中的疗效,随着HER2靶向治疗的广泛应用,耐药性问题逐渐凸显,导致治疗效果下降,目前,仅有少数几种药物被批准用于治疗BCBMs,且疗效有限,亟需探索新的治疗方案,该研究旨在评估来那替尼联合恩美曲妥珠单抗(T-DM1) 在 HER2阳性BCBMs 患者中的疗效和安全性。

方法
这是一项多中心、II期临床试验,共招募了 44 名 HER2阳性BCBMs 患者,分为三个队列:队列 4A:既往未接受过 CNS 治疗的患者;队列 4B:既往接受过 CNS 治疗,但未接受过 T-DM1 的患者;队列 4C:既往接受过 CNS 治疗,并接受过 T-DM1 的患者。所有患者均接受来那替尼 160mg 每日一次口服,以及恩美曲妥珠单抗 3.6mg/kg 静脉注射,每 21 天一次。主要研究终点是每个队列的 CNS 客观缓解率 (ORR),次要终点为CNS 体积缩小率、无进展生存期 (PFS)、总生存期 (OS)和毒性反应。
研究结果
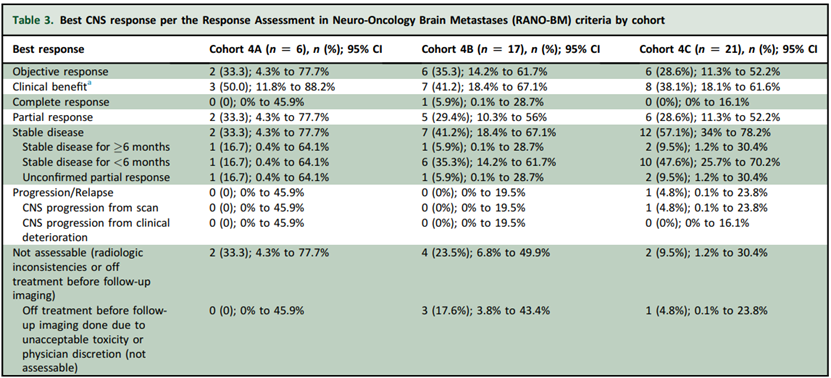
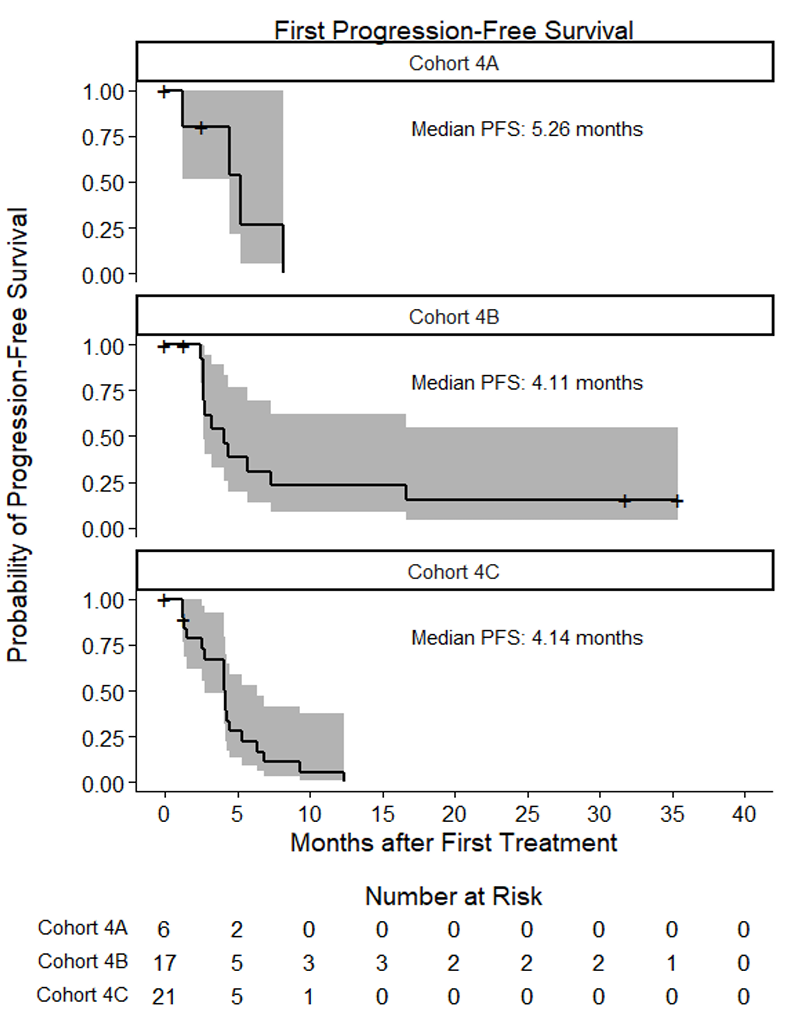
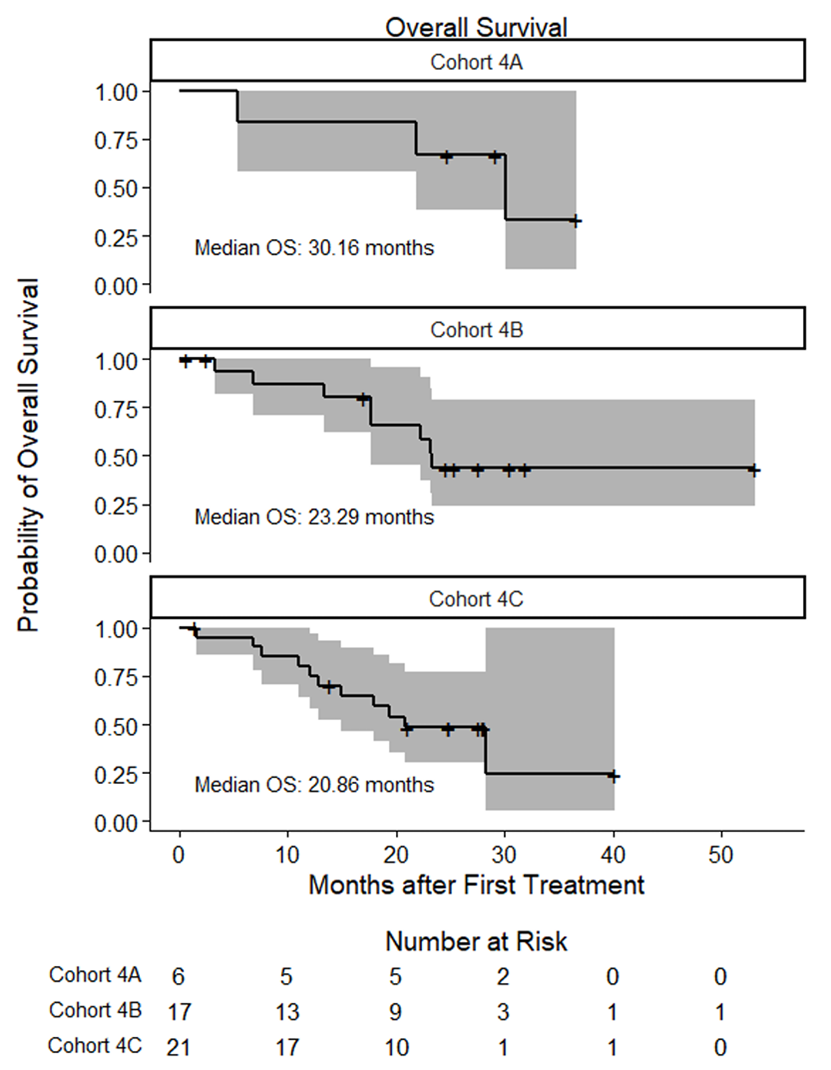
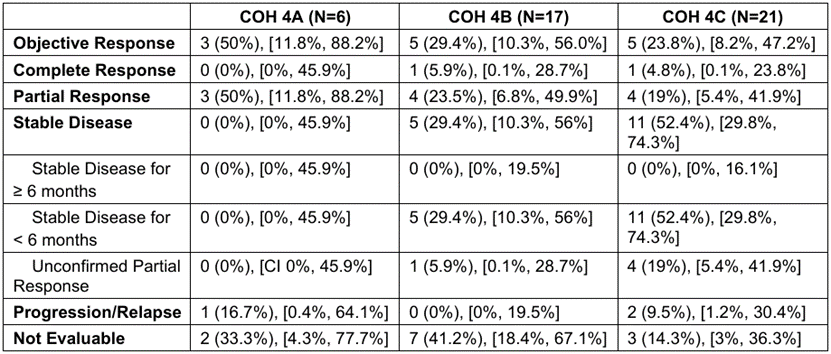
CNS ORR:队列 4A:33.3% (95% CI 4.3% - 77.7%);队列 4B:35.3% (95% CI 14.2% - 61.7%);队列 4C:28.6% (95% CI 11.3% - 52.2%)。CNS 体积缩小率:队列 4A:50% (95% CI 11.8% - 88.2%);队列 4B:29.4% (95% CI 10.3% - 56%);队列 4C:23.8% (95% CI 8.2% - 47.2%)。PFS 和 OS:队列 4A:中位 PFS 为 5.3 个月,中位 OS 为 30.2 个月;队列 4B:中位 PFS 为 4.1 个月,中位 OS 为 23.3 个月;队列 4C:中位 PFS 为 4.1 个月,中位 OS 为 20.9 个月。来那替尼联合恩美曲妥珠单抗在 HER2阳性BCBMs 患者中表现出一定的颅内活性,包括既往接受过恩美曲妥珠单抗治疗的患者。
安全性分析
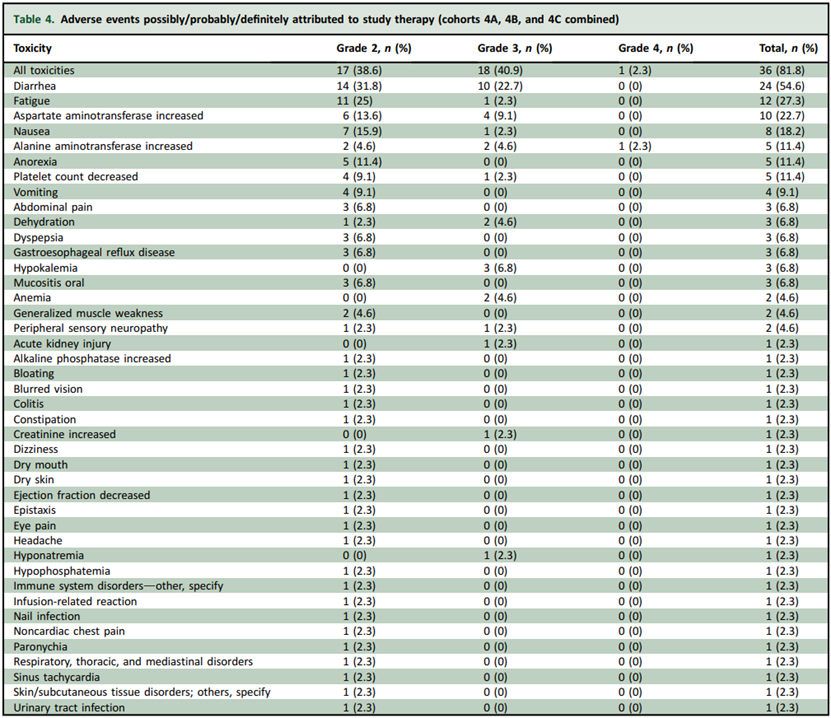
81.8% 的患者报告了可能与治疗相关的不良反应,最常见的2 级不良反应是腹泻 (31.8%) 和疲劳 (27.3%),最常见的3 级不良反应是腹泻 (22.7%) 和转氨酶升高 (13.6%),仅 1 名患者出现 4 级转氨酶升高,无治疗相关死亡事件发生。
结论
来那替尼联合恩美曲妥珠单抗在 HER2阳性BCBMs 患者中表现出一定的颅内活性,包括既往接受过恩美曲妥珠单抗治疗的患者,该联合方案可以延长患者的中位 PFS 和 OS,并提高 12 个月生存率,此外,来那替尼联合恩美曲妥珠单抗的安全性可控,最常见的不良反应是腹泻和疲劳,且可以管理,其他不良反应发生率较低,且可以通过监测和治疗进行管理。该研究为 HER2阳性BCBMs 患者提供了新的治疗选择,尤其是在既往接受过多种治疗的患者中,未来需要进一步研究来那替尼联合恩美曲妥珠单抗的最佳剂量和治疗方案,以降低毒性反应的发生率并提高疗效。
原始出处
Freedman RA, et al. 2024. Neratinib and ado-trastuzumab emtansine for pretreated and untreated human epidermal growth factor receptor 2 (HER2)-positive breast cancer brain metastases: Translational Breast Cancer Research Consortium trial 022. Annals of Oncology.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#来那替尼# #HER2阳性脑转移乳腺癌# #恩美曲妥珠单抗#
30